

Antes da ablação da fibrilhação auricular (FA), recomenda-se 4 semanas de terapêutica anticoagulante para prevenção de tromboembolismo.
Para prevenção de tromboembolismo, recomenda-se 2 meses de terapêutica anticoagulante após a ablação,

A ecocardiografia transesofágica antes da ablação da FA (<24 h) é recomendada apesar de 4 semanas de terapêutica anticoagulante nos seguintes casos:
| ETE antes da ablação – indicações apesar de anticoagulação (4 semanas) |
|---|
| História de ataque isquémico transitório (AIT) |
| História de AVC |
| Utilização irregular de terapêutica anticoagulante |
| INR < 2 (durante terapêutica com varfarina) |
| História de trombo intracardíaco (especialmente no apêndice auricular esquerdo) |
| História de velocidade de esvaziamento do apêndice auricular esquerdo < 20 cm/s |
Antes da ablação da FA, é apropriado suspender a terapêutica antiarrítmica (se a condição do doente o permitir).
Antes da ablação, é apropriado suspender os fármacos antiarrítmicos utilizados para controlo do ritmo (se a condição do doente o permitir), mas não os utilizados para controlo da frequência.
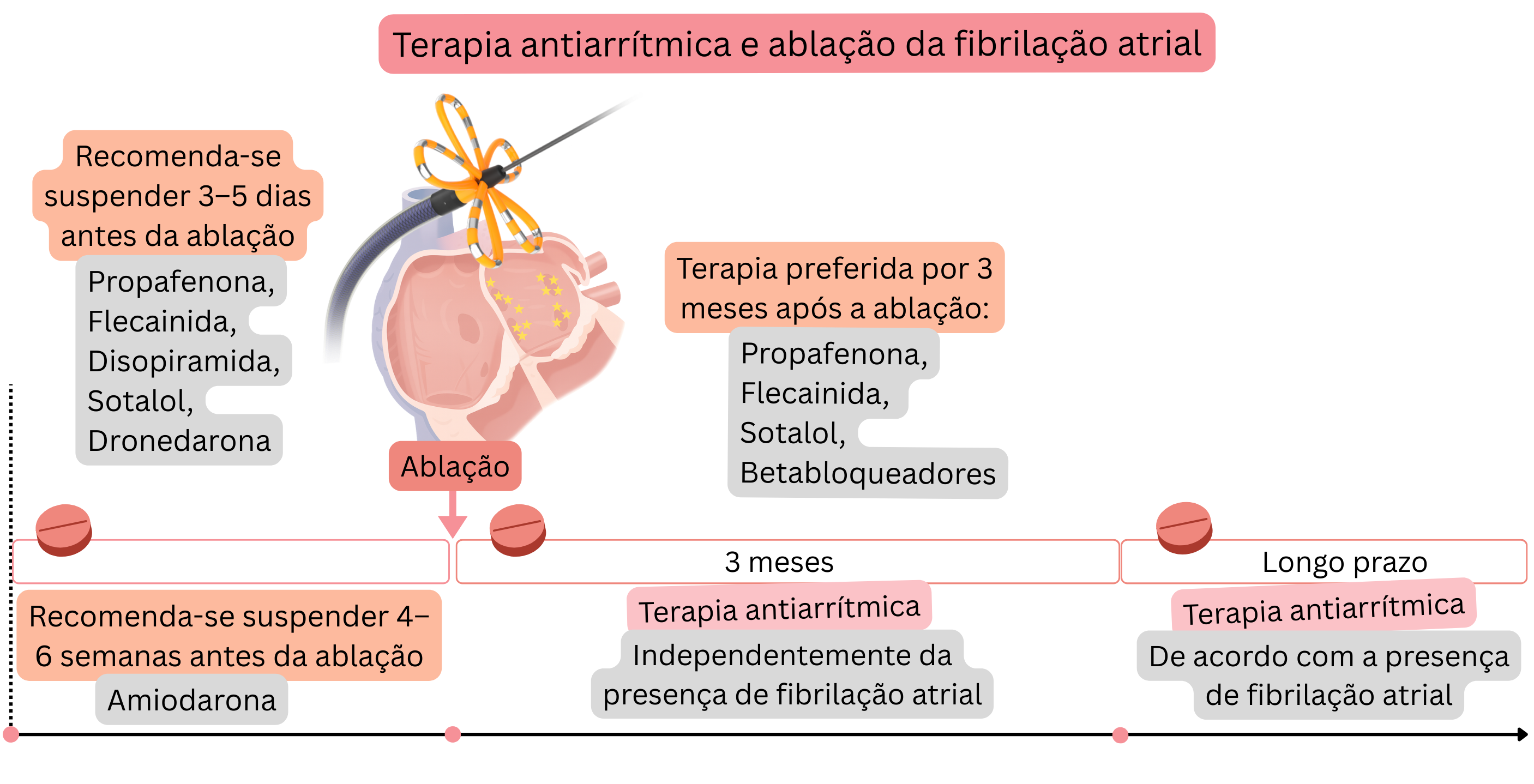
| Suspensão de fármacos antiarrítmicos antes da ablação da fibrilhação auricular | ||
|---|---|---|
| Fármaco | Classe | Suspensão antes da ablação |
| Disopiramida | IA | 3–5 dias |
| Propafenona | IC | 3–5 dias |
| Flecainida | IC | 3–5 dias |
| Sotalol | III | 3–5 dias |
| Amiodarona | III | 4–6 semanas |
| Dronedarona | III | 3–5 dias |
O procedimento de ablação da FA requer 3 acessos vasculares com bainhas através das virilhas (veias femorais):
Após a introdução das bainhas femorais, são administradas 5000 UI de heparina não fracionada (HNF).
| Dose de HNF e prolongamento do ACT | ||
|---|---|---|
| Dose de HNF | ACT a 70 kg (prolongamento em relação ao normal) | ACT a 100 kg (prolongamento em relação ao normal) |
| Sem HNF | 80 – 120 s | 80 – 120 s |
| 1000 UI | 120 – 140 s (↑20–40) | 110 – 130 s (↑10–30) |
| 3000 UI | 150 – 180 s (↑50–80) | 130 – 160 s (↑30–60) |
| 5000 UI | 200 – 240 s (↑100–140) | 170 – 210 s (↑70–110) |
| 7000 UI | 230 – 280 s (↑130–180) | 200 – 250 s (↑100–150) |
| 10000 UI | 280 – 340 s (↑180–240) | 230 – 300 s (↑130–200) |
Um trombo na região das bainhas venosas e na aurícula direita no cateter não é tão perigoso, pois emboliza para os pulmões.
| Risco de formação de trombo na bainha ou no cateter | |
|---|---|
| ACT | Risco estimado |
| 80 – 120 s (sem HNF) | 10–20 % (em 10–20 min.) |
| 250–300 s | 1–2 % |
| 300–350 s | < 1 % |
Após introdução de uma agulha dedicada através da veia femoral para a aurícula direita, é realizada uma punção transeptal.
ACT e HNF durante o procedimento
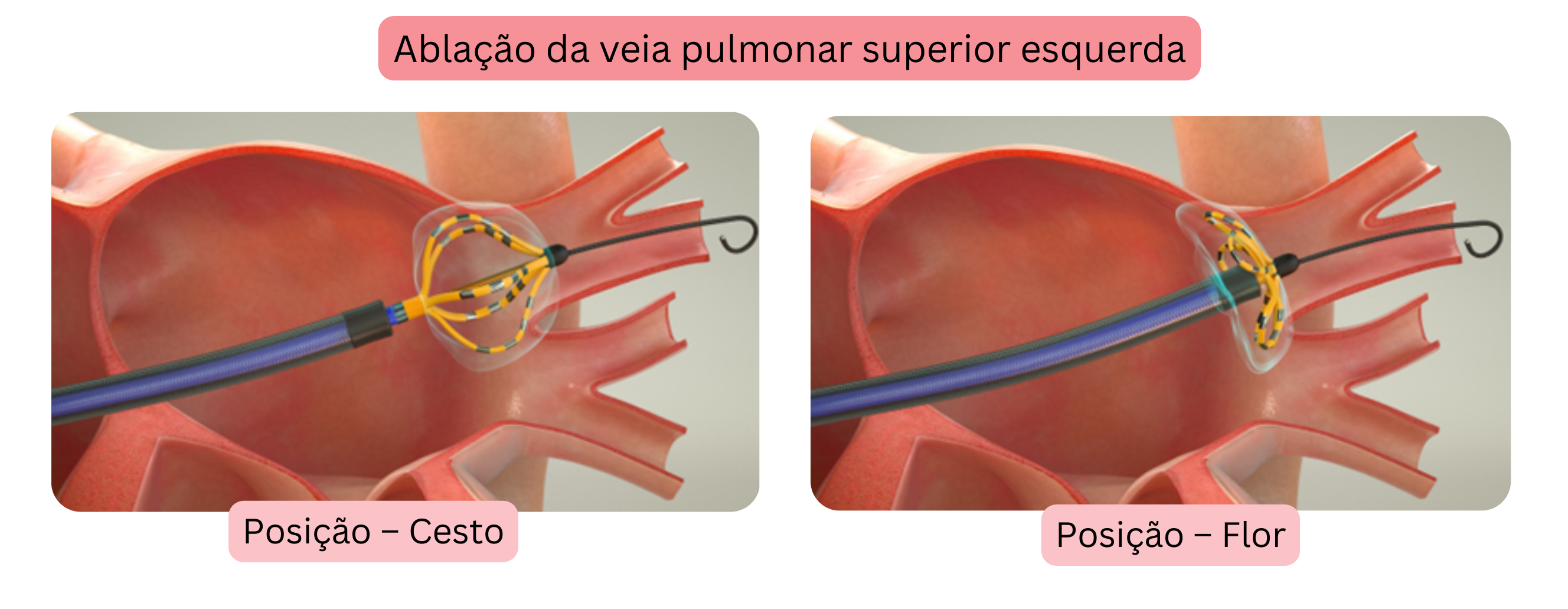
Farawave é um cateter dedicado com duas configurações: cesto e flor.
3–5 min antes da primeira aplicação, é administrada 1 mg de atropina por via intravenosa (pode ser repetida até uma dose máxima de 3 mg).
| Atropina – prevenção de bradicardia antes da ablação | |
|---|---|
| Objetivo | Prevenção de bradicardia |
| Mecanismo | Bloqueia o efeito vagal (efeito antimuscarínico) |
| Dose | 1 mg por via intravenosa (máx. 3 mg) |
| Início de ação | 1–2 min |
| Efeito esperado | Aumento da frequência cardíaca em 20–40/min |
| Duração de ação | 30–60 min |
| Contraindicação | Glaucoma |
Os impulsos elétricos são dolorosos; por isso, são administrados sob anestesia geral ou sedação.
Se a FA persistir após o isolamento das veias pulmonares, é realizada uma ablação mais extensa da aurícula esquerda:
Apêndice auricular esquerdo e ablação.
Se um doente tiver FA e flutter auricular (AFL),
Durante a emissão de pulsos na ablação de FA e AFL, pode ocorrer espasmo coronário se a ablação for realizada próximo de uma artéria coronária.
| Prevenção de espasmo coronário antes da ablação – Isoket vs. nitroglicerina | ||
|---|---|---|
| Fármaco | Isoket (dinitrato de isossorbida) | Nitroglicerina |
| Objetivo | Prevenção de espasmo coronário mais lenta e de maior duração | Prevenção e tratamento rápidos do espasmo coronário |
| Mecanismo de ação | Dador de NO → vasodilatação coronária | Dador de NO → vasodilatação coronária |
| Administração | bólus por via intravenosa 1–2 mg | bólus por via intravenosa 50–200 µg |
| Início de ação | 3–5 min | 1–2 min |
| Duração de ação | 30–60 min | 5–10 min |
| Risco de hipotensão | Mais elevado (maior duração) | Mais baixo (curta duração) |
Alterações ECG durante ablação na região do istmo mitral e tricúspide:
Os impulsos elétricos na ablação por campo pulsado são cardioseletivos:
| Impulsos elétricos na ablação por campo pulsado |
|---|
| Não causam estenose das veias pulmonares |
| Não causam fístula átrio-esofágica |
| Não causam lesão do nervo frénico |
Após a ablação da FA, o sucesso do procedimento pode ser verificado de três formas:
| Verificação do sucesso da ablação da fibrilhação auricular | |||
|---|---|---|---|
| Método | Local de estimulação | O que é avaliado | Sucesso |
| Estimulação a partir das veias pulmonares | Sequencialmente a partir de cada veia pulmonar (utilizando o cateter Farawave) | Se os impulsos provenientes da veia se propagam para a aurícula esquerda | Sem resposta auricular = veia isolada |
| Estimulação em rajadas | A partir do seio coronário (cateter do SC) | Indução de FA após rajadas (8–10 estímulos) | FA não é induzida ou FA não dura > 1 min = sucesso |
| Estimulação em rampa | A partir do seio coronário (cateter do SC) | Se a FA é induzida durante estimulação com encurtamento progressivo do comprimento de ciclo | FA não é induzida ou FA não dura > 1 min = sucesso |
Durante a ablação por campo pulsado, ocorre eletroporação dos cardiomiócitos, que é a perfuração da membrana celular por um campo elétrico. Isto é seguido de apoptose. Enzimas cardioespecíficas são libertadas dos cardiomiócitos danificados e aumentam para níveis elevados em 24 h.
| Enzimas cardioespecíficas nas 24 h após ablação por campo pulsado | |
|---|---|
| Enzima | Valor |
| Troponina | 1500 ng/l (±500) |
| CK | 300 ng/l (±100) |
| CK-MB | 35 mg/l (±10) |
Durante a ablação por campo pulsado, ocorre hemólise, que se manifesta após o procedimento como hematúria macroscópica.
O sucesso da ablação é avaliado pela presença de recorrência de FA no prazo de 1 ano após a ablação.
| Sucesso da ablação da fibrilhação auricular (em 12 meses) | |
|---|---|
| Classificação da FA | Sucesso |
| FA paroxística | 66–82 % |
| FA persistente | 56–72 % |
Período de blanking

| Terapêutica durante o período de blanking (3 meses após a ablação) | ||
|---|---|---|
| Terapêutica | Duração | Nota |
| Fármacos antiarrítmicos | 3 meses | Administrados independentemente de estar presente ritmo sinusal ou FA. |
| Terapêutica anticoagulante | 2 meses | Administrada independentemente do score CHA2DS2-VA |
Na recorrência de FA após ablação—isolamento das veias pulmonares (com energia de campo pulsado), pode ocorrer reconexão de uma veia pulmonar à aurícula esquerda. A reconexão ocorre mais frequentemente em:
Durante e após a ablação da FA por campo pulsado, podem ocorrer complicações, mas são muito raras. A incidência de complicações é:
As complicações major e minor estão listadas na tabela seguinte:
| Complicações major da ablação por campo pulsado | |
|---|---|
| Total | 0,98 % |
| Tamponamento pericárdico | 0,36 % |
| Complicação vascular (necessitando intervenção) | 0,30 % |
| Espasmo coronário | 0,14 % |
| AVC | 0,12 % |
| Hemólise com insuficiência renal aguda | 0,03 % |
| Morte | 0,03 % |
| Outros (trombose, embolia aérea coronária) | 0,006 % |
| Fístula esofágica | 0 % |
| Estenose das veias pulmonares | 0 % |
| Lesão do nervo frénico (permanente) | 0 % |
| Complicações minor da ablação por campo pulsado | |
|---|---|
| Total | 3,21 % |
| Complicações vasculares (sem necessidade de intervenção) | 2,20 % |
| Derrame pericárdico (sem necessidade de intervenção) | 0,33 % |
| Outras complicações minor (hematomas, arritmias) | 0,32 % |
| Pericardite | 0,17 % |
| Ataque isquémico transitório | 0,12 % |
| Lesão do nervo frénico (temporária) | 0,06 % |
Em 5–15% dos doentes, ocorre isquemia cerebral silenciosa assintomática durante a ablação por campo pulsado.
| Ablação da fibrilhação auricular | Classe |
|---|---|
| A ablação por campo pulsado (e não radiofrequência ou crioblação) é recomendada como método preferencial de ablação da fibrilhação auricular. | I |
A ablação por campo pulsado é recomendada em doentes com fibrilhação auricular paroxística ou persistente se a fibrilhação auricular for sintomática:
|
I |
| A ablação por campo pulsado é recomendada em doentes com cardiomiopatia induzida por taquicardia devido a fibrilhação auricular. | I |
| A ablação por campo pulsado deve ser considerada em doentes com fibrilhação auricular que apresentam pausas pré-automáticas sintomáticas. | IIa |
Na recorrência de fibrilhação auricular, a ablação por campo pulsado pode ser repetida (não antes de 3 meses) se a fibrilhação auricular for sintomática:
|
IIa |
| Antes da ablação da fibrilhação auricular, deve ser considerada angio-TC ou angio-RM da aurícula esquerda e das veias pulmonares para avaliação da anatomia das veias pulmonares. | IIa |
A estratégia “pace and ablate” pode ser considerada em doentes com fibrilhação auricular sintomática em que falharam:
|
IIa |
| Terapêutica anticoagulante e ablação da fibrilhação auricular | Classe |
|---|---|
| Recomenda-se terapêutica anticoagulante durante pelo menos 4 semanas antes da ablação da fibrilhação auricular, independentemente do score CHA₂DS₂-VA. | I |
| Recomenda-se que a terapêutica anticoagulante com NOAC não seja tomada na manhã do dia da ablação da fibrilhação auricular. | I |
| Recomenda-se iniciar a terapêutica anticoagulante com NOAC 6 h após a ablação da fibrilhação auricular se não houver sinais de hemorragia. | I |
| Durante terapêutica com varfarina, recomenda-se que a ablação da fibrilhação auricular seja realizada com INR terapêutico de aproximadamente 2,0 no dia do procedimento. | I |
| Recomenda-se terapêutica anticoagulante nos primeiros 2 meses após a ablação da fibrilhação auricular, independentemente do sucesso da ablação e independentemente do score CHA₂DS₂-VA. | I |
| Dois meses após a ablação da fibrilhação auricular, está indicada anticoagulação a longo prazo de acordo com o score CHA₂DS₂-VA, independentemente do sucesso da ablação. | I |
| Recomenda-se terapêutica antiarrítmica (propafenona, flecainida, sotalol, betabloqueadores) nos primeiros 3 meses após a ablação da fibrilhação auricular, independentemente do sucesso da ablação. | I |
| Três meses após a ablação da fibrilhação auricular, a terapêutica antiarrítmica é indicada de acordo com a recorrência de fibrilhação auricular. | I |
| A ablação da fibrilhação auricular pode ser considerada se o doente estiver a receber terapêutica antitrombótica dupla (p.ex., NOAC + clopidogrel). | IIa |
| Ablação da fibrilhação auricular durante cirurgia cardíaca | Classe |
|---|---|
| Num doente submetido a cirurgia cardíaca da válvula mitral, recomenda-se ablação cirúrgica concomitante da fibrilhação auricular utilizando o procedimento Cox-Maze IV. | I |
| Num doente submetido a cirurgia cardíaca diferente de cirurgia da válvula mitral, a ablação cirúrgica concomitante da fibrilhação auricular utilizando o procedimento Cox-Maze IV deve ser considerada. | IIa |
| Durante cirurgia cardíaca, recomenda-se excluir a presença de trombo na aurícula esquerda antes de ablação cirúrgica da fibrilhação auricular. | I |
Estas diretrizes são não oficiais e não representam diretrizes formais emitidas por qualquer sociedade profissional de cardiologia. Destinam-se apenas a fins educacionais e informativos.
