

Antes de la ablación de la fibrilación auricular (FA), se recomiendan 4 semanas de tratamiento anticoagulante como prevención del tromboembolismo.
Para la prevención del tromboembolismo, se recomiendan 2 meses de tratamiento anticoagulante tras la ablación,
Se recomienda ecocardiografía transesofágica antes de la ablación de FA (<24 h) a pesar de 4 semanas de tratamiento anticoagulante en los siguientes casos:
| ETE antes de la ablación – indicaciones a pesar de anticoagulación (4 semanas) |
|---|
| Antecedentes de ataque isquémico transitorio (AIT) |
| Antecedentes de ictus |
| Uso irregular del tratamiento anticoagulante |
| INR < 2 (durante tratamiento con warfarina) |
| Antecedentes de trombo intracardíaco (especialmente en la orejuela auricular izquierda) |
| Antecedentes de velocidad de vaciamiento de la orejuela auricular izquierda < 20 cm/s |
Antes de la ablación de FA, es apropiado suspender el tratamiento antiarrítmico (si la situación del paciente lo permite).
Antes de la ablación, es apropiado suspender los fármacos antiarrítmicos utilizados para el control del ritmo (si la situación del paciente lo permite), pero no los utilizados para el control de la frecuencia.

| Suspensión de fármacos antiarrítmicos antes de la ablación de fibrilación auricular | ||
|---|---|---|
| Fármaco | Clase | Suspensión antes de la ablación |
| Disopiramida | IA | 3–5 días |
| Propafenona | IC | 3–5 días |
| Flecainida | IC | 3–5 días |
| Sotalol | III | 3–5 días |
| Amiodarona | III | 4–6 semanas |
| Dronedarona | III | 3–5 días |
La ablación de FA (procedimiento) requiere 3 introductores de acceso vascular por las ingles (venas femorales):
Tras la inserción de los introductores femorales, se administran 5000 UI de heparina no fraccionada (HNF).
| Dosis de HNF y prolongación del ACT | ||
|---|---|---|
| Dosis de HNF | ACT a 70 kg (prolongación desde lo normal) | ACT a 100 kg (prolongación desde lo normal) |
| Sin HNF | 80 – 120 s | 80 – 120 s |
| 1000 UI | 120 – 140 s (↑20–40) | 110 – 130 s (↑10–30) |
| 3000 UI | 150 – 180 s (↑50–80) | 130 – 160 s (↑30–60) |
| 5000 UI | 200 – 240 s (↑100–140) | 170 – 210 s (↑70–110) |
| 7000 UI | 230 – 280 s (↑130–180) | 200 – 250 s (↑100–150) |
| 10000 UI | 280 – 340 s (↑180–240) | 230 – 300 s (↑130–200) |
Un trombo en la región de los introductores venosos y en la aurícula derecha sobre el catéter no es tan peligroso, ya que emboliza hacia los pulmones.
| Riesgo de formación de trombo en el introductor o el catéter | |
|---|---|
| ACT | Riesgo estimado |
| 80 – 120 s (sin HNF) | 10–20 % (en 10–20 min.) |
| 250–300 s | 1–2 % |
| 300–350 s | < 1 % |
Tras introducir una aguja específica por la vena femoral hasta la aurícula derecha, se realiza una punción transeptal.
ACT y HNF durante el procedimiento

Farawave es un catéter específico con dos configuraciones: cesta y flor.
3–5 min antes de la primera aplicación, se administra 1 mg de atropina por vía intravenosa (puede repetirse hasta una dosis máxima de 3 mg).
| Atropina – prevención de bradicardia antes de la ablación | |
|---|---|
| Objetivo | Prevención de la bradicardia |
| Mecanismo | Bloquea el efecto vagal (efecto antimuscarínico) |
| Dosis | 1 mg intravenosa (máx. 3 mg) |
| Inicio de acción | 1–2 min |
| Efecto esperado | Aumento de la frecuencia cardiaca en 20–40/min |
| Duración de acción | 30–60 min |
| Contraindicación | Glaucoma |
Los impulsos eléctricos son dolorosos; por lo tanto, se administran bajo anestesia general o sedación.
Si la FA persiste tras el aislamiento de las venas pulmonares, se realiza una ablación más extensa de la aurícula izquierda:
Orejuela auricular izquierda y ablación.
Si un paciente tiene FA y flúter auricular (AFl),
Durante el pulso en la ablación de FA y AFl, puede ocurrir espasmo coronario si la ablación se realiza cerca de una arteria coronaria.
| Prevención del espasmo coronario antes de la ablación – Isoket vs. nitroglicerina | ||
|---|---|---|
| Fármaco | Isoket (dinitrato de isosorbida) | Nitroglicerina |
| Objetivo | Prevención del espasmo coronario más lenta y de mayor duración | Prevención y tratamiento rápido del espasmo coronario |
| Mecanismo de acción | Donador de NO → vasodilatación coronaria | Donador de NO → vasodilatación coronaria |
| Administración | bolo intravenoso 1–2 mg | bolo intravenoso 50–200 µg |
| Inicio de acción | 3–5 min | 1–2 min |
| Duración de acción | 30–60 min | 5–10 min |
| Riesgo de hipotensión | Mayor (duración más prolongada) | Menor (duración corta) |
Cambios en el ECG durante la ablación en la región del istmo mitral y tricuspídeo:
Los impulsos eléctricos en la ablación por campo pulsado son cardioselectivos:
| Impulsos eléctricos en la ablación por campo pulsado |
|---|
| No causan estenosis de las venas pulmonares |
| No causan fístula auriculoesofágica |
| No causan lesión del nervio frénico |
Tras la ablación de FA, el éxito del procedimiento puede verificarse de tres maneras:
| Verificación del éxito de la ablación de fibrilación auricular | |||
|---|---|---|---|
| Método | Sitio de estimulación | Qué se evalúa | Éxito |
| Estimulación desde las venas pulmonares | Secuencialmente desde cada vena pulmonar (utilizando el catéter Farawave) | Si los impulsos desde la vena se propagan a la aurícula izquierda | Sin respuesta auricular = vena aislada |
| Estimulación en ráfaga | Desde el seno coronario (catéter del SC) | Inducción de FA tras ráfagas (8–10 estímulos) | No se induce FA o la FA no dura > 1 min = éxito |
| Estimulación en rampa | Desde el seno coronario (catéter del SC) | Si se induce FA durante la estimulación con acortamiento progresivo del ciclo | No se induce FA o la FA no dura > 1 min = éxito |
Durante la ablación por campo pulsado se produce electroporación de cardiomiocitos, que es la perforación de la membrana celular por un campo eléctrico. Esto va seguido de apoptosis. Las enzimas cardioespecíficas se liberan desde los cardiomiocitos dañados y aumentan a niveles elevados en 24 h.
| Enzimas cardioespecíficas dentro de las 24 h tras la ablación por campo pulsado | |
|---|---|
| Enzima | Valor |
| Troponina | 1500 ng/l (±500) |
| CK | 300 ng/l (±100) |
| CK-MB | 35 mg/l (±10) |
Durante la ablación por campo pulsado se produce hemólisis, que se manifiesta tras el procedimiento como hematuria macroscópica.
El éxito de la ablación se evalúa por la presencia de recurrencia de FA en 1 año tras la ablación.
| Éxito de la ablación de fibrilación auricular (en 12 meses) | |
|---|---|
| Clasificación de la FA | Éxito |
| FA paroxística | 66–82 % |
| FA persistente | 56–72 % |
Periodo de blanking

| Tratamiento durante el periodo de blanking (3 meses tras la ablación) | ||
|---|---|---|
| Tratamiento | Duración | Nota |
| Fármacos antiarrítmicos | 3 meses | Se administran independientemente de si hay ritmo sinusal o FA. |
| Tratamiento anticoagulante | 2 meses | Se administra independientemente de la puntuación CHA2DS2-VA |
En la recurrencia de FA tras la ablación—aislamiento de venas pulmonares (con energía de campo pulsado), puede producirse reconexión de una vena pulmonar con la aurícula izquierda. La reconexión ocurre con mayor frecuencia en:
Durante y después de la ablación de FA por campo pulsado pueden ocurrir complicaciones, pero son muy raras. La incidencia de complicaciones es:
Las complicaciones mayores y menores se enumeran en la siguiente tabla:
| Complicaciones mayores de la ablación por campo pulsado | |
|---|---|
| Total | 0,98 % |
| Taponamiento pericárdico | 0,36 % |
| Complicación vascular (que requiere intervención) | 0,30 % |
| Espasmo coronario | 0,14 % |
| Ictus | 0,12 % |
| Hemólisis con insuficiencia renal aguda | 0,03 % |
| Muerte | 0,03 % |
| Otros (trombosis, embolia aérea coronaria) | 0,006 % |
| Fístula esofágica | 0 % |
| Estenosis de venas pulmonares | 0 % |
| Lesión del nervio frénico (permanente) | 0 % |
| Complicaciones menores de la ablación por campo pulsado | |
|---|---|
| Total | 3,21 % |
| Complicaciones vasculares (sin necesidad de intervención) | 2,20 % |
| Derrame pericárdico (sin necesidad de intervención) | 0,33 % |
| Otras complicaciones menores (hematomas, arritmias) | 0,32 % |
| Pericarditis | 0,17 % |
| Ataque isquémico transitorio | 0,12 % |
| Lesión del nervio frénico (transitoria) | 0,06 % |
En el 5–15% de los pacientes, se produce isquemia cerebral silenciosa asintomática durante la ablación por campo pulsado.
| Ablación de la fibrilación auricular | Clase |
|---|---|
| Se recomienda la ablación por campo pulsado (no radiofrecuencia ni crioablación) como método preferido de ablación de la fibrilación auricular. | I |
Se recomienda la ablación por campo pulsado en pacientes con fibrilación auricular paroxística o persistente si la fibrilación auricular es sintomática:
|
I |
| Se recomienda la ablación por campo pulsado en pacientes con miocardiopatía inducida por taquicardia debida a fibrilación auricular. | I |
| Debe considerarse la ablación por campo pulsado en pacientes con fibrilación auricular que presentan pausas preautomáticas sintomáticas. | IIa |
En la recurrencia de fibrilación auricular, la ablación por campo pulsado puede repetirse (no antes de 3 meses) si la fibrilación auricular es sintomática:
|
IIa |
| Antes de la ablación de fibrilación auricular, debe considerarse angio-TC o angio-RM de la aurícula izquierda y las venas pulmonares para evaluar la anatomía de las venas pulmonares. | IIa |
La estrategia “pace and ablate” puede considerarse en pacientes con fibrilación auricular sintomática en los que han fracasado:
|
IIa |
| Tratamiento anticoagulante y ablación de la fibrilación auricular | Clase |
|---|---|
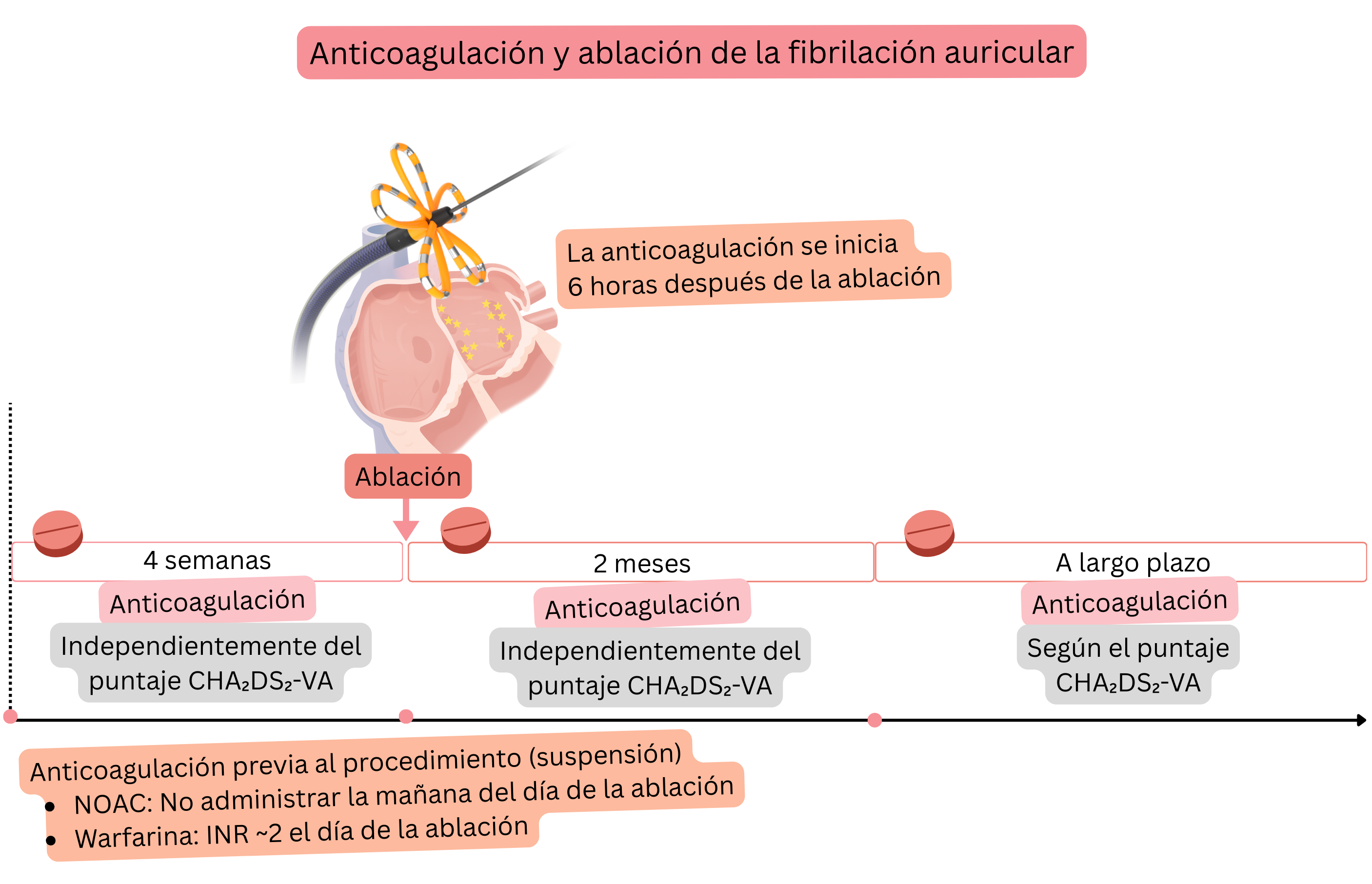
| Se recomienda tratamiento anticoagulante durante al menos 4 semanas antes de la ablación de fibrilación auricular, independientemente de la puntuación CHA₂DS₂-VA. | I |
| Se recomienda no tomar el tratamiento anticoagulante con ACOD por la mañana el día de la ablación de fibrilación auricular. | I |
| Se recomienda reiniciar el tratamiento anticoagulante con ACOD 6 h después de la ablación de fibrilación auricular si no hay signos de sangrado. | I |
| Durante tratamiento con warfarina, se recomienda realizar la ablación de fibrilación auricular con un INR terapéutico de aproximadamente 2,0 el día del procedimiento. | I |
| Se recomienda tratamiento anticoagulante durante los primeros 2 meses tras la ablación de fibrilación auricular, independientemente del éxito de la ablación e independientemente de la puntuación CHA₂DS₂-VA. | I |
| Dos meses después de la ablación de fibrilación auricular, la anticoagulación a largo plazo está indicada según la puntuación CHA₂DS₂-VA, independientemente del éxito de la ablación. | I |
| Se recomienda tratamiento antiarrítmico (propafenona, flecainida, sotalol, betabloqueantes) durante los primeros 3 meses tras la ablación de fibrilación auricular, independientemente del éxito de la ablación. | I |
| Tres meses después de la ablación de fibrilación auricular, el tratamiento antiarrítmico está indicado según la recurrencia de fibrilación auricular. | I |
| Puede considerarse la ablación de fibrilación auricular si el paciente está recibiendo tratamiento antitrombótico dual (p. ej., ACOD + clopidogrel). | IIa |
| Ablación de la fibrilación auricular durante cirugía cardiaca | Clase |
|---|---|
| En un paciente sometido a cirugía cardiaca sobre la válvula mitral, se recomienda la ablación quirúrgica concomitante de fibrilación auricular mediante el procedimiento Cox-Maze IV. | I |
| En un paciente sometido a cirugía cardiaca distinta de la cirugía valvular mitral, debe considerarse la ablación quirúrgica concomitante de fibrilación auricular mediante el procedimiento Cox-Maze IV. | IIa |
| Durante la cirugía cardiaca, se recomienda excluir la presencia de trombo en la aurícula izquierda antes de la ablación quirúrgica de fibrilación auricular. | I |
Estas guías son no oficiales y no representan guías formales emitidas por ninguna sociedad profesional de cardiología. Están destinadas únicamente a fines educativos e informativos.
