

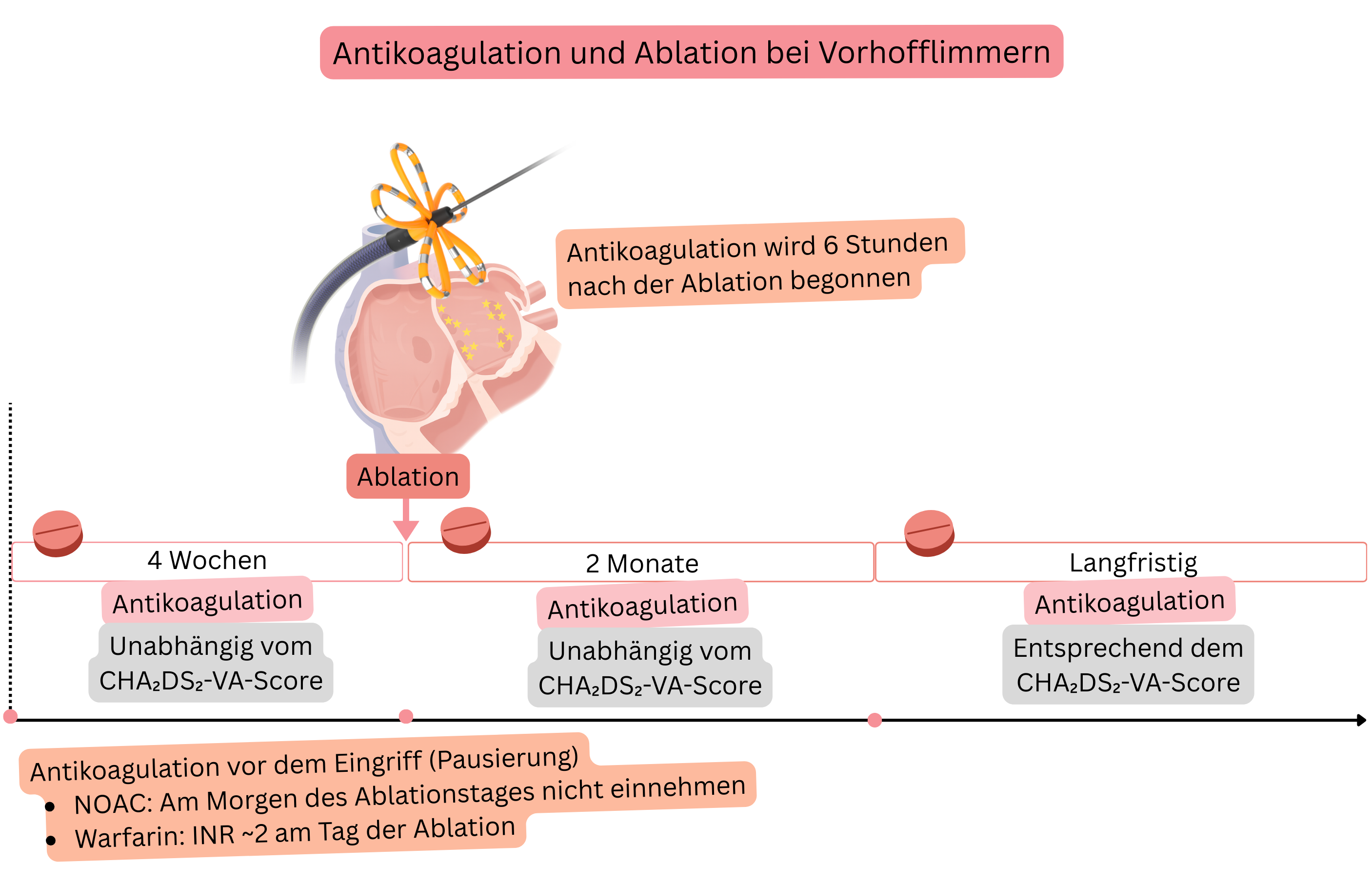
Vor einer Ablation des Vorhofflimmerns (VHF) wird eine Antikoagulationstherapie über 4 Wochen zur Prävention von Thromboembolien empfohlen.
Zur Prävention von Thromboembolien wird nach der Ablation eine Antikoagulationstherapie über 2 Monate empfohlen,
Eine transösophageale Echokardiographie vor VHF-Ablation (<24 h) wird trotz 4-wöchiger Antikoagulationstherapie in folgenden Fällen empfohlen:
| TEE vor Ablation – Indikationen trotz Antikoagulation (4 Wochen) |
|---|
| Anamnese einer transitorisch ischämischen Attacke (TIA) |
| Anamnese eines Schlaganfalls |
| Unregelmäßige Einnahme der Antikoagulationstherapie |
| INR < 2 (unter Warfarintherapie) |
| Anamnese eines intrakardialen Thrombus (insbesondere im linken Vorhofohr) |
| Anamnese einer Entleerungsgeschwindigkeit des linken Vorhofohrs < 20 cm/s |
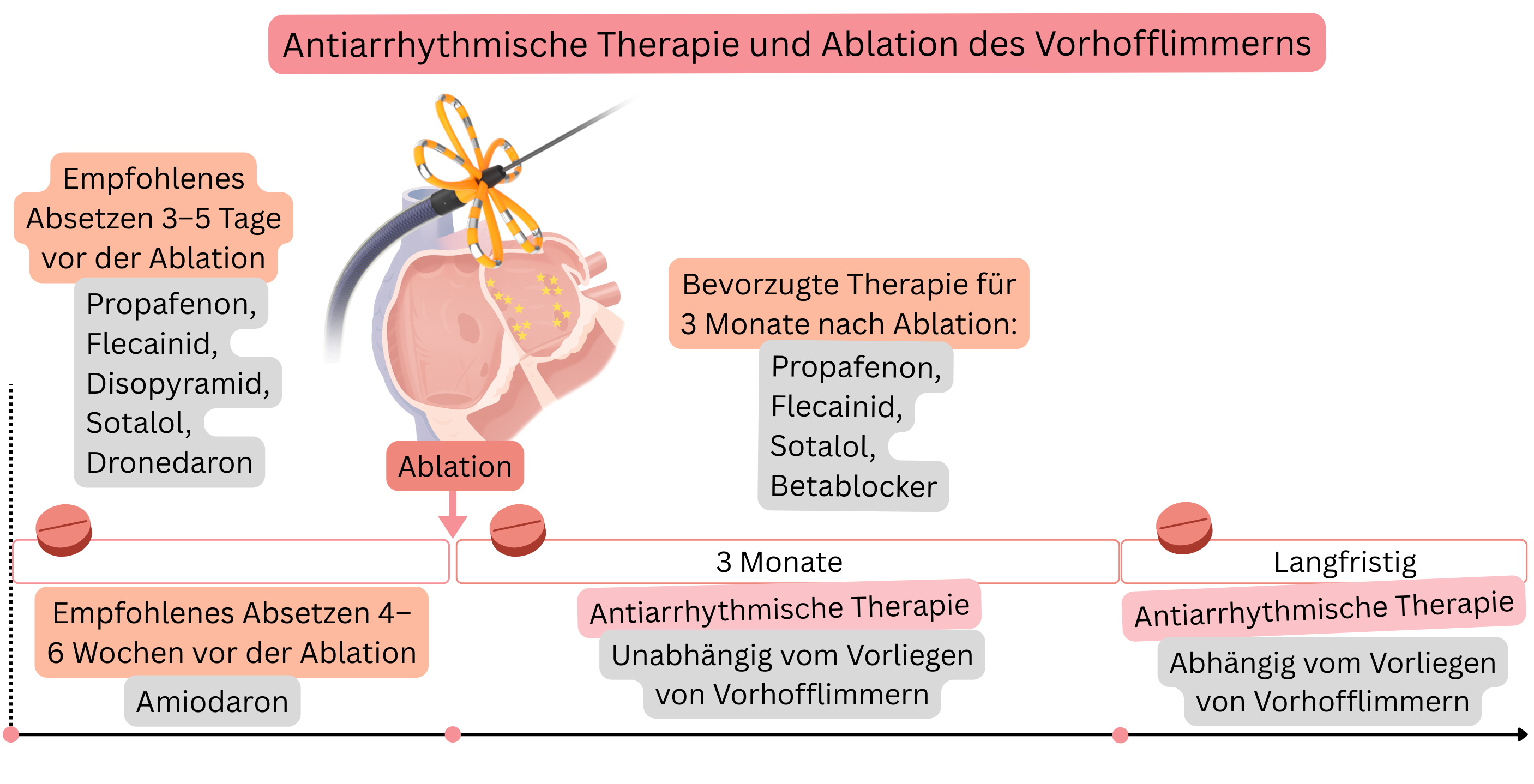
Vor einer VHF-Ablation ist es sinnvoll, die antiarrhythmische Therapie (sofern der Zustand des Patienten dies erlaubt) abzusetzen.
Vor der Ablation ist es sinnvoll, antiarrhythmische Medikamente zur Rhythmuskontrolle (sofern der Zustand des Patienten dies erlaubt) abzusetzen, nicht jedoch solche zur Frequenzkontrolle.
| Absetzen antiarrhythmischer Medikamente vor Ablation des Vorhofflimmerns | ||
|---|---|---|
| Medikament | Klasse | Absetzen vor Ablation |
| Disopyramid | IA | 3–5 Tage |
| Propafenon | IC | 3–5 Tage |
| Flecainid | IC | 3–5 Tage |
| Sotalol | III | 3–5 Tage |
| Amiodaron | III | 4–6 Wochen |
| Dronedaron | III | 3–5 Tage |
Die VHF-Ablation (Prozedur) erfordert 3 vaskuläre Zugangsschleusen über die Leisten (Vv. femorales):
Nach Einbringen der femoralen Schleusen werden 5000 I.E. unfraktioniertes Heparin (UFH) verabreicht.
| UFH-Dosis und ACT-Verlängerung | ||
|---|---|---|
| UFH-Dosis | ACT bei 70 kg (Verlängerung gegenüber normal) | ACT bei 100 kg (Verlängerung gegenüber normal) |
| Kein UFH | 80 – 120 s | 80 – 120 s |
| 1000 I.E. | 120 – 140 s (↑20–40) | 110 – 130 s (↑10–30) |
| 3000 I.E. | 150 – 180 s (↑50–80) | 130 – 160 s (↑30–60) |
| 5000 I.E. | 200 – 240 s (↑100–140) | 170 – 210 s (↑70–110) |
| 7000 I.E. | 230 – 280 s (↑130–180) | 200 – 250 s (↑100–150) |
| 10000 I.E. | 280 – 340 s (↑180–240) | 230 – 300 s (↑130–200) |
Ein Thrombus im Bereich der venösen Schleusen und im rechten Vorhof am Katheter ist weniger gefährlich, da er in die Lunge embolisiert.
| Risiko der Thrombusbildung an Schleuse oder Katheter | |
|---|---|
| ACT | Geschätztes Risiko |
| 80 – 120 s (kein UFH) | 10–20 % (innerhalb von 10–20 min.) |
| 250–300 s | 1–2 % |
| 300–350 s | < 1 % |
Nach Einbringen einer speziellen Nadel über die V. femoralis in den rechten Vorhof erfolgt die transseptale Punktion.
ACT und UFH während der Prozedur
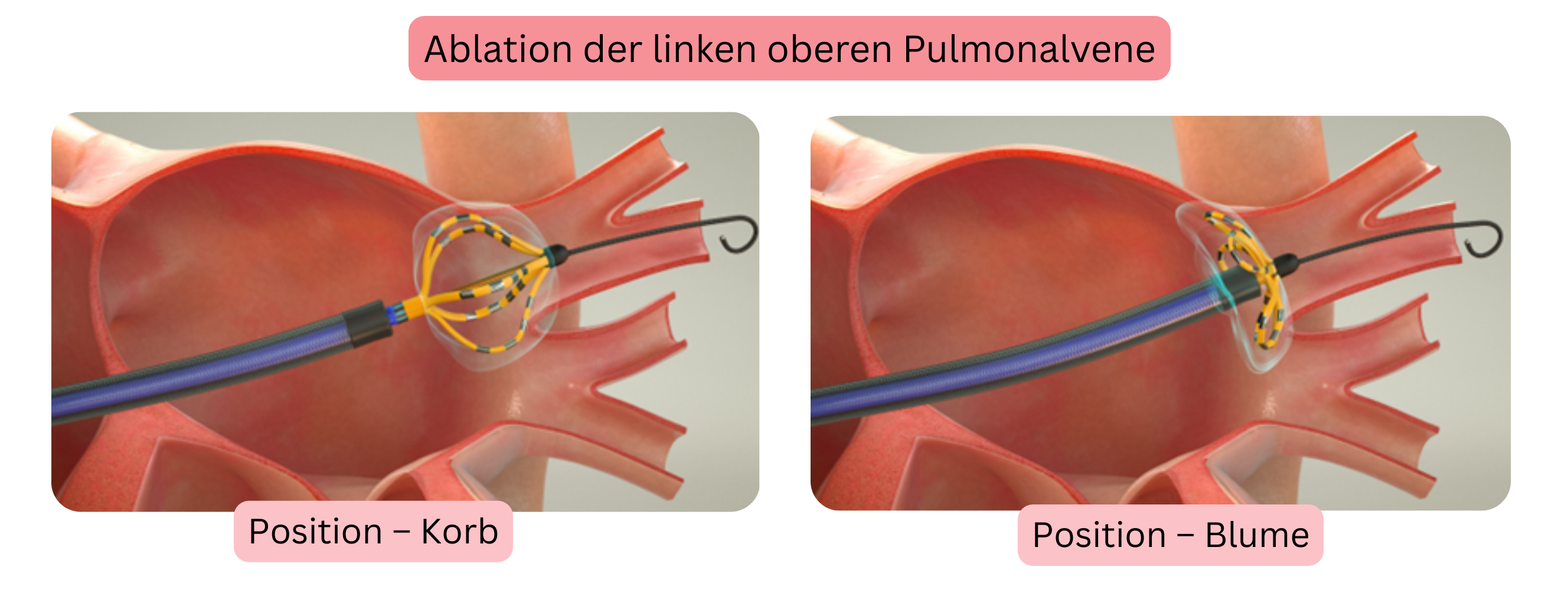
Farawave ist ein spezieller Katheter mit zwei Konfigurationen: Basket und Flower.
3–5 min vor der ersten Applikation werden 1 mg Atropin intravenös verabreicht (kann bis zu einer maximalen Dosis von 3 mg wiederholt werden).
| Atropin – Prävention der Bradykardie vor Ablation | |
|---|---|
| Zweck | Prävention der Bradykardie |
| Wirkmechanismus | Blockiert den vagalen Effekt (antimuskarinischer Effekt) |
| Dosis | 1 mg intravenös (max. 3 mg) |
| Wirkeintritt | 1–2 min |
| Erwarteter Effekt | Anstieg der Herzfrequenz um 20–40/min |
| Wirkdauer | 30–60 min |
| Kontraindikation | Glaukom |
Elektrische Impulse sind schmerzhaft; daher werden sie unter Allgemeinanästhesie oder Sedierung appliziert.
Persistiert VHF nach Pulmonalvenenisolation, wird eine ausgedehntere linksatriale Ablation durchgeführt:
Linkes Vorhofohr und Ablation.
Hat ein Patient VHF und Vorhofflattern (VHFla),
Während des Pulsens bei VHF- und VHFla-Ablation kann ein Koronarspasmus auftreten, wenn die Ablation in Nähe einer Koronararterie erfolgt.
| Prävention des Koronarspasmus vor Ablation – Isoket vs. Nitroglycerin | ||
|---|---|---|
| Medikament | Isoket (Isosorbiddinitrat) | Nitroglycerin |
| Zweck | Langsamere, länger anhaltende Prävention des Koronarspasmus | Schnelle Prävention und Therapie des Koronarspasmus |
| Wirkmechanismus | NO-Donor → koronare Vasodilatation | NO-Donor → koronare Vasodilatation |
| Applikation | intravenöser Bolus 1–2 mg | intravenöser Bolus 50–200 µg |
| Wirkeintritt | 3–5 min | 1–2 min |
| Wirkdauer | 30–60 min | 5–10 min |
| Risiko einer Hypotonie | Höher (längere Dauer) | Niedriger (kurze Dauer) |
EKG-Veränderungen während Ablation im Bereich des Mitral- und Trikuspidalisthmus:
Elektrische Impulse bei der Pulsed-Field-Ablation sind kardioselektiv:
| Elektrische Impulse bei der Pulsed-Field-Ablation |
|---|
| Verursachen keine Pulmonalvenenstenose |
| Verursachen keine atrioösophageale Fistel |
| Verursachen keine Phrenikusparese |
Nach der VHF-Ablation kann der Prozedurerfolg auf drei Arten überprüft werden:
| Verifikation des Erfolgs der Vorhofflimmernablation | |||
|---|---|---|---|
| Methode | Ort des Pacings | Was beurteilt wird | Erfolg |
| Pacing aus den Pulmonalvenen | Sequenziell aus jeder Pulmonalvene (mit dem Farawave-Katheter) | Ob Impulse aus der Vene in den linken Vorhof propagieren | Keine atriale Antwort = Vene isoliert |
| Burst-Pacing | Aus dem Koronarsinus (KS-Katheter) | Induktion von VHF nach Bursts (8–10 Stimuli) | VHF wird nicht induziert oder VHF dauert nicht > 1 min = Erfolg |
| Ramp-Pacing | Aus dem Koronarsinus (KS-Katheter) | Ob VHF während Pacings mit progressiver Zyklusverkürzung induziert wird | VHF wird nicht induziert oder VHF dauert nicht > 1 min = Erfolg |
Während der Pulsed-Field-Ablation kommt es zur Elektroporation von Kardiomyozyten, d. h. zur Perforation der Zellmembran durch ein elektrisches Feld. Darauf folgt Apoptose. Kardiospezifische Enzyme werden aus geschädigten Kardiomyozyten freigesetzt und steigen innerhalb von 24 h auf hohe Werte an.
| Kardiospezifische Enzyme innerhalb von 24 h nach Pulsed-Field-Ablation | |
|---|---|
| Enzym | Wert |
| Troponin | 1500 ng/l (±500) |
| CK | 300 ng/l (±100) |
| CK-MB | 35 mg/l (±10) |
Während der Pulsed-Field-Ablation kommt es zur Hämolyse, die sich nach der Prozedur als makroskopische Hämaturie manifestiert.
Der Ablationserfolg wird anhand des Auftretens eines VHF-Rezidivs innerhalb von 1 Jahr nach Ablation beurteilt.
| Erfolg der Vorhofflimmernablation (innerhalb von 12 Monaten) | |
|---|---|
| VHF-Klassifikation | Erfolg |
| Paroxysmales VHF | 66–82 % |
| Persistierendes VHF | 56–72 % |
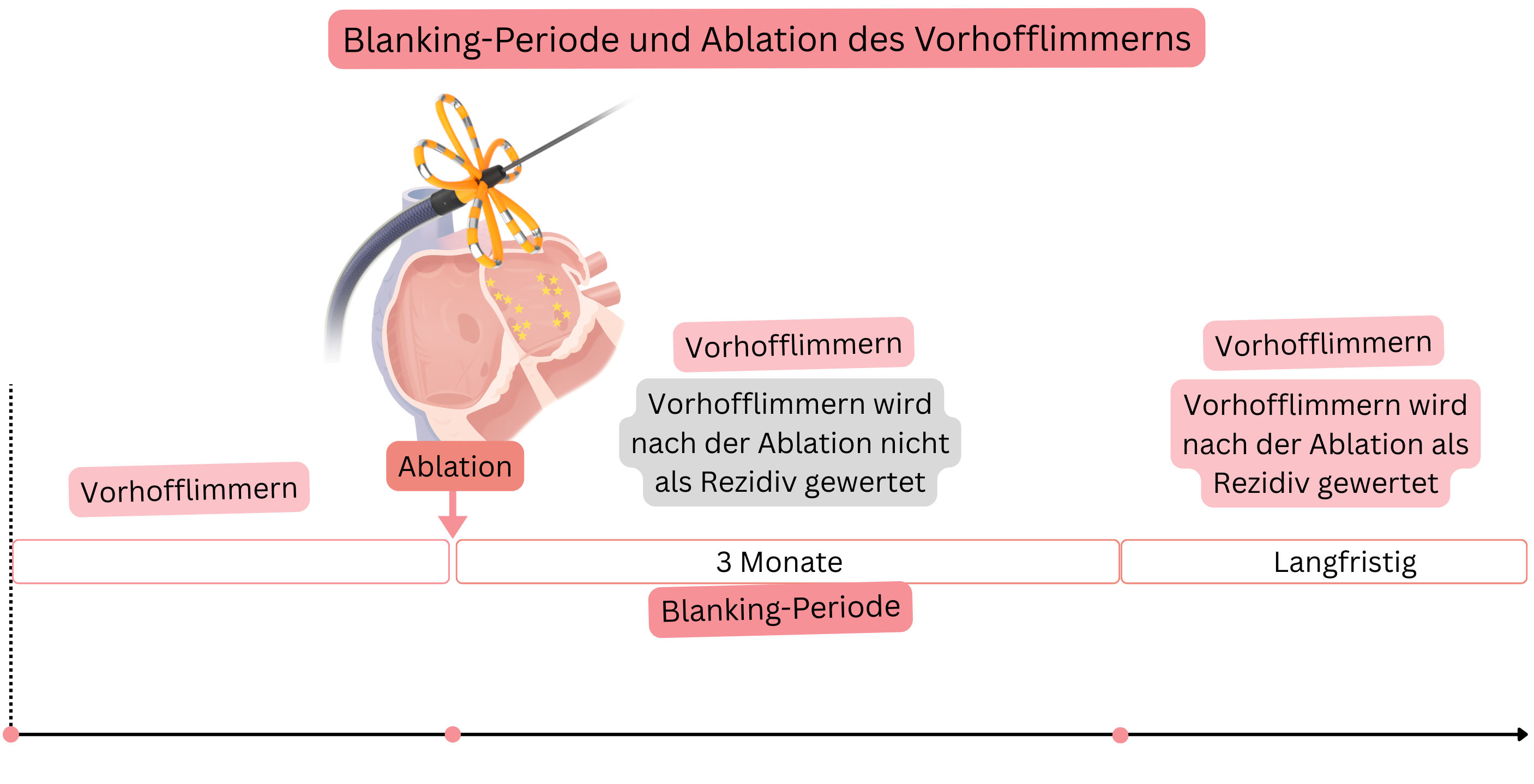
Blanking-Periode
| Therapie während der Blanking-Periode (3 Monate nach Ablation) | ||
|---|---|---|
| Therapie | Dauer | Hinweis |
| Antiarrhythmika | 3 Monate | Verabreicht unabhängig davon, ob Sinusrhythmus oder VHF vorliegt. |
| Antikoagulationstherapie | 2 Monate | Verabreicht unabhängig vom CHA2DS2-VA-Score |
Bei VHF-Rezidiv nach Ablation – Pulmonalvenenisolation (mit Pulsed-Field-Energie) kann es zu einer Re-Konnektierung einer Pulmonalvene an den linken Vorhof kommen. Re-Konnektierung tritt am häufigsten auf in:
Während und nach Pulsed-Field-VHF-Ablation können Komplikationen auftreten, sie sind jedoch sehr selten. Die Inzidenz von Komplikationen beträgt:
Schwere und leichte Komplikationen sind in der folgenden Tabelle aufgeführt:
| Schwere Komplikationen der Pulsed-Field-Ablation | |
|---|---|
| Gesamt | 0,98 % |
| Perikardtamponade | 0,36 % |
| Vaskuläre Komplikation (interventionspflichtig) | 0,30 % |
| Koronarspasmus | 0,14 % |
| Schlaganfall | 0,12 % |
| Hämolyse mit akutem Nierenversagen | 0,03 % |
| Tod | 0,03 % |
| Andere (Thrombose, koronare Luftembolie) | 0,006 % |
| Ösophagusfistel | 0 % |
| Pulmonalvenenstenose | 0 % |
| Phrenikusparese (permanent) | 0 % |
| Leichte Komplikationen der Pulsed-Field-Ablation | |
|---|---|
| Gesamt | 3,21 % |
| Vaskuläre Komplikationen (nicht interventionspflichtig) | 2,20 % |
| Perikarderguss (nicht interventionspflichtig) | 0,33 % |
| Andere leichte Komplikationen (Hämatome, Arrhythmien) | 0,32 % |
| Perikarditis | 0,17 % |
| Transitorisch ischämische Attacke | 0,12 % |
| Phrenikusparese (temporär) | 0,06 % |
Bei 5–15% der Patienten tritt während der Pulsed-Field-Ablation eine asymptomatische „silent“ zerebrale Ischämie auf.
| Ablation des Vorhofflimmerns | Klasse |
|---|---|
| Pulsed-Field-Ablation (nicht Radiofrequenz- oder Kryoablation) wird als bevorzugte Methode der Ablation des Vorhofflimmerns empfohlen. | I |
Pulsed-Field-Ablation wird bei Patienten mit paroxysmalem oder persistierendem Vorhofflimmern empfohlen, wenn Vorhofflimmern symptomatisch ist:
|
I |
| Pulsed-Field-Ablation wird bei Patienten mit tachykardieinduzierter Kardiomyopathie infolge von Vorhofflimmern empfohlen. | I |
| Pulsed-Field-Ablation sollte bei Patienten mit Vorhofflimmern erwogen werden, die symptomatische präautomatische Pausen haben. | IIa |
Bei Vorhofflimmernrezidiv kann die Pulsed-Field-Ablation wiederholt werden (nicht früher als 3 Monate), wenn Vorhofflimmern symptomatisch ist:
|
IIa |
| Vor Vorhofflimmernablation sollte eine CT- oder MR-Angiographie des linken Vorhofs und der Pulmonalvenen zur Beurteilung der Pulmonalvenenanatomie erwogen werden. | IIa |
Die „pace and ablate“-Strategie kann bei Patienten mit symptomatischem Vorhofflimmern erwogen werden, bei denen Folgendes versagt hat:
|
IIa |
| Antikoagulationstherapie und Ablation des Vorhofflimmerns | Klasse |
|---|---|
| Eine Antikoagulationstherapie wird für mindestens 4 Wochen vor der Vorhofflimmernablation empfohlen, unabhängig vom CHA₂DS₂-VA-Score. | I |
| Eine NOAK-Antikoagulationstherapie wird empfohlen, am Morgen des Tages der Vorhofflimmernablation nicht einzunehmen. | I |
| Eine NOAK-Antikoagulationstherapie wird empfohlen, 6 h nach Vorhofflimmernablation zu beginnen, wenn keine Blutungszeichen vorliegen. | I |
| Unter Warfarintherapie wird empfohlen, die Vorhofflimmernablation am Tag der Prozedur bei therapeutischem INR von ungefähr 2,0 durchzuführen. | I |
| Eine Antikoagulationstherapie wird für die ersten 2 Monate nach Vorhofflimmernablation empfohlen, unabhängig vom Ablationserfolg und unabhängig vom CHA₂DS₂-VA-Score. | I |
| Zwei Monate nach Vorhofflimmernablation ist eine langfristige Antikoagulation gemäß dem CHA₂DS₂-VA-Score indiziert, unabhängig vom Ablationserfolg. | I |
| Eine antiarrhythmische Therapie (Propafenon, Flecainid, Sotalol, Betablocker) wird für die ersten 3 Monate nach Vorhofflimmernablation empfohlen, unabhängig vom Ablationserfolg. | I |
| Drei Monate nach Vorhofflimmernablation ist eine antiarrhythmische Therapie gemäß Vorhofflimmernrezidiv indiziert. | I |
| Eine Vorhofflimmernablation kann erwogen werden, wenn der Patient eine duale antithrombotische Therapie erhält (z. B. NOAK + Clopidogrel). | IIa |
| Vorhofflimmernablation während der Herzchirurgie | Klasse |
|---|---|
| Bei einem Patienten, der sich einer herzchirurgischen Mitralklappenoperation unterzieht, wird eine concomitante chirurgische Vorhofflimmernablation mittels Cox-Maze-IV-Prozedur empfohlen. | I |
| Bei einem Patienten, der sich einer herzchirurgischen Operation außerhalb der Mitralklappenchirurgie unterzieht, sollte eine concomitante chirurgische Vorhofflimmernablation mittels Cox-Maze-IV-Prozedur erwogen werden. | IIa |
| Während einer Herzoperation wird empfohlen, das Vorliegen eines Thrombus im linken Vorhof vor chirurgischer Vorhofflimmernablation auszuschließen. | I |
Diese Leitlinien sind inoffiziell und stellen keine offiziellen Leitlinien dar, die von einer kardiologischen Fachgesellschaft herausgegeben wurden. Sie dienen ausschließlich zu Bildungs- und Informationszwecken.
