

心房細動アブレーション前には、血栓塞栓症予防として4週間の抗凝固療法が推奨される。
血栓塞栓症予防として、アブレーション後2か月間の抗凝固療法が推奨される。
心房細動アブレーション前(<24 h)の経食道心エコー(TEE)は、4週間の抗凝固療法を実施していても以下の場合に推奨される:
| アブレーション前TEE―抗凝固療法(4週間)施行下でも行う適応 |
|---|
| 一過性脳虚血発作(TIA)の既往 |
| 脳卒中の既往 |
| 抗凝固療法の不規則な内服 |
| INR < 2(ワルファリン療法中) |
| 心腔内血栓の既往(特に左心耳) |
| 左心耳排出速度 < 20 cm/sの既往 |
心房細動アブレーション前には、患者の状態が許せば抗不整脈療法を中止することが適切である。
アブレーション前には、患者の状態が許せばリズムコントロール目的の抗不整脈薬は中止することが適切であるが、レートコントロール目的薬は中止しない。
| 心房細動アブレーション前の抗不整脈薬中止 | ||
|---|---|---|
| 薬剤 | クラス | アブレーション前の中止期間 |
| ジソピラミド | IA | 3~5日 |
| プロパフェノン | IC | 3~5日 |
| フレカイニド | IC | 3~5日 |
| ソタロール | III | 3~5日 |
| アミオダロン | III | 4~6週間 |
| ドロネダロン | III | 3~5日 |
心房細動アブレーション(手技)では、鼠径部(大腿静脈)から3本の血管アクセス用シースを要する:
大腿シース挿入後、未分画ヘパリン(UFH)5000 IUを投与する。
| UFH用量とACT延長 | ||
|---|---|---|
| UFH用量 | 体重70 kgにおけるACT(正常からの延長) | 体重100 kgにおけるACT(正常からの延長) |
| UFHなし | 80~120秒 | 80~120秒 |
| 1000 IU | 120~140秒(↑20~40) | 110~130秒(↑10~30) |
| 3000 IU | 150~180秒(↑50~80) | 130~160秒(↑30~60) |
| 5000 IU | 200~240秒(↑100~140) | 170~210秒(↑70~110) |
| 7000 IU | 230~280秒(↑130~180) | 200~250秒(↑100~150) |
| 10000 IU | 280~340秒(↑180~240) | 230~300秒(↑130~200) |
静脈シース周囲および右心房内カテーテル上の血栓は、肺へ塞栓するため危険性は相対的に低い。
| シースまたはカテーテル上の血栓形成リスク | |
|---|---|
| ACT | 推定リスク |
| 80~120秒(UFHなし) | 10~20%(10~20分以内) |
| 250~300秒 | 1~2% |
| 300~350秒 | < 1% |
大腿静脈より専用針を右心房へ導入後、経中隔穿刺を行う。
手技中のACTおよびUFH
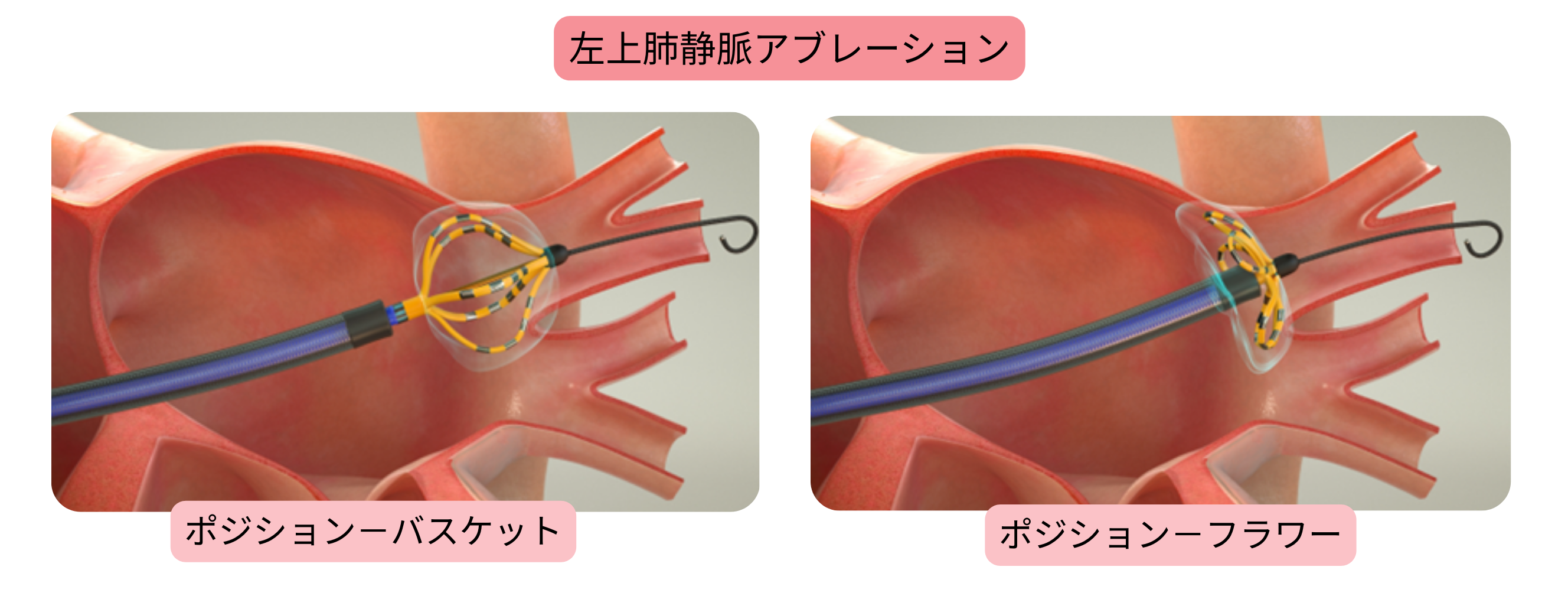
Farawaveは、バスケットとフラワーの2つの形状を有する専用カテーテルである。
初回アプリケーションの3~5分前に、硫酸アトロピン1 mgを静脈内投与する(最大3 mgまで反復可)。
| アトロピン―アブレーション前の徐脈予防 | |
|---|---|
| 目的 | 徐脈の予防 |
| 作用機序 | 迷走神経作用の遮断(抗ムスカリン作用) |
| 用量 | 1 mg 静脈内投与(最大3 mg) |
| 作用発現 | 1~2分 |
| 期待される効果 | 心拍数が20~40/分増加 |
| 作用持続 | 30~60分 |
| 禁忌 | 緑内障 |
電気パルスは疼痛を伴うため、全身麻酔または鎮静下に送達する。
肺静脈隔離後も心房細動が持続する場合は、左心房の追加アブレーションを施行する:
左心耳とアブレーション。
心房細動と心房粗動(AFL)を併存する患者では、
心房細動および心房粗動アブレーション中のパルス送達では、冠動脈近傍でアブレーションを行うと冠攣縮を来し得る。
| アブレーション前の冠攣縮予防―Isoketとニトログリセリンの比較 | ||
|---|---|---|
| 薬剤 | Isoket(硝酸イソソルビド) | ニトログリセリン |
| 目的 | 冠攣縮の予防(発現は緩徐で持続が長い) | 冠攣縮の迅速な予防および治療 |
| 作用機序 | NO供与体→冠動脈拡張 | NO供与体→冠動脈拡張 |
| 投与 | 静脈内ボーラス 1~2 mg | 静脈内ボーラス 50~200 µg |
| 作用発現 | 3~5分 | 1~2分 |
| 作用持続 | 30~60分 | 5~10分 |
| 低血圧リスク | 高い(持続が長い) | 低い(持続が短い) |
僧帽弁峡部および三尖弁峡部領域のアブレーション時の心電図変化:
パルスフィールドアブレーションの電気パルスは心筋選択性を有する:
| パルスフィールドアブレーションの電気パルス |
|---|
| 肺静脈狭窄を来さない |
| 心房食道瘻を来さない |
| 横隔神経障害を来さない |
心房細動アブレーション後の手技成功は、以下の3つの方法で確認できる:
| 心房細動アブレーション成功の確認 | |||
|---|---|---|---|
| 方法 | ペーシング部位 | 評価項目 | 成功 |
| 肺静脈からのペーシング | 各肺静脈より順次(Farawaveカテーテル) | 肺静脈からの刺激が左心房へ伝播するか | 心房反応なし=肺静脈隔離 |
| バーストペーシング | 冠静脈洞(CSカテーテル) | バースト(8~10刺激)後の心房細動誘発 | 心房細動が誘発されない、または心房細動が> 1分持続しない=成功 |
| ランプペーシング | 冠静脈洞(CSカテーテル) | 周期長を段階的に短縮するペーシング中に心房細動が誘発されるか | 心房細動が誘発されない、または心房細動が> 1分持続しない=成功 |
パルスフィールドアブレーション中には、電場により心筋細胞膜に穿孔(エレクトロポレーション)が生じ、その後アポトーシスに至る。 障害心筋細胞から心筋特異的酵素が放出され、24時間以内に高値となる。
| パルスフィールドアブレーション後24時間以内の心筋特異的酵素 | |
|---|---|
| 酵素 | 値 |
| トロポニン | 1500 ng/l(±500) |
| CK | 300 ng/l(±100) |
| CK-MB | 35 mg/l(±10) |
パルスフィールドアブレーション中には溶血が生じ、手技後に肉眼的血尿として認められる。
アブレーション成功は、アブレーション後1年以内の心房細動再発の有無で評価する。
| 心房細動アブレーション成功率(12か月以内) | |
|---|---|
| 心房細動分類 | 成功 |
| 発作性心房細動 | 66~82 % |
| 持続性心房細動 | 56~72 % |
ブランキング期間
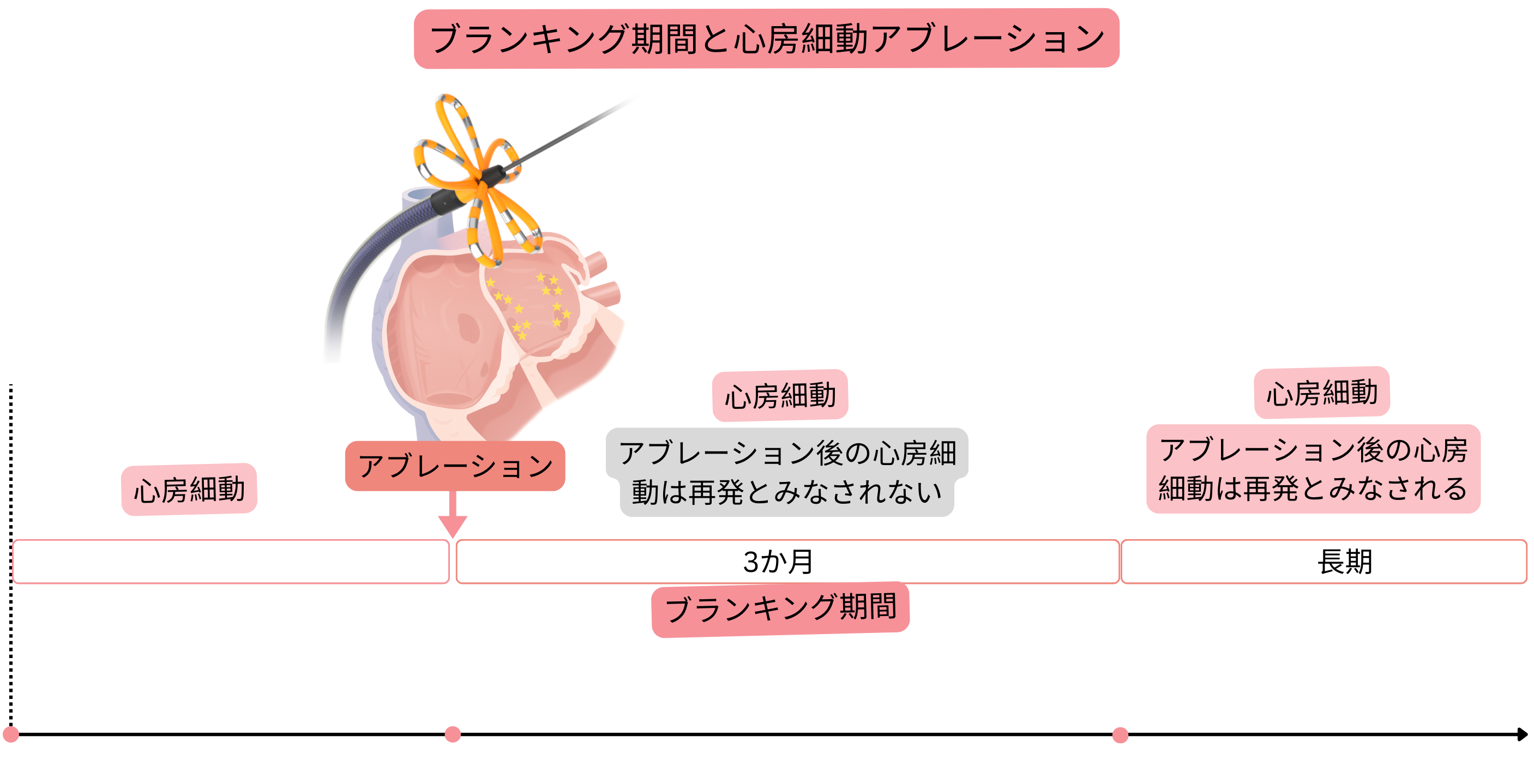
| ブランキング期間(アブレーション後3か月間)の治療 | ||
|---|---|---|
| 治療 | 期間 | 備考 |
| 抗不整脈薬 | 3か月 | 洞調律か心房細動かにかかわらず投与する。 |
| 抗凝固療法 | 2か月 | CHA2DS2-VAスコアにかかわらず投与する |
アブレーション後の心房細動再発では、肺静脈隔離(パルスフィールドエネルギー)後に肺静脈と左心房の再伝導が生じ得る。再伝導は以下で最も多い:
パルスフィールド心房細動アブレーションの手技中および手技後に合併症を来し得るが、極めて稀である。合併症発生率は:
主要合併症および軽微合併症を以下の表に示す:
| パルスフィールドアブレーションの主要合併症 | |
|---|---|
| 総計 | 0.98 % |
| 心タンポナーデ | 0.36 % |
| 血管合併症(介入を要する) | 0.30 % |
| 冠攣縮 | 0.14 % |
| 脳卒中 | 0.12 % |
| 溶血に伴う急性腎不全 | 0.03 % |
| 死亡 | 0.03 % |
| その他(血栓症、冠動脈空気塞栓) | 0.006 % |
| 食道瘻 | 0 % |
| 肺静脈狭窄 | 0 % |
| 横隔神経障害(永続) | 0 % |
| パルスフィールドアブレーションの軽微合併症 | |
|---|---|
| 総計 | 3.21 % |
| 血管合併症(介入を要しない) | 2.20 % |
| 心嚢液貯留(介入を要しない) | 0.33 % |
| その他の軽微合併症(血腫、不整脈) | 0.32 % |
| 心膜炎 | 0.17 % |
| 一過性脳虚血発作 | 0.12 % |
| 横隔神経障害(一過性) | 0.06 % |
パルスフィールドアブレーション中に、無症候性のサイレント脳虚血が5~15%の患者で生じる。
| 心房細動アブレーション | クラス |
|---|---|
| パルスフィールドアブレーション(高周波アブレーションまたはクライオアブレーションではなく)を、心房細動アブレーションの第一選択法として推奨する。 | I |
症候性の発作性または持続性心房細動患者において、以下の場合にパルスフィールドアブレーションを推奨する:
|
I |
| 心房細動による頻脈誘発性心筋症患者において、パルスフィールドアブレーションを推奨する。 | I |
| 症候性の自動能抑制性休止を有する心房細動患者では、パルスフィールドアブレーションを考慮する。 | IIa |
心房細動再発時、症候性で以下の場合には、パルスフィールドアブレーションの再施行を考慮してよい(3か月以内は行わない):
|
IIa |
| 心房細動アブレーション前に、肺静脈解剖評価のため左心房および肺静脈のCTまたはMR血管造影を考慮する。 | IIa |
症候性心房細動患者において、以下が無効であった場合、「ペース・アンド・アブレート」戦略を考慮してよい:
|
IIa |
| 抗凝固療法と心房細動アブレーション | クラス |
|---|---|
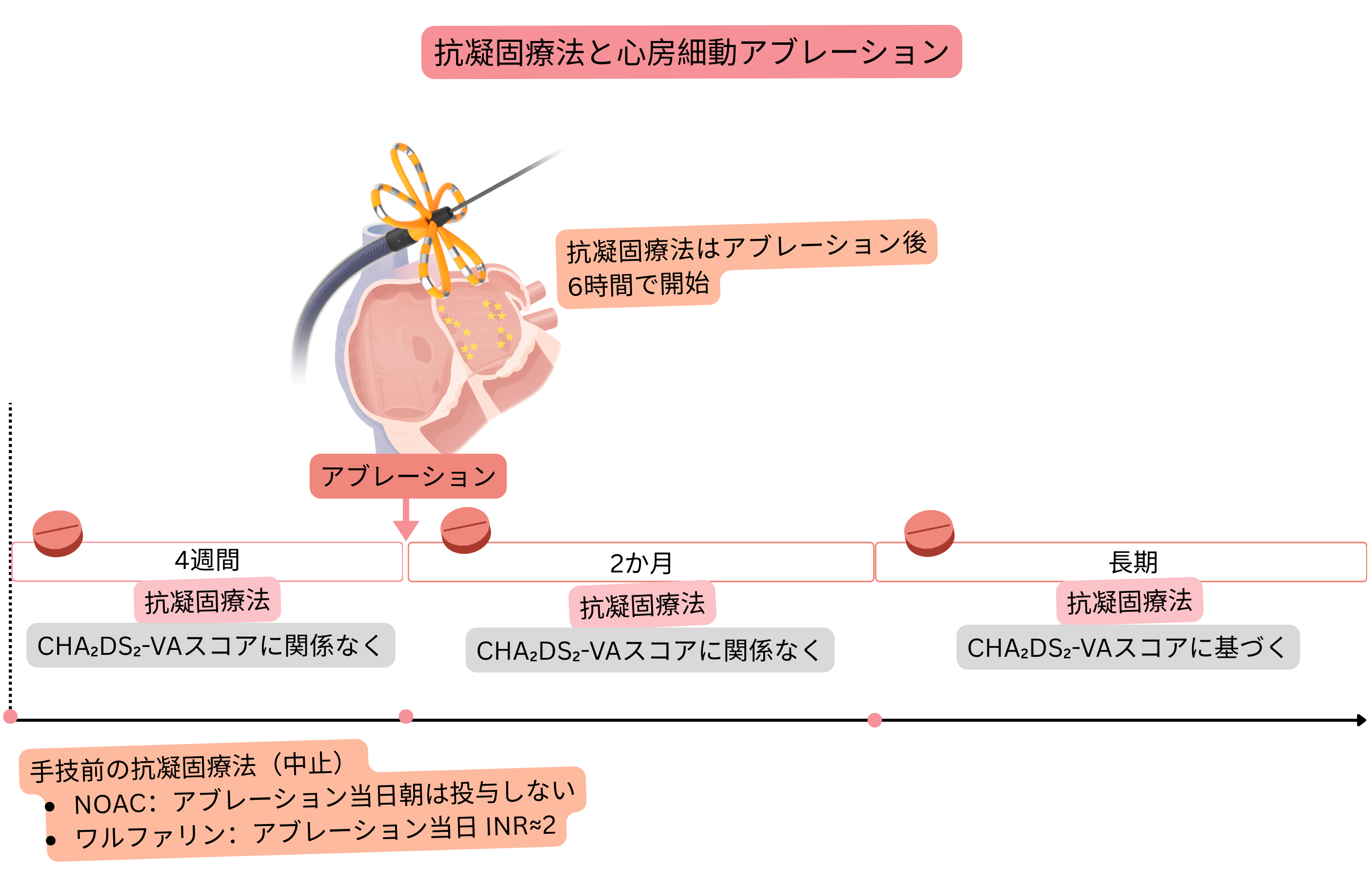
| 心房細動アブレーション前には、CHA₂DS₂-VAスコアにかかわらず、少なくとも4週間の抗凝固療法が推奨される。 | I |
| 心房細動アブレーション当日の朝は、NOACによる抗凝固療法を内服しないことを推奨する。 | I |
| 心房細動アブレーション後、出血所見がなければ6時間後にNOACによる抗凝固療法を開始することを推奨する。 | I |
| ワルファリン療法中は、手技当日のINRが約2.0の治療域で心房細動アブレーションを施行することを推奨する。 | I |
| 心房細動アブレーション後最初の2か月間は、アブレーション成功の有無およびCHA₂DS₂-VAスコアにかかわらず、抗凝固療法を推奨する。 | I |
| 心房細動アブレーション2か月後以降は、アブレーション成功の有無にかかわらず、CHA₂DS₂-VAスコアに基づき長期抗凝固療法を行う。 | I |
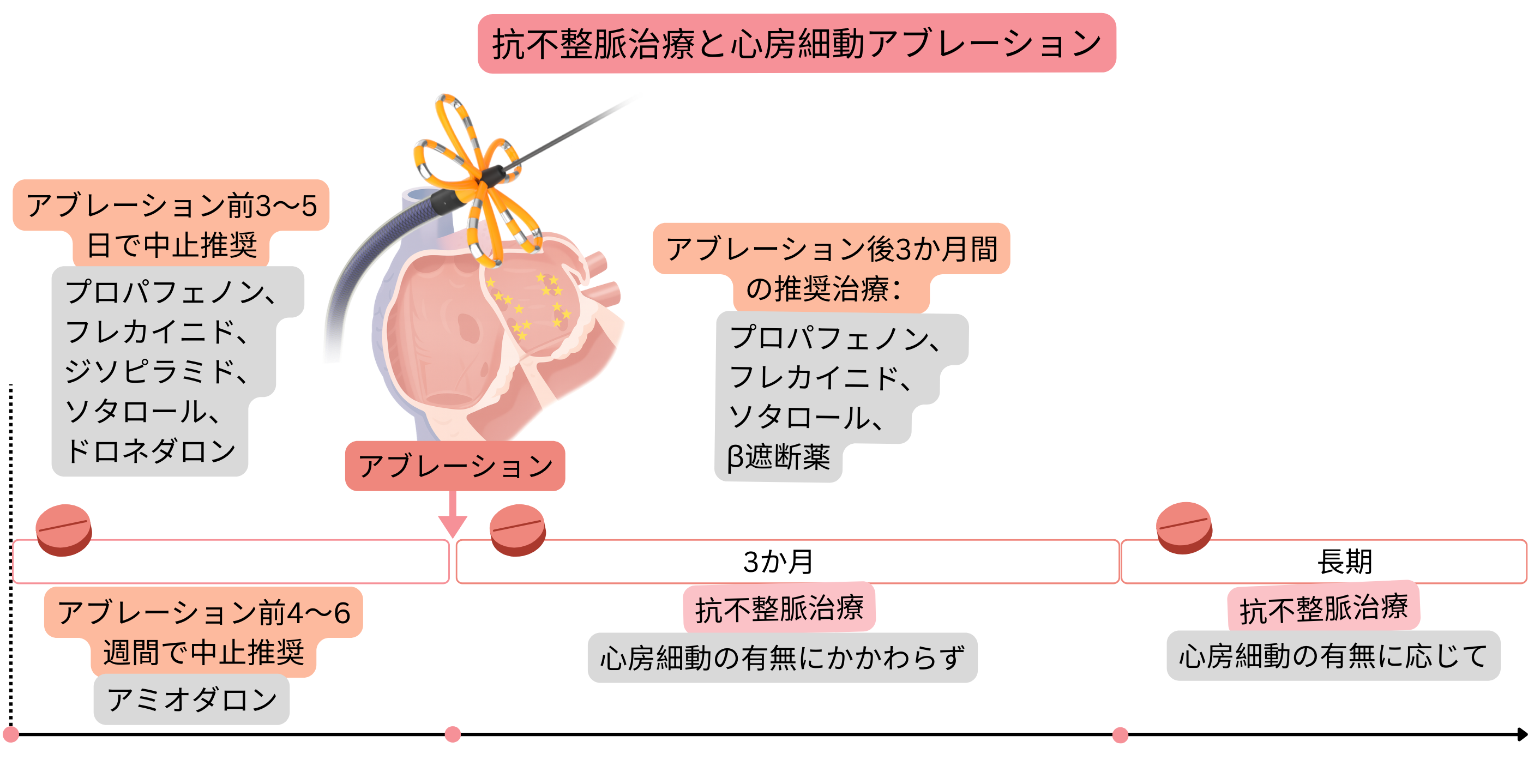
| 心房細動アブレーション後最初の3か月間は、アブレーション成功の有無にかかわらず、抗不整脈療法(プロパフェノン、フレカイニド、ソタロール、β遮断薬)を推奨する。 | I |
| 心房細動アブレーション3か月後以降は、心房細動再発に応じて抗不整脈療法を行う。 | I |
| 二重抗血栓療法(例:NOAC+クロピドグレル)施行中の患者では、心房細動アブレーションを考慮してよい。 | IIa |
| 心臓手術時の心房細動アブレーション | クラス |
|---|---|
| 僧帽弁手術を受ける患者では、Cox-Maze IV手技による同時外科的心房細動アブレーションを推奨する。 | I |
| 僧帽弁手術以外の心臓手術を受ける患者では、Cox-Maze IV手技による同時外科的心房細動アブレーションを考慮する。 | IIa |
| 心臓手術中は、外科的心房細動アブレーション前に左心房内血栓の有無を除外することを推奨する。 | I |
これらのガイドラインは非公式であり、いかなる専門的な心臓病学会が発行した正式なガイドラインを代表するものではありません。教育および情報提供のみを目的としています。
