

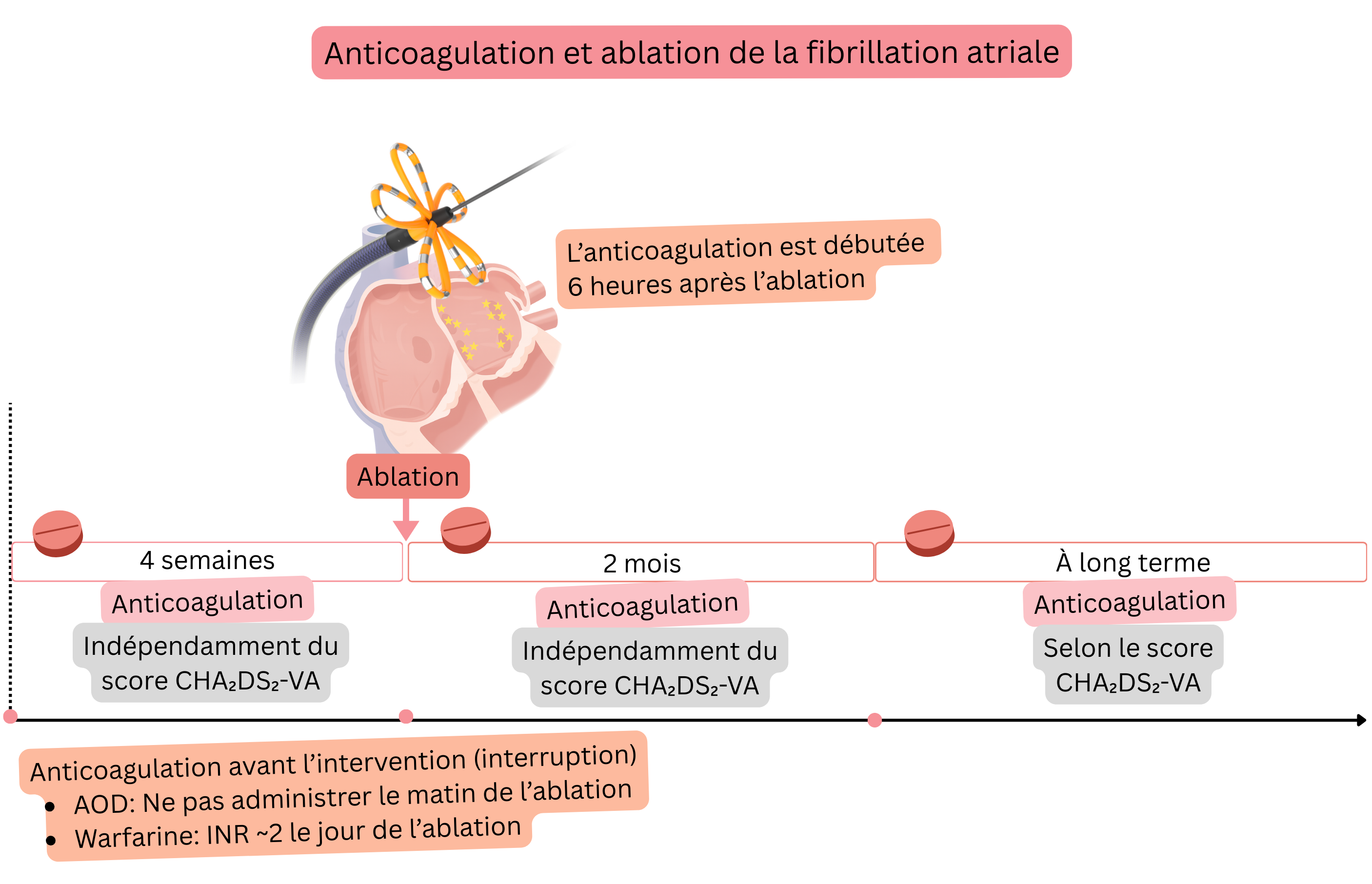
Avant une ablation de la fibrillation atriale (FA), 4 semaines de traitement anticoagulant sont recommandées pour la prévention du thromboembolisme.
Pour la prévention du thromboembolisme, 2 mois de traitement anticoagulant sont recommandés après l’ablation,
Une échocardiographie transœsophagienne avant ablation de la FA (<24 h) est recommandée malgré 4 semaines de traitement anticoagulant dans les cas suivants :
| ETO avant ablation – indications malgré anticoagulation (4 semaines) |
|---|
| Antécédent d’accident ischémique transitoire (AIT) |
| Antécédent d’AVC |
| Prise irrégulière du traitement anticoagulant |
| INR < 2 (sous traitement par warfarine) |
| Antécédent de thrombus intracardiaque (en particulier dans l’appendice auriculaire gauche) |
| Antécédent de vélocité de vidange de l’appendice auriculaire gauche < 20 cm/s |
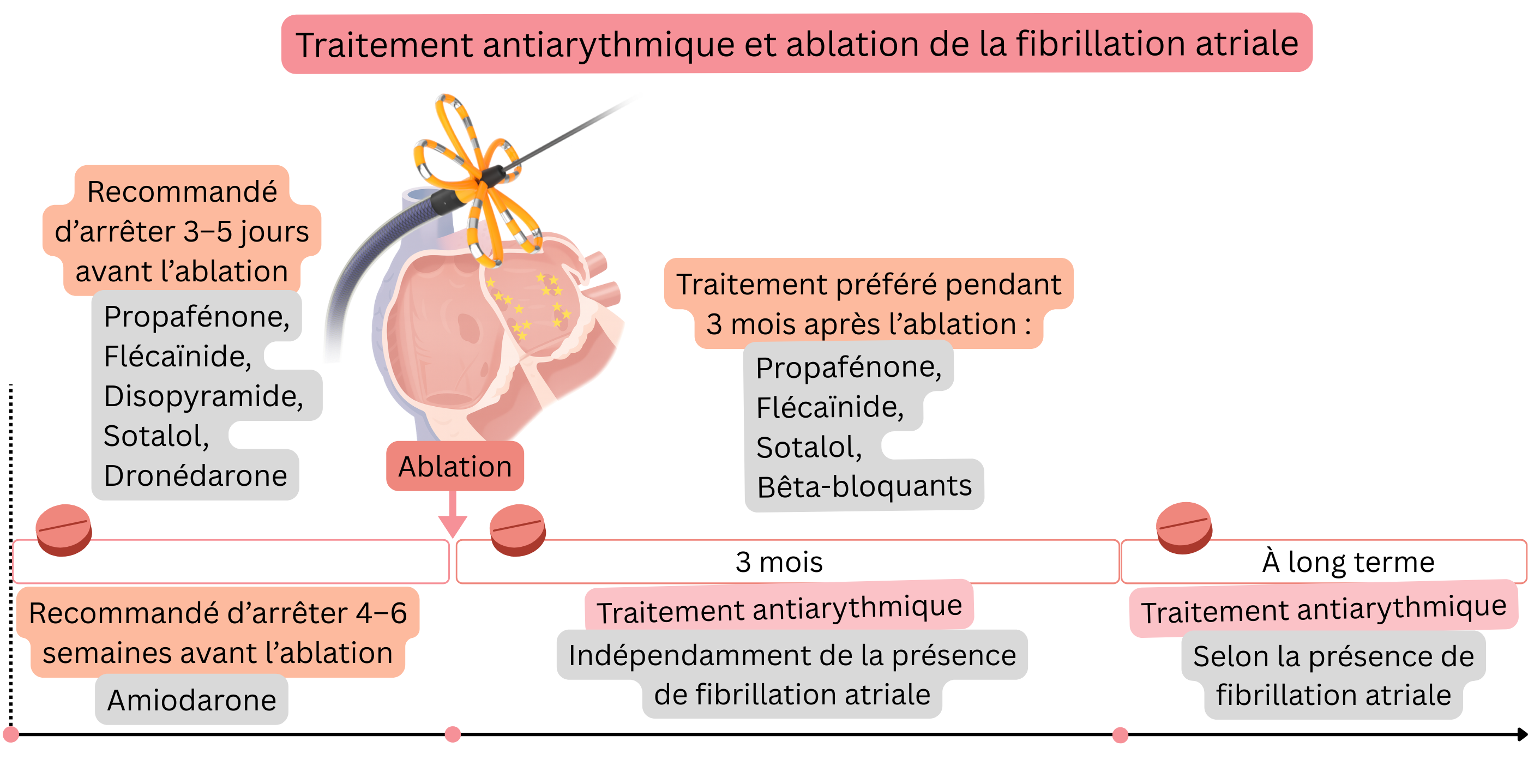
Avant l’ablation de la FA, il est approprié d’interrompre le traitement antiarythmique (si l’état du patient le permet).
Avant l’ablation, il est approprié d’interrompre les antiarythmiques utilisés pour le contrôle du rythme (si l’état du patient le permet), mais pas ceux utilisés pour le contrôle de la fréquence.
| Interruption des antiarythmiques avant ablation de la fibrillation atriale | ||
|---|---|---|
| Médicament | Classe | Arrêt avant l’ablation |
| Disopyramide | IA | 3–5 jours |
| Propafénone | IC | 3–5 jours |
| Flécaïnide | IC | 3–5 jours |
| Sotalol | III | 3–5 jours |
| Amiodarone | III | 4–6 semaines |
| Dronédarone | III | 3–5 jours |
La procédure d’ablation de la FA nécessite 3 introducteurs d’accès vasculaire au niveau des aines (veines fémorales) :
Après mise en place des introducteurs fémoraux, 5000 UI d’héparine non fractionnée (HNF) sont administrées.
| Dose d’HNF et allongement de l’ACT | ||
|---|---|---|
| Dose d’HNF | ACT à 70 kg (allongement par rapport à la normale) | ACT à 100 kg (allongement par rapport à la normale) |
| Sans HNF | 80 – 120 s | 80 – 120 s |
| 1000 UI | 120 – 140 s (↑20–40) | 110 – 130 s (↑10–30) |
| 3000 UI | 150 – 180 s (↑50–80) | 130 – 160 s (↑30–60) |
| 5000 UI | 200 – 240 s (↑100–140) | 170 – 210 s (↑70–110) |
| 7000 UI | 230 – 280 s (↑130–180) | 200 – 250 s (↑100–150) |
| 10000 UI | 280 – 340 s (↑180–240) | 230 – 300 s (↑130–200) |
Un thrombus au niveau des gaines veineuses et dans l’oreillette droite sur le cathéter est moins dangereux, car il embolise vers les poumons.
| Risque de formation de thrombus sur une gaine ou un cathéter | |
|---|---|
| ACT | Risque estimé |
| 80 – 120 s (sans HNF) | 10–20 % (en 10–20 min) |
| 250–300 s | 1–2 % |
| 300–350 s | < 1 % |
Après introduction d’une aiguille dédiée par la veine fémorale dans l’oreillette droite, une ponction transseptale est réalisée.
ACT et HNF pendant la procédure
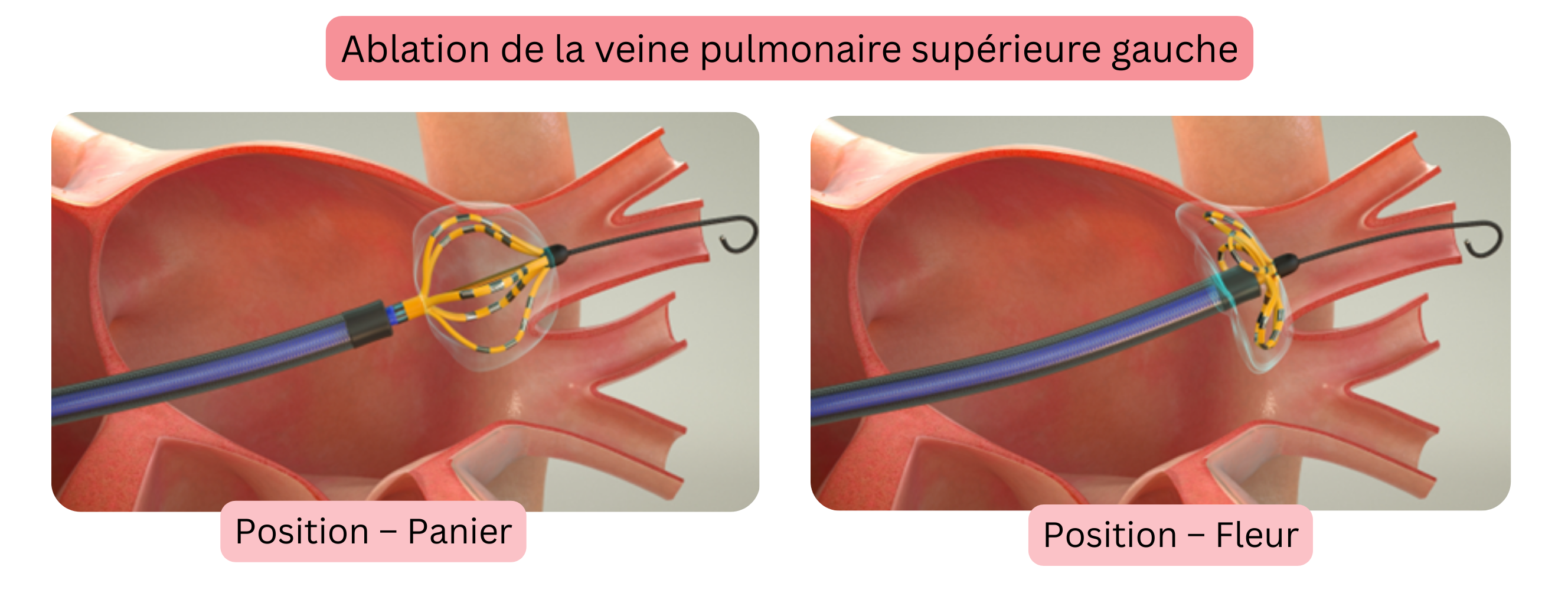
Farawave est un cathéter dédié avec deux configurations : panier et fleur.
3–5 min avant la première application, 1 mg d’atropine est administré par voie intraveineuse (peut être répété jusqu’à une dose maximale de 3 mg).
| Atropine – prévention de la bradycardie avant ablation | |
|---|---|
| Objectif | Prévention de la bradycardie |
| Mécanisme | Blocage de l’effet vagal (effet antimuscarinique) |
| Dose | 1 mg intraveineux (max. 3 mg) |
| Début d’action | 1–2 min |
| Effet attendu | Augmentation de la fréquence cardiaque de 20–40/min |
| Durée d’action | 30–60 min |
| Contre-indication | Glaucome |
Les impulsions électriques sont douloureuses ; elles sont donc délivrées sous anesthésie générale ou sédation.
Si la FA persiste après l’isolation des veines pulmonaires, une ablation plus étendue de l’oreillette gauche est réalisée :
Appendice auriculaire gauche et ablation.
Si un patient présente une FA et un flutter atrial (FLA),
Lors des impulsions pendant l’ablation de FA et de FLA, un spasme coronaire peut survenir si l’ablation est réalisée à proximité d’une artère coronaire.
| Prévention du spasme coronaire avant ablation – Isoket vs nitroglycérine | ||
|---|---|---|
| Médicament | Isoket (dinitrate d’isosorbide) | Nitroglycérine |
| Objectif | Prévention du spasme coronaire plus lente, plus prolongée | Prévention et traitement rapides du spasme coronaire |
| Mécanisme d’action | Donneur de NO → vasodilatation coronaire | Donneur de NO → vasodilatation coronaire |
| Administration | bolus intraveineux 1–2 mg | bolus intraveineux 50–200 µg |
| Début d’action | 3–5 min | 1–2 min |
| Durée d’action | 30–60 min | 5–10 min |
| Risque d’hypotension | Plus élevé (durée plus longue) | Plus faible (durée plus courte) |
Modifications ECG pendant l’ablation dans la région des isthmes mitral et tricuspide :
Les impulsions électriques lors de l’ablation par champ pulsé sont cardiosélectives :
| Impulsions électriques lors de l’ablation par champ pulsé |
|---|
| Ne provoquent pas de sténose des veines pulmonaires |
| Ne provoquent pas de fistule atrio-œsophagienne |
| Ne provoquent pas de lésion du nerf phrénique |
Après l’ablation de la FA, le succès procédural peut être vérifié de trois façons :
| Vérification du succès de l’ablation de la fibrillation atriale | |||
|---|---|---|---|
| Méthode | Site de stimulation | Ce qui est évalué | Succès |
| Stimulation depuis les veines pulmonaires | Séquentiellement depuis chaque veine pulmonaire (avec le cathéter Farawave) | Propagation des impulsions depuis la veine vers l’oreillette gauche | Absence de réponse atriale = veine isolée |
| Stimulation par salves | Depuis le sinus coronaire (cathéter SC) | Induction d’une FA après salves (8–10 stimuli) | FA non induite ou FA ne durant pas > 1 min = succès |
| Stimulation en rampe | Depuis le sinus coronaire (cathéter SC) | Induction d’une FA lors de la stimulation avec raccourcissement progressif de la longueur de cycle | FA non induite ou FA ne durant pas > 1 min = succès |
Pendant l’ablation par champ pulsé, une électroporation des cardiomyocytes survient, correspondant à une perforation de la membrane cellulaire par un champ électrique. Elle est suivie d’une apoptose. Des enzymes cardiospécifiques sont libérées par les cardiomyocytes lésés et s’élèvent à des niveaux élevés dans les 24 h.
| Enzymes cardiospécifiques dans les 24 h suivant une ablation par champ pulsé | |
|---|---|
| Enzyme | Valeur |
| Troponine | 1500 ng/l (±500) |
| CK | 300 ng/l (±100) |
| CK-MB | 35 mg/l (±10) |
Pendant l’ablation par champ pulsé, une hémolyse survient, se manifestant après la procédure par une hématurie macroscopique.
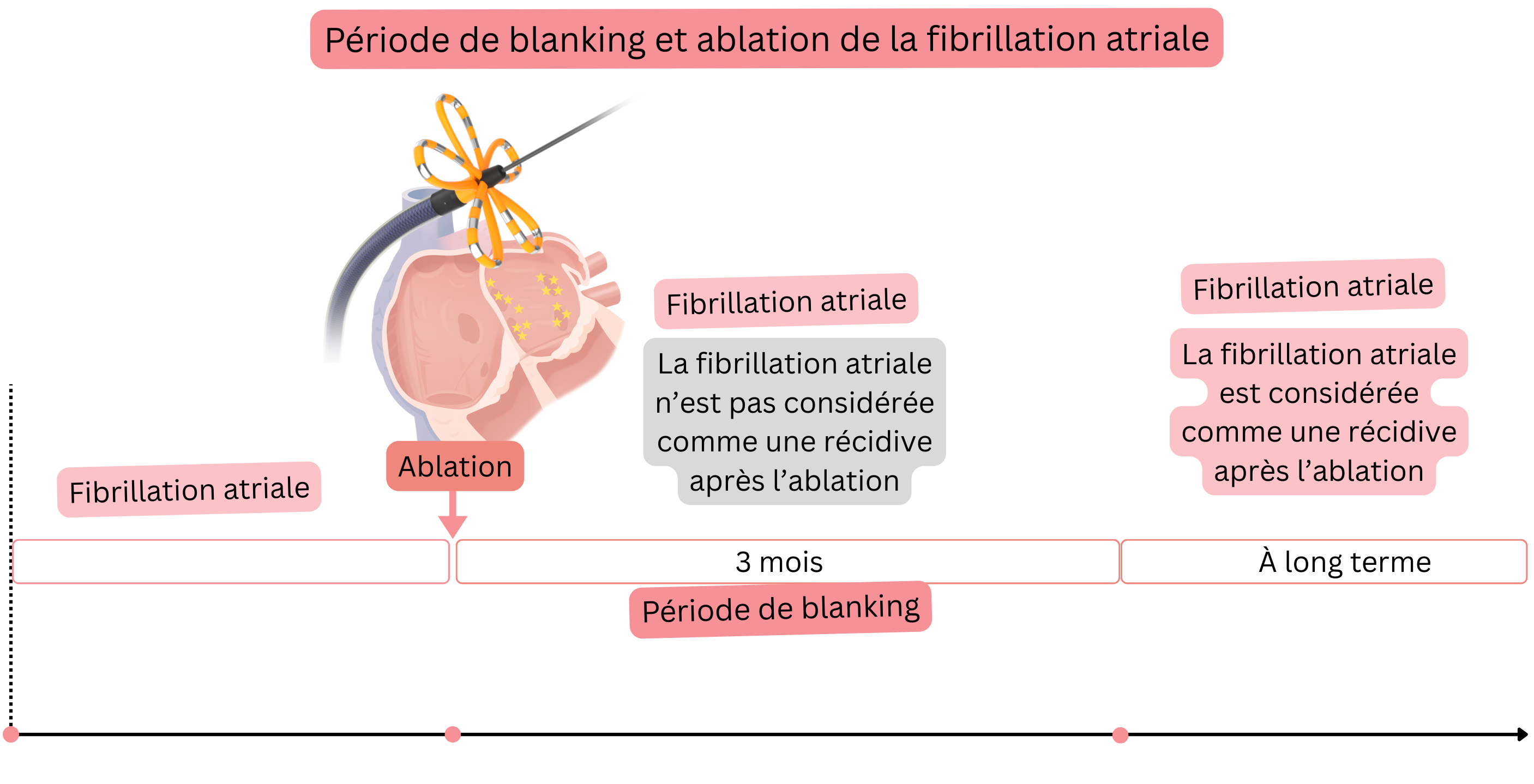
Le succès de l’ablation est évalué par la présence d’une récidive de FA dans l’année suivant l’ablation.
| Succès de l’ablation de la fibrillation atriale (dans les 12 mois) | |
|---|---|
| Classification de la FA | Succès |
| FA paroxystique | 66–82 % |
| FA persistante | 56–72 % |
Période de blanking
| Traitement pendant la période de blanking (3 mois après l’ablation) | ||
|---|---|---|
| Traitement | Durée | Note |
| Antiarythmiques | 3 mois | Administrés quel que soit le rythme (rythme sinusal ou FA). |
| Traitement anticoagulant | 2 mois | Administré indépendamment du score CHA2DS2-VA |
En cas de récidive de FA après ablation — après isolation des veines pulmonaires (par énergie de champ pulsé), une reconnexion d’une veine pulmonaire à l’oreillette gauche peut survenir. La reconnexion survient le plus souvent au niveau de :
Pendant et après une ablation de FA par champ pulsé, des complications peuvent survenir, mais elles sont très rares. L’incidence des complications est :
Les complications majeures et mineures sont listées dans le tableau suivant :
| Complications majeures de l’ablation par champ pulsé | |
|---|---|
| Total | 0,98 % |
| Tamponnade péricardique | 0,36 % |
| Complication vasculaire (nécessitant une intervention) | 0,30 % |
| Spasme coronaire | 0,14 % |
| AVC | 0,12 % |
| Hémolyse avec insuffisance rénale aiguë | 0,03 % |
| Décès | 0,03 % |
| Autres (thrombose, embolie gazeuse coronaire) | 0,006 % |
| Fistule œsophagienne | 0 % |
| Sténose des veines pulmonaires | 0 % |
| Lésion du nerf phrénique (permanente) | 0 % |
| Complications mineures de l’ablation par champ pulsé | |
|---|---|
| Total | 3,21 % |
| Complications vasculaires (ne nécessitant pas d’intervention) | 2,20 % |
| Épanchement péricardique (ne nécessitant pas d’intervention) | 0,33 % |
| Autres complications mineures (hématomes, arythmies) | 0,32 % |
| Péricardite | 0,17 % |
| Accident ischémique transitoire | 0,12 % |
| Lésion du nerf phrénique (transitoire) | 0,06 % |
Chez 5–15 % des patients, une ischémie cérébrale silencieuse asymptomatique survient au cours de l’ablation par champ pulsé.
| Ablation de la fibrillation atriale | Classe |
|---|---|
| L’ablation par champ pulsé (et non la radiofréquence ou la cryoablation) est recommandée comme méthode préférentielle d’ablation de la fibrillation atriale. | I |
L’ablation par champ pulsé est recommandée chez les patients présentant une fibrillation atriale paroxystique ou persistante si la fibrillation atriale est symptomatique :
|
I |
| L’ablation par champ pulsé est recommandée chez les patients présentant une cardiomyopathie induite par la tachycardie due à la fibrillation atriale. | I |
| L’ablation par champ pulsé devrait être envisagée chez les patients atteints de fibrillation atriale présentant des pauses pré-automatiques symptomatiques. | IIa |
En cas de récidive de fibrillation atriale, l’ablation par champ pulsé peut être répétée (pas avant 3 mois) si la fibrillation atriale est symptomatique :
|
IIa |
| Avant une ablation de la fibrillation atriale, une angiographie par CT ou IRM de l’oreillette gauche et des veines pulmonaires devrait être envisagée afin d’évaluer l’anatomie des veines pulmonaires. | IIa |
La stratégie « pace and ablate » peut être envisagée chez les patients présentant une fibrillation atriale symptomatique chez lesquels ont échoué :
|
IIa |
| Traitement anticoagulant et ablation de la fibrillation atriale | Classe |
|---|---|
| Un traitement anticoagulant est recommandé pendant au moins 4 semaines avant l’ablation de la fibrillation atriale, indépendamment du score CHA₂DS₂-VA. | I |
| Il est recommandé de ne pas prendre le traitement anticoagulant par AOD le matin du jour de l’ablation de la fibrillation atriale. | I |
| Il est recommandé de débuter le traitement anticoagulant par AOD 6 h après l’ablation de la fibrillation atriale en l’absence de signes de saignement. | I |
| Sous traitement par warfarine, il est recommandé de réaliser l’ablation de la fibrillation atriale avec un INR thérapeutique d’environ 2,0 le jour de la procédure. | I |
| Un traitement anticoagulant est recommandé pendant les 2 premiers mois après l’ablation de la fibrillation atriale, indépendamment du succès de l’ablation et indépendamment du score CHA₂DS₂-VA. | I |
| Deux mois après l’ablation de la fibrillation atriale, une anticoagulation au long cours est indiquée selon le score CHA₂DS₂-VA, indépendamment du succès de l’ablation. | I |
| Un traitement antiarythmique (propafénone, flécaïnide, sotalol, bêtabloquants) est recommandé pendant les 3 premiers mois après l’ablation de la fibrillation atriale, indépendamment du succès de l’ablation. | I |
| Trois mois après l’ablation de la fibrillation atriale, un traitement antiarythmique est indiqué selon la récidive de fibrillation atriale. | I |
| L’ablation de la fibrillation atriale peut être envisagée si le patient reçoit une bithérapie antithrombotique (p. ex. AOD + clopidogrel). | IIa |
| Ablation de la fibrillation atriale lors d’une chirurgie cardiaque | Classe |
|---|---|
| Chez un patient bénéficiant d’une chirurgie cardiaque de la valve mitrale, une ablation chirurgicale concomitante de la fibrillation atriale selon la procédure Cox-Maze IV est recommandée. | I |
| Chez un patient bénéficiant d’une chirurgie cardiaque autre qu’une chirurgie mitrale, une ablation chirurgicale concomitante de la fibrillation atriale selon la procédure Cox-Maze IV devrait être envisagée. | IIa |
| Lors d’une chirurgie cardiaque, il est recommandé d’exclure la présence de thrombus dans l’oreillette gauche avant une ablation chirurgicale de la fibrillation atriale. | I |
Ces recommandations sont non officielles et ne représentent pas des recommandations formelles émises par une société professionnelle de cardiologie. Elles sont destinées uniquement à des fins éducatives et informatives.
