

Prima dell’ablazione della fibrillazione atriale (FA), è raccomandata una terapia anticoagulante per 4 settimane come prevenzione del tromboembolismo.
Per la prevenzione del tromboembolismo, è raccomandata una terapia anticoagulante per 2 mesi dopo l’ablazione,

L’ecocardiografia transesofagea prima dell’ablazione della FA (<24 h) è raccomandata nonostante 4 settimane di terapia anticoagulante nei seguenti casi:
| ETE prima dell’ablazione – indicazioni nonostante anticoagulazione (4 settimane) |
|---|
| Anamnesi di attacco ischemico transitorio (TIA) |
| Anamnesi di ictus |
| Assunzione irregolare della terapia anticoagulante |
| INR < 2 (durante terapia con warfarin) |
| Anamnesi di trombo intracardiaco (soprattutto nell’auricola sinistra) |
| Anamnesi di velocità di svuotamento dell’auricola sinistra < 20 cm/s |
Prima dell’ablazione della FA, è opportuno sospendere la terapia antiaritmica (se le condizioni del paziente lo consentono).
Prima dell’ablazione, è opportuno sospendere i farmaci antiaritmici utilizzati per il controllo del ritmo (se le condizioni del paziente lo consentono), ma non quelli utilizzati per il controllo della frequenza.

| Sospensione dei farmaci antiaritmici prima dell’ablazione della fibrillazione atriale | ||
|---|---|---|
| Farmaco | Classe | Sospensione prima dell’ablazione |
| Disopiramide | IA | 3–5 giorni |
| Propafenone | IC | 3–5 giorni |
| Flecainide | IC | 3–5 giorni |
| Sotalolo | III | 3–5 giorni |
| Amiodarone | III | 4–6 settimane |
| Dronedarone | III | 3–5 giorni |
L’ablazione della FA (procedura) richiede 3 accessi vascolari tramite introduttori in sede inguinale (vene femorali):
Dopo l’inserimento degli introduttori femorali, vengono somministrate 5000 UI di eparina non frazionata (ENF).
| Dose di ENF e prolungamento dell’ACT | ||
|---|---|---|
| Dose di ENF | ACT a 70 kg (prolungamento rispetto al normale) | ACT a 100 kg (prolungamento rispetto al normale) |
| Nessuna ENF | 80 – 120 s | 80 – 120 s |
| 1000 UI | 120 – 140 s (↑20–40) | 110 – 130 s (↑10–30) |
| 3000 UI | 150 – 180 s (↑50–80) | 130 – 160 s (↑30–60) |
| 5000 UI | 200 – 240 s (↑100–140) | 170 – 210 s (↑70–110) |
| 7000 UI | 230 – 280 s (↑130–180) | 200 – 250 s (↑100–150) |
| 10000 UI | 280 – 340 s (↑180–240) | 230 – 300 s (↑130–200) |
Un trombo in sede degli introduttori venosi e nell’atrio destro sul catetere non è altrettanto pericoloso, poiché embolizza ai polmoni.
| Rischio di formazione di trombo su introduttore o catetere | |
|---|---|
| ACT | Rischio stimato |
| 80 – 120 s (nessuna ENF) | 10–20 % (entro 10–20 min.) |
| 250–300 s | 1–2 % |
| 300–350 s | < 1 % |
Dopo l’introduzione di un ago dedicato tramite la vena femorale nell’atrio destro, viene eseguita una puntura transettale.
ACT ed ENF durante la procedura

Farawave è un catetere dedicato con due configurazioni: basket e flower.
3–5 min prima della prima applicazione, vengono somministrati 1 mg di atropina per via endovenosa (può essere ripetuta fino a una dose massima di 3 mg).
| Atropina – prevenzione della bradicardia prima dell’ablazione | |
|---|---|
| Scopo | Prevenzione della bradicardia |
| Meccanismo | Blocca l’effetto vagale (effetto antimuscarinico) |
| Dose | 1 mg endovenosa (max 3 mg) |
| Inizio d’azione | 1–2 min |
| Effetto atteso | Aumento della frequenza cardiaca di 20–40/min |
| Durata d’azione | 30–60 min |
| Controindicazione | Glaucoma |
Gli impulsi elettrici sono dolorosi; pertanto, vengono erogati in anestesia generale o sedazione.
Se la FA persiste dopo l’isolamento delle vene polmonari, viene eseguita un’ablazione più estesa dell’atrio sinistro:
Auricola sinistra e ablazione.
Se un paziente presenta FA e flutter atriale (AFl),
Durante il pulsing nell’ablazione di FA e AFl, può verificarsi uno spasmo coronarico se l’ablazione viene eseguita in prossimità di un’arteria coronarica.
| Prevenzione dello spasmo coronarico prima dell’ablazione – Isoket vs. nitroglicerina | ||
|---|---|---|
| Farmaco | Isoket (isosorbide dinitrato) | Nitroglicerina |
| Scopo | Prevenzione dello spasmo coronarico più lenta e di maggiore durata | Prevenzione e trattamento rapidi dello spasmo coronarico |
| Meccanismo d’azione | Donatore di NO → vasodilatazione coronarica | Donatore di NO → vasodilatazione coronarica |
| Somministrazione | bolo endovenoso 1–2 mg | bolo endovenoso 50–200 µg |
| Inizio d’azione | 3–5 min | 1–2 min |
| Durata d’azione | 30–60 min | 5–10 min |
| Rischio di ipotensione | Più elevato (durata più lunga) | Più basso (durata breve) |
Modifiche ECG durante ablazione in sede di istmo mitralico e tricuspide:
Gli impulsi elettrici nell’ablazione a campo pulsato sono cardioselettivi:
| Impulsi elettrici nell’ablazione a campo pulsato |
|---|
| Non causano stenosi delle vene polmonari |
| Non causano fistola atrio-esofagea |
| Non causano lesione del nervo frenico |
Dopo l’ablazione della FA, il successo procedurale può essere verificato in tre modi:
| Verifica del successo dell’ablazione della fibrillazione atriale | |||
|---|---|---|---|
| Metodo | Sede di stimolazione | Cosa viene valutato | Successo |
| Stimolazione dalle vene polmonari | Sequenzialmente da ciascuna vena polmonare (con il catetere Farawave) | Se gli impulsi dalla vena si propagano all’atrio sinistro | Nessuna risposta atriale = vena isolata |
| Burst pacing | Dal seno coronarico (catetere CS) | Induzione di FA dopo burst (8–10 stimoli) | FA non indotta oppure FA non dura > 1 min = successo |
| Ramp pacing | Dal seno coronarico (catetere CS) | Se la FA viene indotta durante stimolazione con progressiva riduzione del ciclo | FA non indotta oppure FA non dura > 1 min = successo |
Durante l’ablazione a campo pulsato si verifica elettroporazione dei cardiomiociti, cioè perforazione della membrana cellulare indotta da un campo elettrico. Segue apoptosi. Enzimi cardiospecifici vengono rilasciati dai cardiomiociti danneggiati e aumentano a valori elevati entro 24 h.
| Enzimi cardiospecifici entro 24 h dopo ablazione a campo pulsato | |
|---|---|
| Enzima | Valore |
| Troponina | 1500 ng/l (±500) |
| CK | 300 ng/l (±100) |
| CK-MB | 35 mg/l (±10) |
Durante l’ablazione a campo pulsato si verifica emolisi, che si manifesta dopo la procedura come ematuria macroscopica.
Il successo dell’ablazione viene valutato in base alla presenza di recidiva di FA entro 1 anno dopo l’ablazione.
| Successo dell’ablazione della fibrillazione atriale (entro 12 mesi) | |
|---|---|
| Classificazione della FA | Successo |
| FA parossistica | 66–82 % |
| FA persistente | 56–72 % |
Periodo di blanking
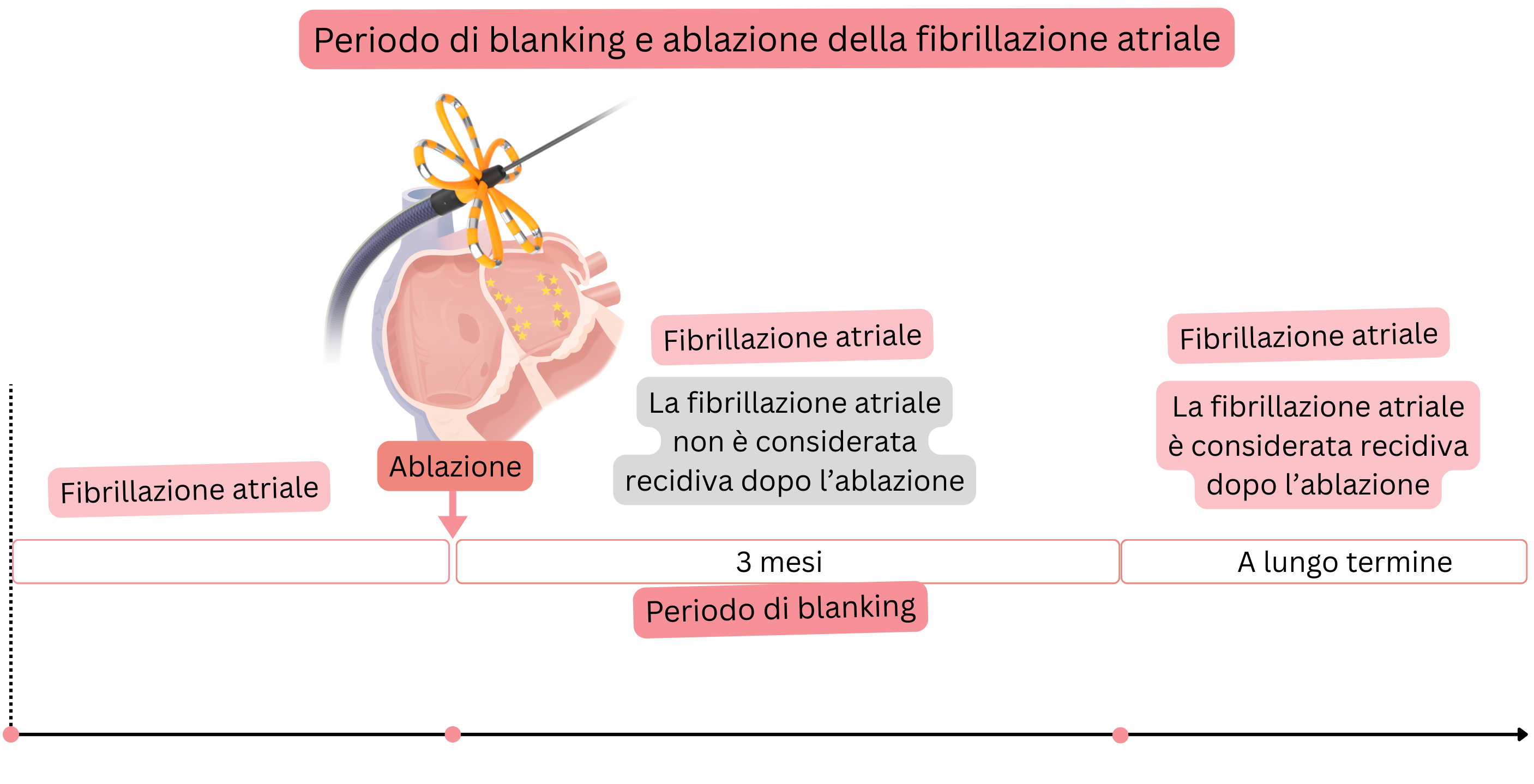
| Terapia durante il periodo di blanking (3 mesi dopo ablazione) | ||
|---|---|---|
| Terapia | Durata | Nota |
| Farmaci antiaritmici | 3 mesi | Somministrati indipendentemente dalla presenza di ritmo sinusale o FA. |
| Terapia anticoagulante | 2 mesi | Somministrata indipendentemente dal punteggio CHA2DS2-VA |
In caso di recidiva di FA dopo ablazione—isolamento delle vene polmonari (con energia a campo pulsato), può verificarsi ricanalizzazione di una vena polmonare verso l’atrio sinistro. La ricanalizzazione si verifica più comunemente in:
Durante e dopo l’ablazione della FA a campo pulsato possono verificarsi complicanze, ma sono molto rare. L’incidenza delle complicanze è:
Le complicanze maggiori e minori sono elencate nella seguente tabella:
| Complicanze maggiori dell’ablazione a campo pulsato | |
|---|---|
| Totale | 0.98 % |
| Tamponamento pericardico | 0.36 % |
| Complicanza vascolare (che richiede intervento) | 0.30 % |
| Spasmo coronarico | 0.14 % |
| Ictus | 0.12 % |
| Emolisi con insufficienza renale acuta | 0.03 % |
| Morte | 0.03 % |
| Altro (trombosi, embolia coronarica gassosa) | 0.006 % |
| Fistola esofagea | 0 % |
| Stenosi delle vene polmonari | 0 % |
| Lesione del nervo frenico (permanente) | 0 % |
| Complicanze minori dell’ablazione a campo pulsato | |
|---|---|
| Totale | 3.21 % |
| Complicanze vascolari (che non richiedono intervento) | 2.20 % |
| Versamento pericardico (che non richiede intervento) | 0.33 % |
| Altre complicanze minori (ematomi, aritmie) | 0.32 % |
| Pericardite | 0.17 % |
| Attacco ischemico transitorio | 0.12 % |
| Lesione del nervo frenico (temporanea) | 0.06 % |
Nel 5–15% dei pazienti, durante l’ablazione a campo pulsato si verifica ischemia cerebrale silente asintomatica.
| Ablazione della fibrillazione atriale | Classe |
|---|---|
| L’ablazione a campo pulsato (non radiofrequenza o crioblazione) è raccomandata come metodo preferenziale per l’ablazione della fibrillazione atriale. | I |
L’ablazione a campo pulsato è raccomandata nei pazienti con fibrillazione atriale parossistica o persistente se la fibrillazione atriale è sintomatica:
|
I |
| L’ablazione a campo pulsato è raccomandata nei pazienti con cardiomiopatia indotta da tachicardia dovuta a fibrillazione atriale. | I |
| L’ablazione a campo pulsato dovrebbe essere presa in considerazione nei pazienti con fibrillazione atriale che presentano pause pre-automatiche sintomatiche. | IIa |
In caso di recidiva di fibrillazione atriale, l’ablazione a campo pulsato può essere ripetuta (non prima di 3 mesi) se la fibrillazione atriale è sintomatica:
|
IIa |
| Prima dell’ablazione della fibrillazione atriale, angiografia TC o RM dell’atrio sinistro e delle vene polmonari dovrebbe essere presa in considerazione per valutare l’anatomia delle vene polmonari. | IIa |
La strategia “pace and ablate” può essere presa in considerazione nei pazienti con fibrillazione atriale sintomatica nei quali hanno fallito:
|
IIa |
| Terapia anticoagulante e ablazione della fibrillazione atriale | Classe |
|---|---|
| È raccomandata terapia anticoagulante per almeno 4 settimane prima dell’ablazione della fibrillazione atriale, indipendentemente dal punteggio CHA₂DS₂-VA. | I |
| È raccomandato non assumere la terapia anticoagulante con NOAC al mattino nel giorno dell’ablazione della fibrillazione atriale. | I |
| È raccomandato iniziare la terapia anticoagulante con NOAC 6 h dopo l’ablazione della fibrillazione atriale se non vi sono segni di sanguinamento. | I |
| Durante terapia con warfarin, è raccomandato eseguire l’ablazione della fibrillazione atriale con INR terapeutico di circa 2.0 nel giorno della procedura. | I |
| È raccomandata terapia anticoagulante per i primi 2 mesi dopo l’ablazione della fibrillazione atriale, indipendentemente dal successo dell’ablazione e indipendentemente dal punteggio CHA₂DS₂-VA. | I |
| A due mesi dall’ablazione della fibrillazione atriale, l’anticoagulazione a lungo termine è indicata in base al punteggio CHA₂DS₂-VA, indipendentemente dal successo dell’ablazione. | I |
| È raccomandata terapia antiaritmica (propafenone, flecainide, sotalolo, beta-bloccanti) per i primi 3 mesi dopo l’ablazione della fibrillazione atriale, indipendentemente dal successo dell’ablazione. | I |
| A tre mesi dall’ablazione della fibrillazione atriale, la terapia antiaritmica è indicata in base alla recidiva di fibrillazione atriale. | I |
| L’ablazione della fibrillazione atriale può essere presa in considerazione se il paziente è in terapia antitrombotica duale (ad esempio NOAC + clopidogrel). | IIa |
| Ablazione della fibrillazione atriale durante cardiochirurgia | Classe |
|---|---|
| In un paziente sottoposto a cardiochirurgia sulla valvola mitrale, è raccomandata l’ablazione chirurgica concomitante della fibrillazione atriale mediante procedura Cox-Maze IV. | I |
| In un paziente sottoposto a cardiochirurgia diversa dalla chirurgia della valvola mitrale, l’ablazione chirurgica concomitante della fibrillazione atriale mediante procedura Cox-Maze IV dovrebbe essere presa in considerazione. | IIa |
| Durante la cardiochirurgia, è raccomandato escludere la presenza di trombo nell’atrio sinistro prima dell’ablazione chirurgica della fibrillazione atriale. | I |
Queste linee guida sono non ufficiali e non rappresentano linee guida formali emesse da alcuna società professionale di cardiologia. Sono destinate esclusivamente a scopi educativi e informativi.
