

Przewlekły zespół wieńcowy (CCS)

Ostry zespół wieńcowy (ACS)
Zawał serca typu 1
Zawał serca typu 2
Rewaskularyzacja to przywrócenie przepływu krwi przez zwężenie lub okluzję tętnicy wieńcowej. Metody rewaskularyzacji obejmują:
ACS jest ostrym stanem krytycznym, który może wywołać lub nasilić epizod MP.
Częstość nowo występującego MP w ciągu 24 godzin po ACS wynosi 2–23 %.
10–15 % pacjentów z MP poddaje się PCI z powodu choroby tętnic wieńcowych.
Tachy-MP (częstość komór >100/min) może powodować zawał serca typu 2.
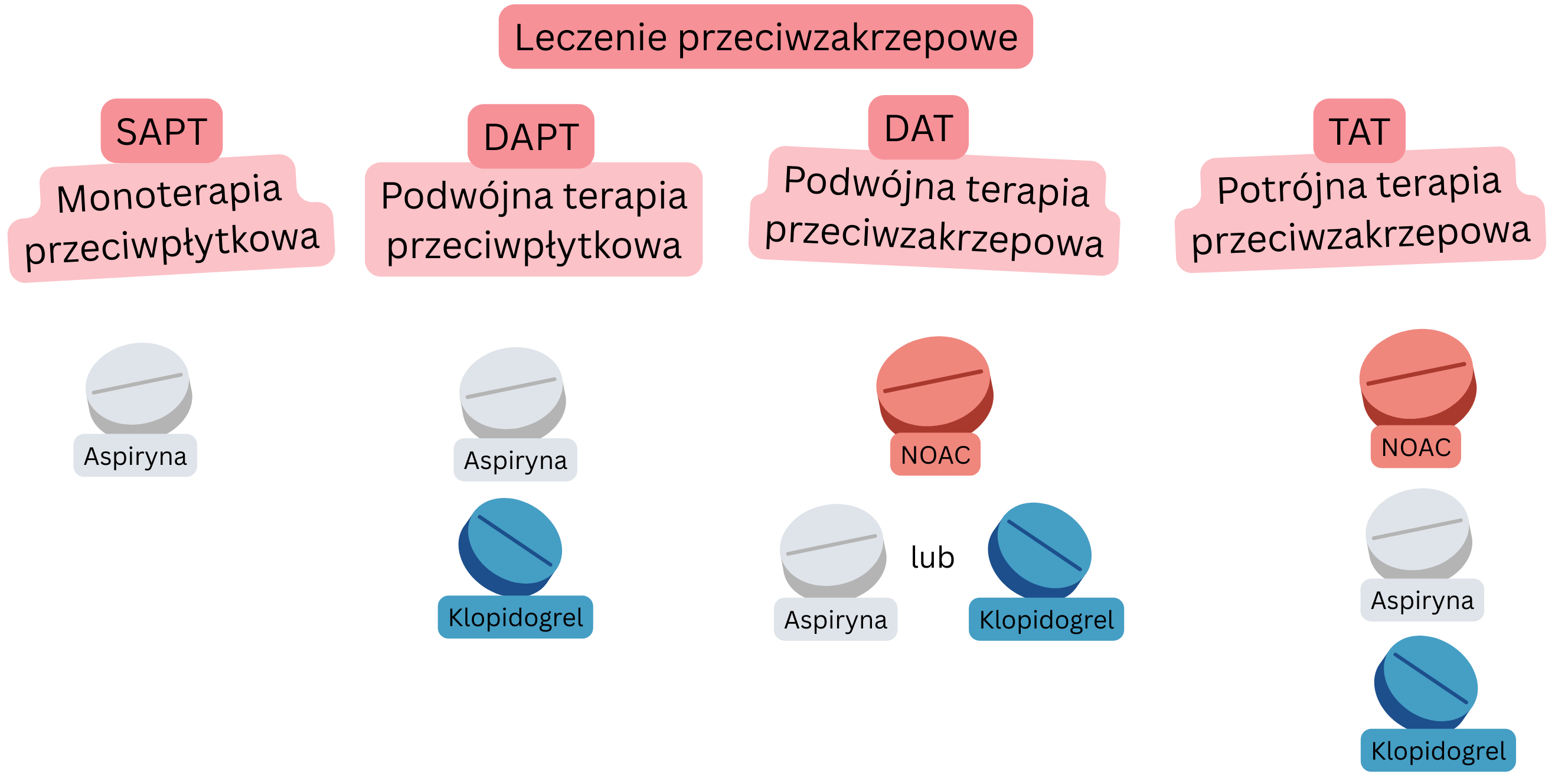
Pacjenci z ACS i MP wymagają skojarzonej terapii przeciwzakrzepowej:
| Terapia przeciwzakrzepowa (Terminologia) w zespole wieńcowym i migotaniu przedsionków | |||
|---|---|---|---|
| Termin | Definicja | Najczęstsze połączenie | Najczęstsze zastosowanie |
| SAPT (Single Antiplatelet Therapy) |
1 lek przeciwpłytkowy | Aspiryna | Profilaktyka w CCS u pacjentów bez MP |
| DAPT (Dual Antiplatelet Therapy) |
2 leki przeciwpłytkowe | Aspiryna + klopidogrel | 6 miesięcy po PCI ze stentem u pacjentów bez MP |
| DAT (Dual Antithrombotic Therapy) |
Leczenie przeciwkrzepliwe + leczenie przeciwpłytkowe | NOAC + klopidogrel | 12 miesięcy po PCI u pacjentów z MP |
| TAT (Triple Antithrombotic Therapy) |
Leczenie przeciwkrzepliwe + DAPT | NOAC + Aspiryna + klopidogrel |
Pierwszy tydzień po PCI u pacjentów z MP (na NOAC) |
NOAC – Non-vitamin K Oral Anticoagulant, P2Y12 – P2Y12 adenosine diphosphate (ADP) receptor inhibitor (e.g. Clopidogrel, Prasugrel, Ticagrelor), CCS – Chronic coronary syndrome, PCI – Percutaneous coronary intervention (coronary angioplasty with stent)
ACS po PCI wymaga leczenia przeciwpłytkowego; dlatego pacjenci z MP (jeżeli wymagają leczenia przeciwkrzepliwego) oraz ACS po PCI wymagają:
W ACS i MP preferuje się NOAC (a nie warfarynę) jako leczenie przeciwkrzepliwe.
Preferowanym inhibitorem P2Y12 jest klopidogrel (a nie tikagrelor i prasugrel).
Nie zaleca się łączenia leczenia przeciwkrzepliwego (warfaryna lub NOAC) z (tikagrelorem lub prasugrelem),
Podczas DAT (warfaryna + leczenie przeciwpłytkowe)
Preferowaną DAT w MP po ACS lub po PCI jest:
Podczas TAT i DAT zaleca się stosowanie inhibitorów pompy protonowej (pantoprazol) w profilaktyce krwawienia z przewodu pokarmowego.
U pacjentów z MP i stabilnym CCS zaleca się wyłącznie leczenie przeciwkrzepliwe (a nie DAT).
| Leczenie przeciwkrzepliwe i przeciwpłytkowe w migotaniu przedsionków | Klasa |
|---|---|
| W terapii skojarzonej (OAC + leczenie przeciwpłytkowe) preferuje się NOAC (a nie warfarynę) jako OAC ze względu na niższe ryzyko krwawienia i lepszą prewencję zdarzeń zakrzepowo-zatorowych. | I |
| Jeżeli pacjent przyjmuje (riwaroksaban + leczenie przeciwpłytkowe), można rozważyć redukcję dawki riwaroksabanu 20 mg → 15 mg raz na dobę w celu zmniejszenia ryzyka krwawienia. | IIa |
| Jeżeli pacjent przyjmuje (dabigatran + leczenie przeciwpłytkowe), można rozważyć redukcję dawki dabigatranu 150 mg → 110 mg dwa razy na dobę w celu zmniejszenia ryzyka krwawienia. | IIa |
| Jeżeli pacjent przyjmuje (warfaryna + leczenie przeciwpłytkowe), można rozważyć docelowy INR 2–2,5 w celu zmniejszenia ryzyka krwawienia. | IIa |
OAC - Oral anticoagulation, NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
| Ostry zespół wieńcowy a migotanie przedsionków | Klasa |
|---|---|
U pacjentów z MP i ACS po PCI (niskie ryzyko niedokrwienne) zaleca się:
|
I |
U pacjentów z MP i ACS po PCI (wysokie ryzyko niedokrwienne) zaleca się:
|
IIa |
NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), ACS – Acute coronary syndrome, PCI – Percutaneous coronary intervention
| Wysokie ryzyko niedokrwienne po przezskórnej interwencji wieńcowej (PCI) | |
|---|---|
| Wywiad zakrzepicy w stencie (pomimo adekwatnej terapii przeciwpłytkowej) | |
| Implantacja stentu w ostatniej drożnej tętnicy wieńcowej | |
| Rozlana choroba tętnic wieńcowych (zwłaszcza u pacjentów z cukrzycą) | |
| Przewlekła choroba nerek kreatynina ≥133 µmol/L (CrCl <60 ml/min) | |
| Implantacja ≥3 stentów | |
| Leczenie ≥3 zmian w tętnicach wieńcowych | |
| Leczenie zmiany w miejscu rozwidlenia z użyciem 2 stentów | |
| Całkowita długość stentów >60 mm | |
| Leczenie CTO (Chronic Total Occlusion) | |
| Przewlekły zespół wieńcowy a migotanie przedsionków | Klasa |
|---|---|
U pacjentów z MP i CCS po PCI (niskie ryzyko niedokrwienne) zaleca się:
|
I |
U pacjentów z MP i CCS po PCI (wysokie ryzyko niedokrwienne) zaleca się:
|
IIa |
NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), CCS - Chronic coronary syndrome, PCI – Percutaneous coronary intervention
| Czas trwania leczenia przeciwpłytkowego po ACS u pacjentów z migotaniem przedsionków | Klasa |
|---|---|
| U stabilnych pacjentów po ACS z MP nie zaleca się kontynuowania leczenia przeciwpłytkowego powyżej 12 miesięcy. | III |
ACS – Acute coronary syndrome
| Terapia przeciwzakrzepowa w ACS, CCS i migotaniu przedsionków | Klasa |
|---|---|
| NOAC (a nie warfaryna) są preferowanym leczeniem przeciwkrzepliwym w skojarzeniu z leczeniem przeciwpłytkowym. | I |
| Dawki NOAC redukuje się zgodnie ze standardowymi kryteriami redukcji dawki NOAC. | I |
| Podczas leczenia (warfaryna + leczenie przeciwpłytkowe) można rozważyć docelowy INR 2–2,5. | IIa |
| Podczas terapii warfaryną (bez leczenia przeciwpłytkowego) zaleca się docelowy INR 2–3. | I |
| Preferowanym inhibitorem P2Y12 w skojarzeniu z leczeniem przeciwkrzepliwym jest klopidogrel (a nie tikagrelor ani prasugrel). | IIa |
ACS – Acute coronary syndrome, CCS - Chronic coronary syndrome, NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
Wszyscy poniżsi pacjenci:

ACS po PCI (Niskie ryzyko niedokrwienne)
Przykład: Pacjent z MP (na NOAC) przebył zawał (STEMI lub NSTEMI), został przekazany do ośrodka kardiologicznego, gdzie wykonano PCI z implantacją 1 stentu w tętnicy okalającej.

ACS po PCI (Wysokie ryzyko niedokrwienne)
Przykład: Pacjent z MP przebył zawał (STEMI lub NSTEMI), został przekazany do ośrodka kardiologicznego, gdzie wykonano PCI z implantacją 3 stentów.

CCS po PCI (Niskie ryzyko niedokrwienne)
Przykład: Pacjent z MP (na NOAC) miał stabilną dławicę piersiową i istotne zwężenie wieńcowe (>70 %) w angiografii CT tętnic wieńcowych; wykonano PCI z implantacją 1 stentu w prawej tętnicy wieńcowej.

CCS po PCI (Wysokie ryzyko niedokrwienne)
Przykład: Pacjent z MP (na NOAC) miał stabilną dławicę piersiową; koronarografia wykazała 3 ciężkie zwężenia (>70 %), a podczas PCI implantowano 3 stenty.

Stabilny CCS
Przykład: Pacjent z MP (na NOAC) ma CCS z nieistotnym zwężeniem wieńcowym (<50 %), bez wskazań do PCI.
U pacjentów po PCI ryzyko krwawienia ocenia się za pomocą skali ARC-HBR (Academic Research Consortium – High Bleeding Risk).
| Skala ARC-HBR (Ryzyko krwawienia) |
|---|
Kryteria duże (wystarczy 1)
|
Kryteria małe (wymagane ≥2)
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban). eGFR = estimated Glomerular Filtration Rate. NSAIDs - non-steroidal anti-inflammatory drugs
| Ryzyko krwawienia według skali ARC-HBR oraz skrócenie terapii przeciwzakrzepowej po PCI | ||
|---|---|---|
| Skala ARC-HBR | Ryzyko dużego krwawienia (w ciągu 1 roku po PCI) |
Terapia przeciwzakrzepowa po PCI |
| Dodatnia (≥ 1 kryterium duże lub ≥ 2 kryteria małe) |
4 – 9 % |
|
| Ujemna | 1 – 3 % |
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. DAT - Dual Antithrombotic Therapy. TAT - Triple Antithrombotic Therapy.
Niniejsze wytyczne są nieoficjalne i nie stanowią oficjalnych wytycznych wydanych przez żadne profesjonalne towarzystwo kardiologiczne. Służą wyłącznie celom edukacyjnym i informacyjnym.
