

慢性冠動脈症候群(CCS)
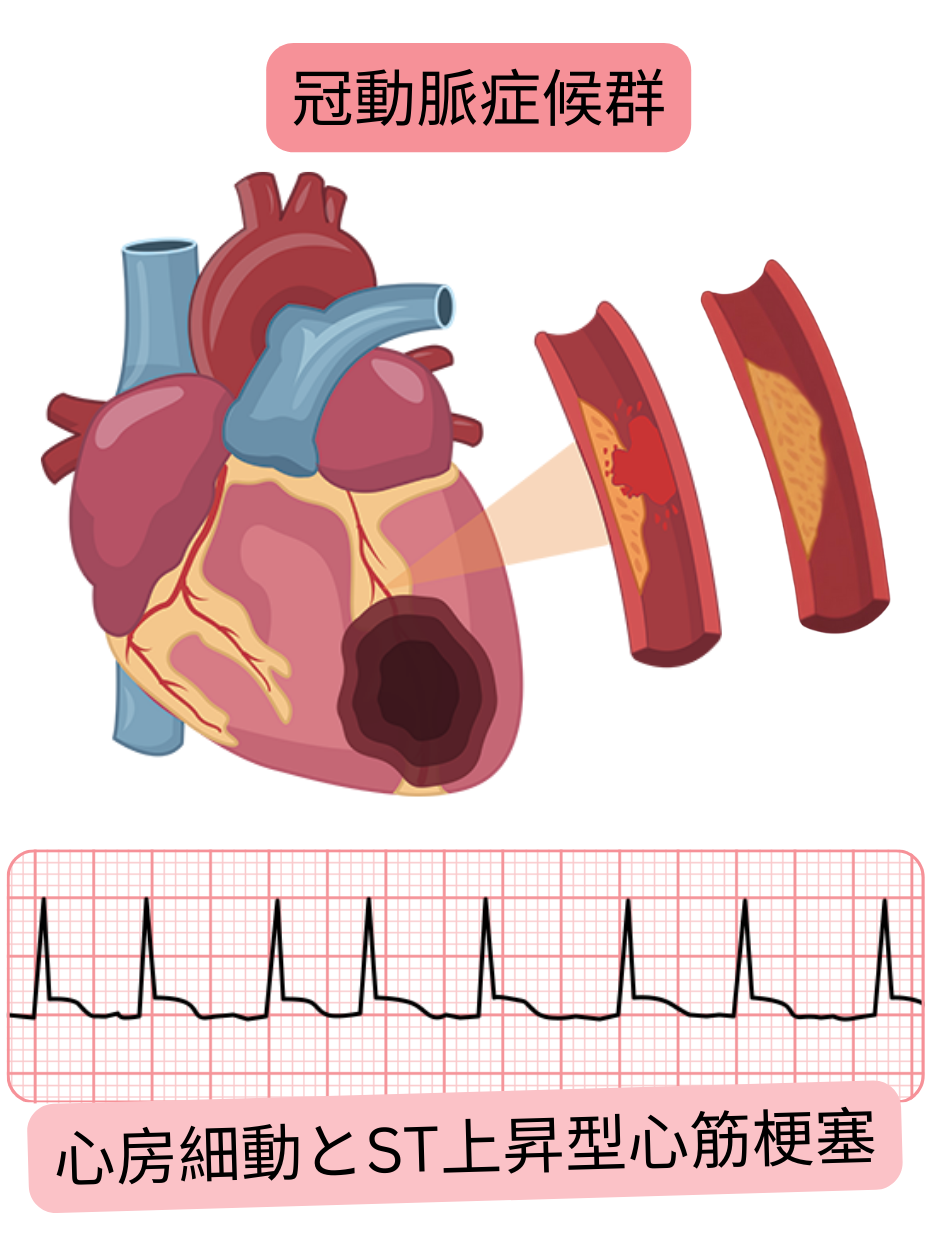
急性冠動脈症候群(ACS)
1型心筋梗塞
2型心筋梗塞
血行再建は、冠動脈狭窄または閉塞部位を越えて血流を再開させることである。血行再建法には以下が含まれる:
ACSは心房細動発作を誘発または増悪させ得る急性重篤病態である。
ACS後24時間以内の新規発症心房細動の頻度は2–23%である。
心房細動患者の10–15%が冠動脈疾患に対してPCIを受ける。
頻脈性心房細動(心室拍数>100/分)は2型心筋梗塞を来し得る。
ACSと心房細動を合併する患者では、抗血栓療法の併用を要する:
| 冠動脈症候群と心房細動における抗血栓療法(用語) | |||
|---|---|---|---|
| 用語 | 定義 | 最も一般的な組合せ | 最も一般的な使用 |
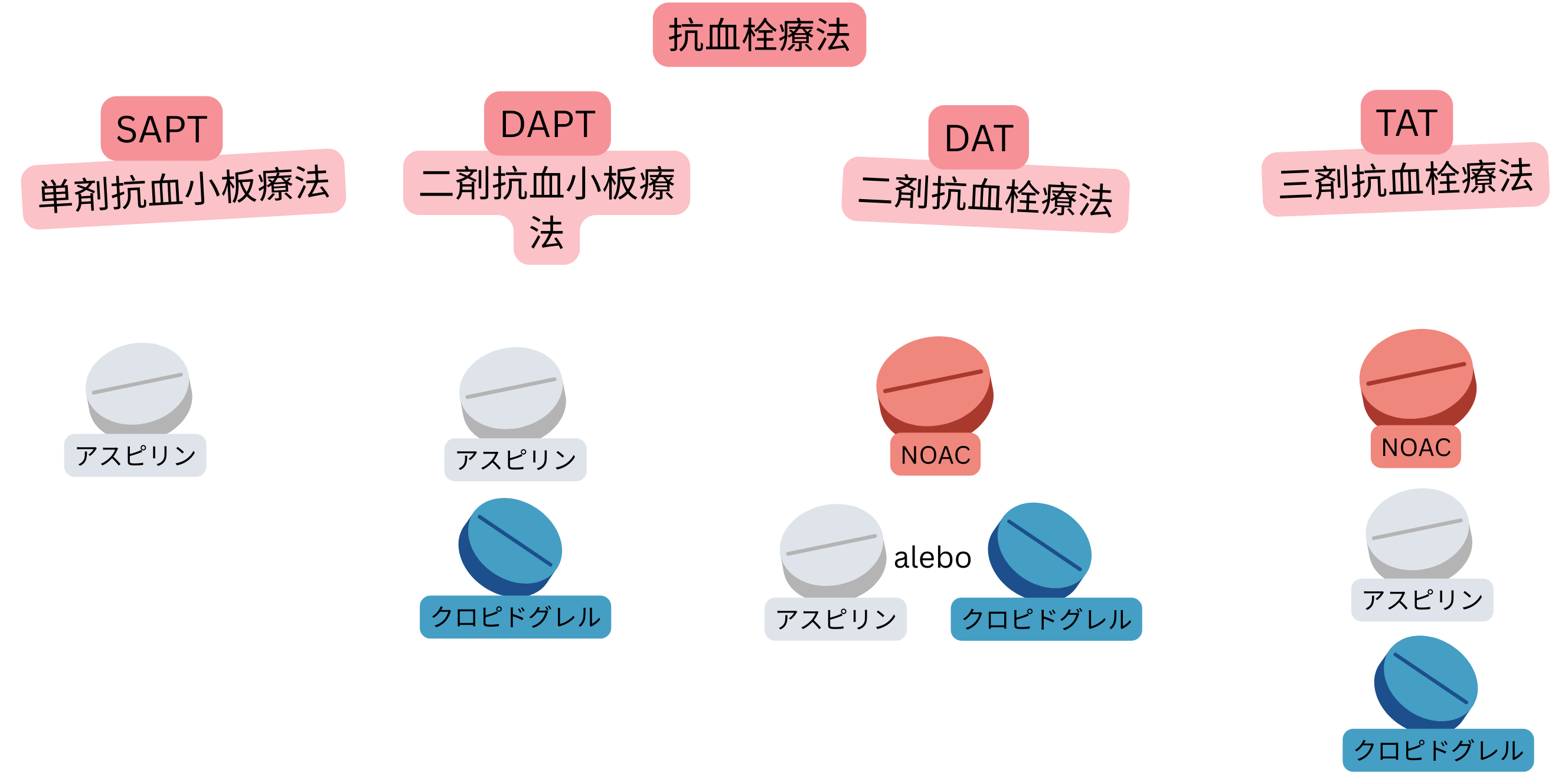
| SAPT (Single Antiplatelet Therapy) |
抗血小板薬1剤 | アスピリン | 心房細動を伴わないCCS患者の予防 |
| DAPT (Dual Antiplatelet Therapy) |
抗血小板薬2剤 | アスピリン + クロピドグレル | 心房細動を伴わない患者のステント留置後PCI後6か月 |
| DAT (Dual Antithrombotic Therapy) |
抗凝固療法 + 抗血小板療法 | NOAC + クロピドグレル | 心房細動患者のPCI後12か月 |
| TAT (Triple Antithrombotic Therapy) |
抗凝固療法 + DAPT | NOAC + アスピリン + クロピドグレル |
心房細動患者(NOAC内服中)のPCI後最初の1週間 |
NOAC – Non-vitamin K Oral Anticoagulant, P2Y12 – P2Y12 adenosine diphosphate (ADP) receptor inhibitor (e.g. Clopidogrel, Prasugrel, Ticagrelor), CCS – Chronic coronary syndrome, PCI – Percutaneous coronary intervention (coronary angioplasty with stent)
PCI後ACSでは抗血小板療法を要するため、心房細動患者(抗凝固療法が必要な場合)でPCI後ACSを合併する場合には、以下を要する:
ACSと心房細動の合併では、抗凝固療法としてNOAC(ワルファリンではなく)を優先する。
推奨されるP2Y12阻害薬はクロピドグレル(チカグレロルおよびプラスグレルではない)である。
抗凝固療法(ワルファリンまたはNOAC)と(チカグレロルまたはプラスグレル)の併用は推奨されない。
DAT(ワルファリン + 抗血小板療法)中は、
ACS後またはPCI後の心房細動における推奨DATは以下である:
TATおよびDAT施行中は、消化管出血予防としてプロトンポンプ阻害薬(パントプラゾール)を推奨する。
心房細動を有し安定したCCSの患者では、抗凝固療法単独を推奨する(DATではない)。
| 心房細動における抗凝固療法および抗血小板療法 | クラス |
|---|---|
| 併用療法(OAC + 抗血小板療法)では、出血リスクが低く血栓塞栓症予防効果が良好であるため、OACとしてNOAC(ワルファリンではなく)を優先する。 | I |
| (リバーロキサバン + 抗血小板療法)内服中の患者では、出血リスク低減のため、リバーロキサバンの用量減量20 mg → 15 mg 1日1回を考慮してよい。 | IIa |
| (ダビガトラン + 抗血小板療法)内服中の患者では、出血リスク低減のため、ダビガトランの用量減量150 mg → 110 mg 1日2回を考慮してよい。 | IIa |
| (ワルファリン + 抗血小板療法)内服中の患者では、出血リスク低減のため、目標INR 2–2.5を考慮してよい。 | IIa |
OAC - Oral anticoagulation, NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
| 急性冠動脈症候群と心房細動 | クラス |
|---|---|
心房細動を合併し、PCI後ACS(虚血リスク低)である患者では、以下を推奨する:
|
I |
心房細動を合併し、PCI後ACS(虚血リスク高)である患者では、以下を推奨する:
|
IIa |
NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), ACS – Acute coronary syndrome, PCI – Percutaneous coronary intervention
| 経皮的冠動脈インターベンション(PCI)後の高虚血リスク | |
|---|---|
| ステント血栓症の既往(適切な抗血小板療法にもかかわらず) | |
| 最後に開存する冠動脈へのステント留置 | |
| びまん性冠動脈疾患(特に糖尿病患者) | |
| 慢性腎臓病 クレアチニン ≥133 µmol/L(CrCl <60 ml/min) | |
| ≥3本のステント留置 | |
| ≥3病変の治療 | |
| 2本ステントによる分岐部病変治療 | |
| 総ステント長 >60 mm | |
| CTO(Chronic Total Occlusion)の治療 | |
| 慢性冠動脈症候群と心房細動 | クラス |
|---|---|
心房細動を合併し、PCI後CCS(虚血リスク低)である患者では、以下を推奨する:
|
I |
心房細動を合併し、PCI後CCS(虚血リスク高)である患者では、以下を推奨する:
|
IIa |
NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), CCS - Chronic coronary syndrome, PCI – Percutaneous coronary intervention
| 心房細動を伴うACS後の抗血小板療法期間 | クラス |
|---|---|
| ACS後の心房細動を伴う安定患者において、抗血小板療法を12か月を超えて継続することは推奨されない。 | III |
ACS – Acute coronary syndrome
| ACS、CCS、および心房細動における抗血栓療法 | クラス |
|---|---|
| 抗血小板療法との併用における抗凝固療法としては、NOAC(ワルファリンではなく)を優先する。 | I |
| NOACの用量は、標準的なNOAC減量基準に従い減量する。 | I |
| (ワルファリン + 抗血小板療法)治療中は、目標INR 2–2.5を考慮してよい。 | IIa |
| ワルファリン単独療法(抗血小板療法なし)では、目標INR 2–3を推奨する。 | I |
| 抗凝固療法との併用における推奨P2Y12阻害薬は、クロピドグレル(チカグレロルまたはプラスグレルではない)である。 | IIa |
ACS – Acute coronary syndrome, CCS - Chronic coronary syndrome, NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
以下のすべての患者:
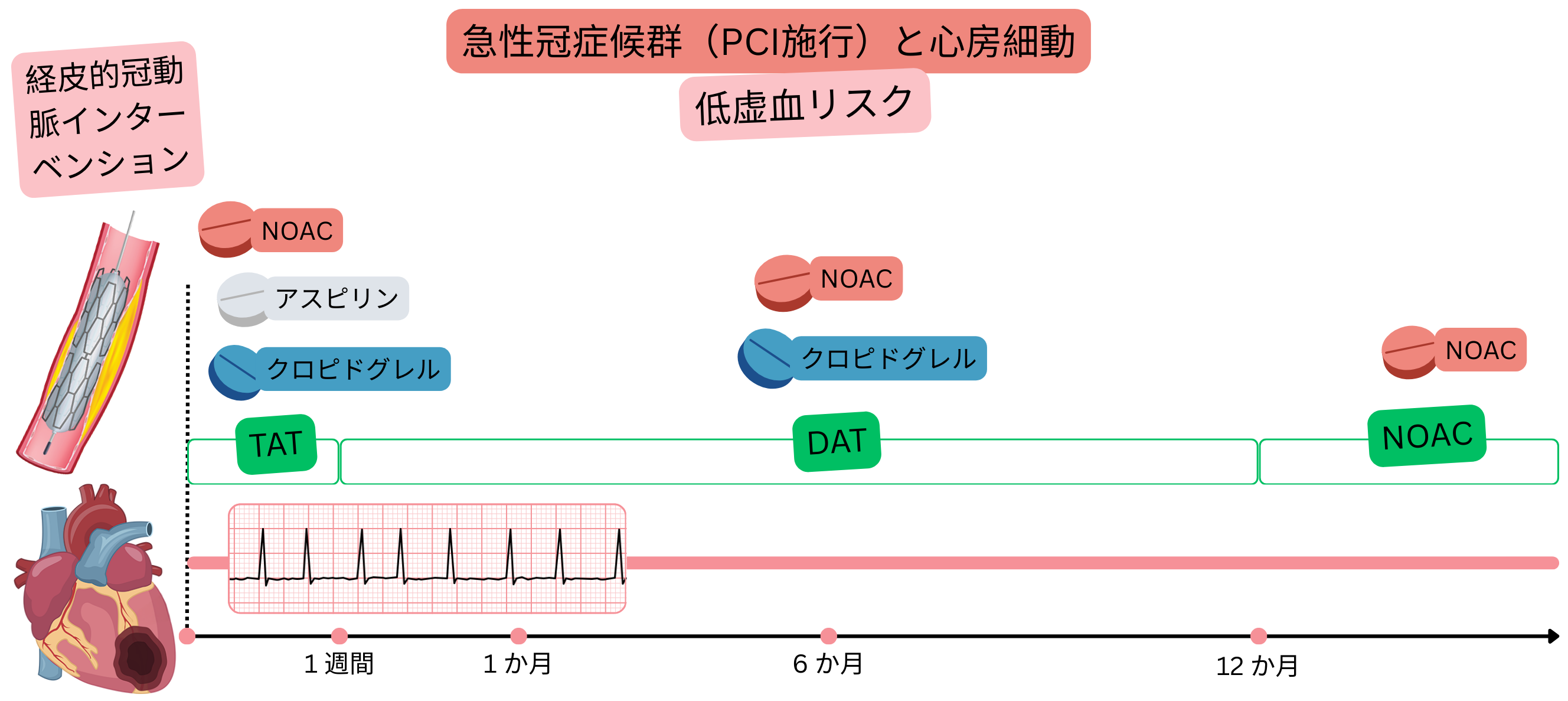
PCI後ACS(虚血リスク低)
例:心房細動患者(NOAC内服中)が梗塞(STEMIまたはNSTEMI)を発症し、心臓センターへ搬送され、回旋枝に1本のステント留置を伴うPCIを施行した。
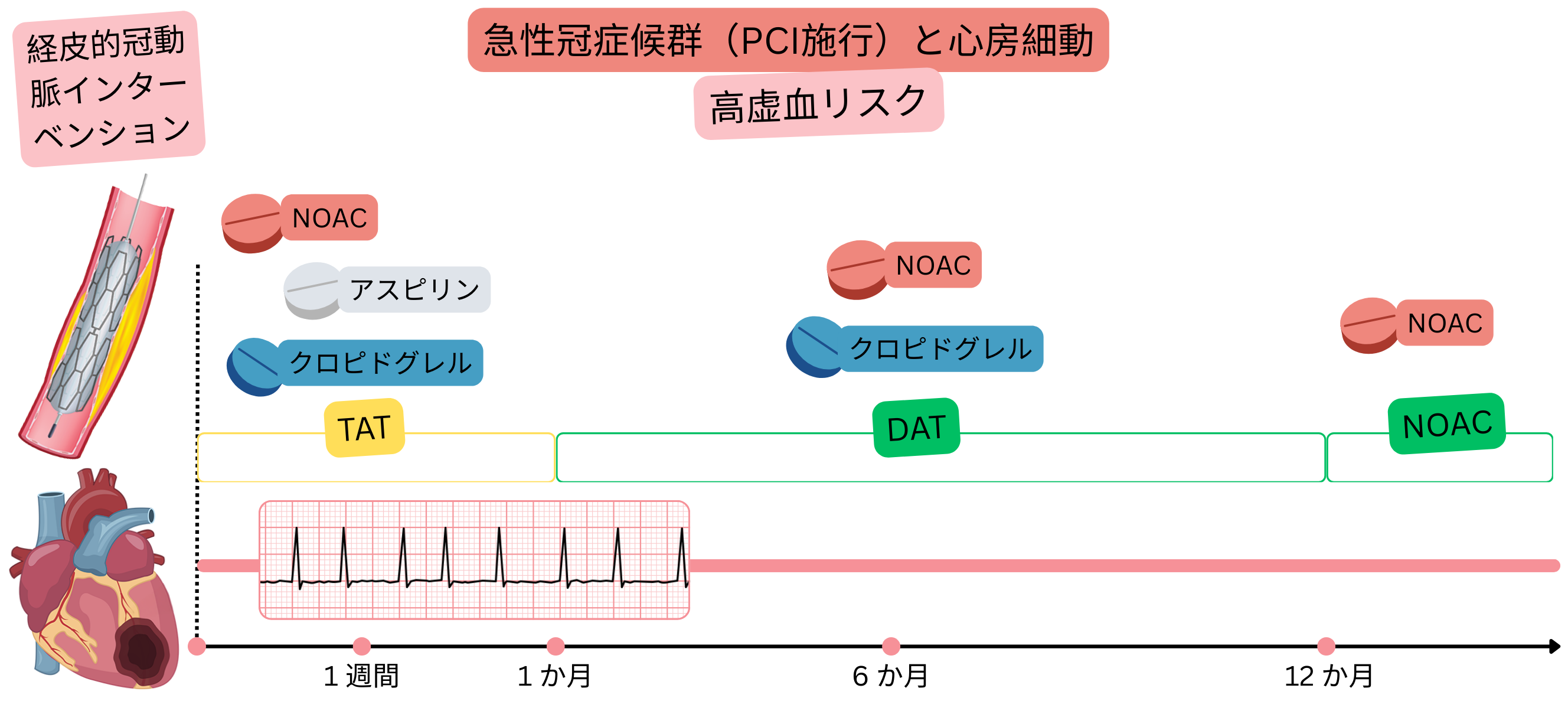
PCI後ACS(虚血リスク高)
例:心房細動患者が梗塞(STEMIまたはNSTEMI)を発症し、心臓センターへ搬送され、PCIで3本のステントを留置した。
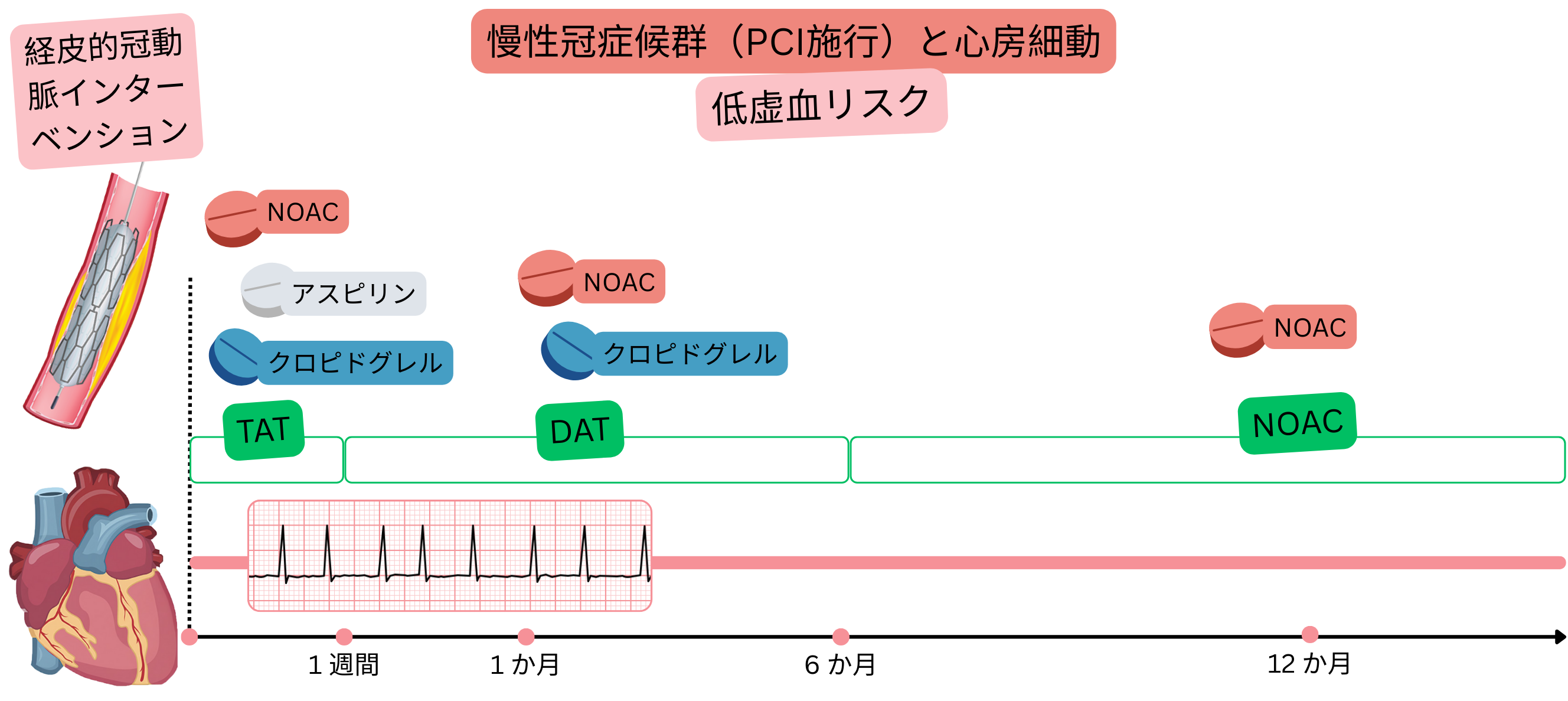
PCI後CCS(虚血リスク低)
例:心房細動患者(NOAC内服中)が安定狭心症を有し、CT冠動脈造影で有意冠動脈狭窄(>70%)を認め、右冠動脈に1本のステント留置を伴うPCIを施行した。
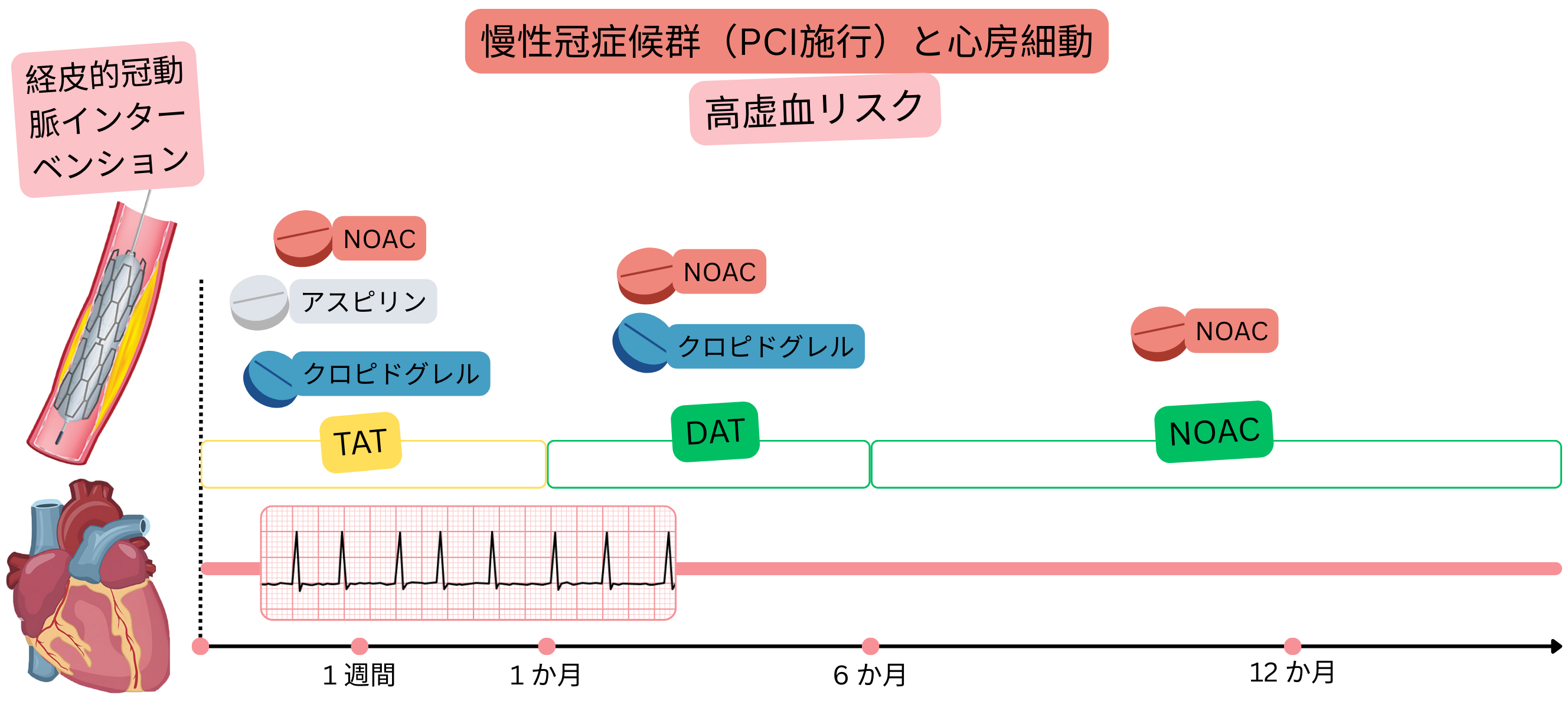
PCI後CCS(虚血リスク高)
例:心房細動患者(NOAC内服中)が安定狭心症を有し、冠動脈造影で重症狭窄(>70%)を3か所に認め、PCIで3本のステントを留置した。
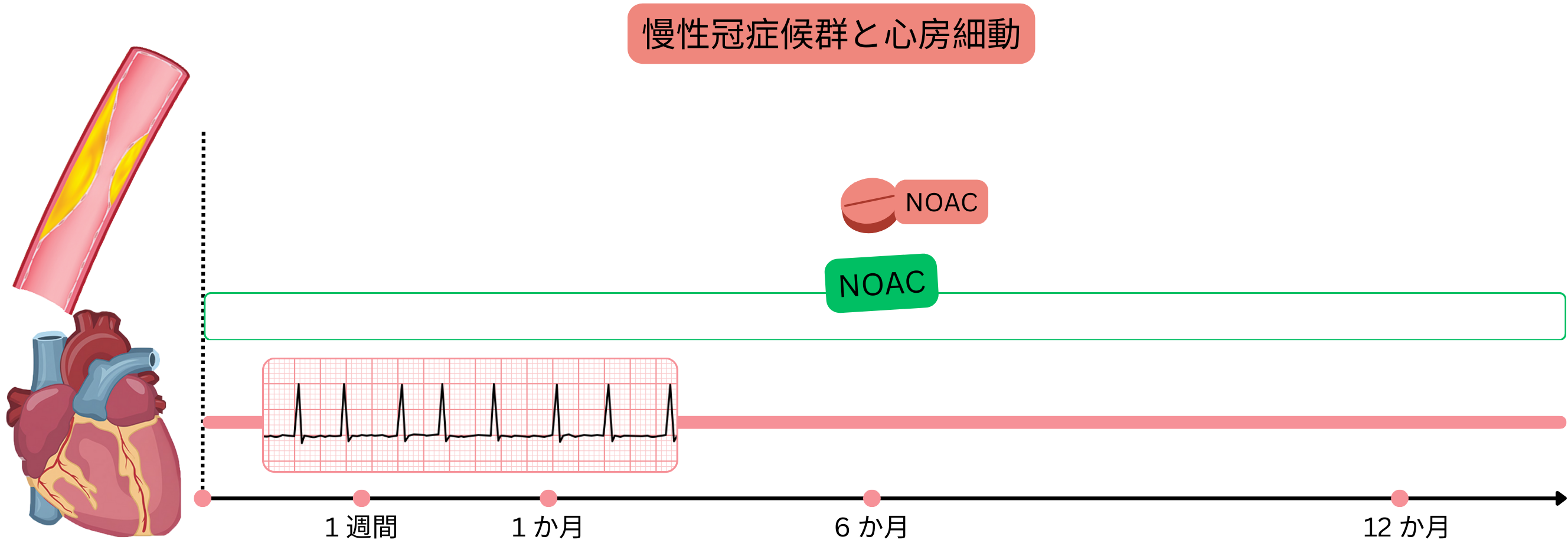
安定CCS
例:心房細動患者(NOAC内服中)がCCSを有し、冠動脈狭窄は非有意(<50%)で、PCI適応はない。
PCI後患者では、ARC-HBR(Academic Research Consortium – High Bleeding Risk)スコアを用いて出血リスクを評価する。
| ARC-HBRスコア(出血リスク) |
|---|
主要基準(1項目で十分)
|
副次基準(≥2項目が必要)
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban). eGFR = estimated Glomerular Filtration Rate. NSAIDs - non-steroidal anti-inflammatory drugs
| ARC-HBRスコアに基づく出血リスクとPCI後抗血栓療法期間短縮 | ||
|---|---|---|
| ARC-HBRスコア | 大出血リスク (PCI後1年以内) |
PCI後抗血栓療法 |
| 陽性 (主要基準≥1または 副次基準≥2) |
4 – 9 % |
|
| 陰性 | 1 – 3 % |
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. DAT - Dual Antithrombotic Therapy. TAT - Triple Antithrombotic Therapy.
これらのガイドラインは非公式であり、いかなる専門的な心臓病学会が発行した正式なガイドラインを代表するものではありません。教育および情報提供のみを目的としています。
