

متلازمة الشريان التاجي المزمنة (CCS)
المتلازمة التاجية الحادة (ACS)
احتشاء عضلة القلب من النمط 1
احتشاء عضلة القلب من النمط 2
إعادة التوعي هي استعادة تدفق الدم عبر تضيّق أو انسداد في شريان تاجي. تشمل طرق إعادة التوعي:
تُعد ACS حالة حادة حرجة قد تُحرِّض نوبة رجفان أذيني أو تُفاقمها.
تبلغ نسبة حدوث الرجفان الأذيني حديث البدء خلال 24 ساعة بعد ACS نحو 2–23 %.
يخضع 10–15 % من مرضى الرجفان الأذيني لإجراء PCI بسبب مرض الشريان التاجي.
قد يسبب الرجفان الأذيني المتسارع (معدل بطيني >100/دقيقة) احتشاء عضلة القلب من النمط 2.
يتطلب المرضى المصابون بـ ACS وAF علاجًا مضادًا للخثار مركبًا:
| العلاج المضاد للخثار (المصطلحات) في المتلازمة التاجية والرجفان الأذيني | |||
|---|---|---|---|
| المصطلح | التعريف | التركيبة الأكثر شيوعًا | الاستخدام الأكثر شيوعًا |
| SAPT (Single Antiplatelet Therapy) |
دواء واحد مضاد للصفيحات | Aspirin | الوقاية في CCS لدى المرضى دون AF |
| DAPT (Dual Antiplatelet Therapy) |
دواءان مضادان للصفيحات | Aspirin + clopidogrel | لمدة 6 أشهر بعد PCI مع دعامة لدى المرضى دون AF |
| DAT (Dual Antithrombotic Therapy) |
علاج مضاد للتخثر + علاج مضاد للصفيحات | NOAC + clopidogrel | لمدة 12 شهرًا بعد PCI لدى مرضى AF |
| TAT (Triple Antithrombotic Therapy) |
علاج مضاد للتخثر + DAPT | NOAC + Aspirin + clopidogrel |
الأسبوع الأول بعد PCI لدى مرضى AF (على NOAC) |
NOAC – Non-vitamin K Oral Anticoagulant, P2Y12 – P2Y12 adenosine diphosphate (ADP) receptor inhibitor (e.g. Clopidogrel, Prasugrel, Ticagrelor), CCS – Chronic coronary syndrome, PCI – Percutaneous coronary intervention (coronary angioplasty with stent)
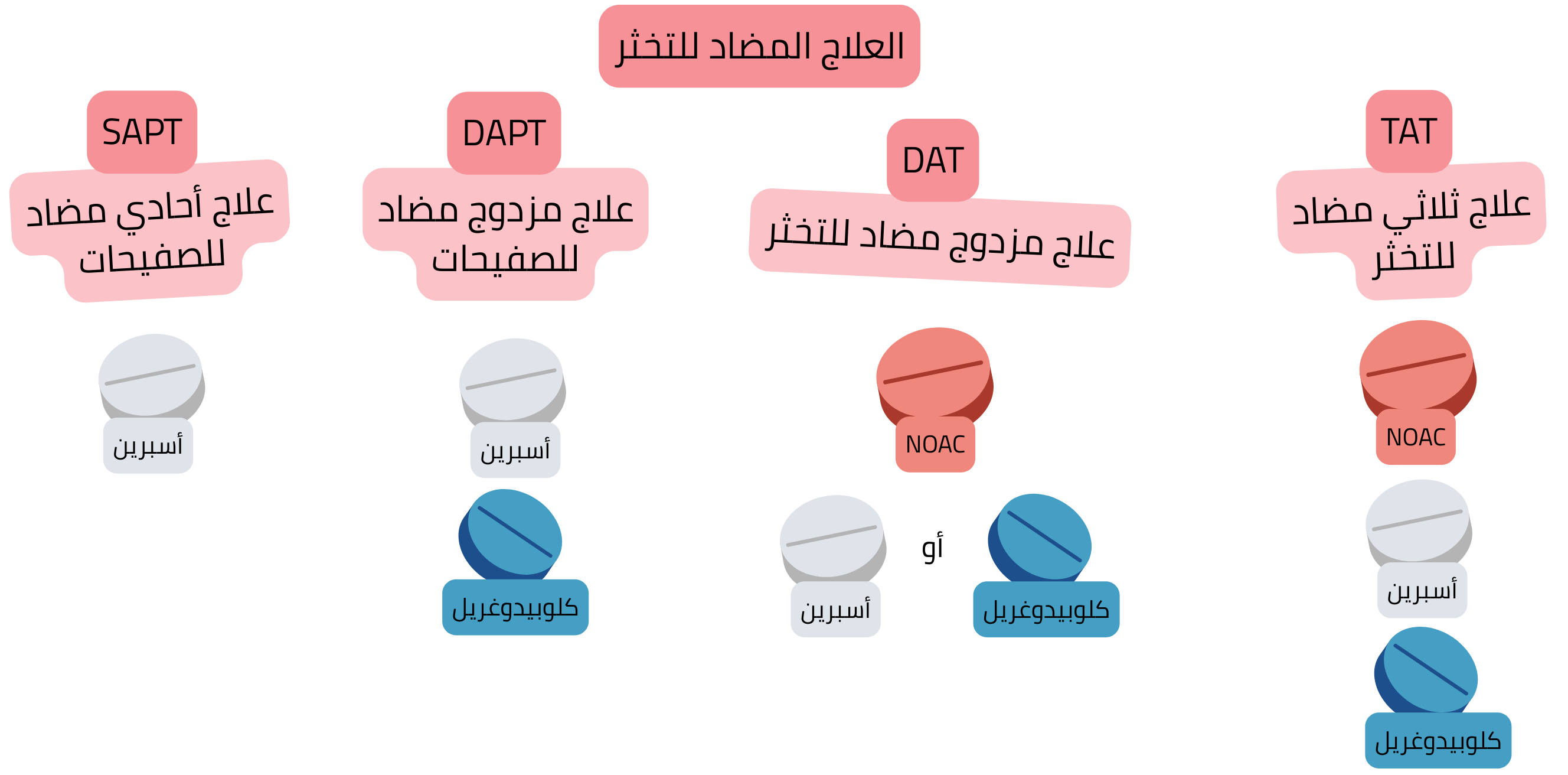
تتطلب ACS بعد PCI علاجًا مضادًا للصفيحات؛ لذلك فإن مرضى AF (إذا كانوا يحتاجون إلى علاج مضاد للتخثر) وACS بعد PCI يحتاجون إلى:
في ACS وAF، تُفضَّل NOAC (وليس warfarin) كعلاج مضاد للتخثر.
مثبط P2Y12 المفضل هو clopidogrel (وليس ticagrelor وprasugrel).
لا يُوصى بمشاركة العلاج المضاد للتخثر (warfarin أو NOAC) مع (ticagrelor أو prasugrel)،
أثناء DAT (warfarin + علاج مضاد للصفيحات)
DAT المفضل لدى مرضى AF بعد ACS أو بعد PCI هو:
أثناء TAT وDAT، يُوصى بمثبطات مضخة البروتون (pantoprazole) للوقاية من النزف الهضمي.
في المرضى المصابين بـ AF وCCS المستقرة، يُوصى بالعلاج المضاد للتخثر وحده (وليس DAT).
| العلاج المضاد للتخثر والعلاج المضاد للصفيحات في الرجفان الأذيني | الفئة |
|---|---|
| في العلاج المركب (OAC + علاج مضاد للصفيحات)، تُفضَّل NOAC (وليس warfarin) كـ OAC بسبب انخفاض خطر النزف وتحسن الوقاية من الخثار الصمي. | I |
| إذا كان المريض يتناول (rivaroxaban + علاجًا مضادًا للصفيحات)، يمكن النظر في خفض جرعة rivaroxaban 20 mg → 15 mg مرة واحدة يوميًا لتقليل خطر النزف. | IIa |
| إذا كان المريض يتناول (dabigatran + علاجًا مضادًا للصفيحات)، يمكن النظر في خفض جرعة dabigatran 150 mg → 110 mg مرتين يوميًا لتقليل خطر النزف. | IIa |
| إذا كان المريض يتناول (warfarin + علاجًا مضادًا للصفيحات)، يمكن النظر في استهداف INR 2–2.5 لتقليل خطر النزف. | IIa |
OAC - Oral anticoagulation, NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
| المتلازمة التاجية الحادة والرجفان الأذيني | الفئة |
|---|---|
في المرضى المصابين بـ AF وACS بعد PCI (خطر إقفاري منخفض)، يُوصى بما يلي:
|
I |
في المرضى المصابين بـ AF وACS بعد PCI (خطر إقفاري مرتفع)، يُوصى بما يلي:
|
IIa |
NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), ACS – Acute coronary syndrome, PCI – Percutaneous coronary intervention
| خطر إقفاري مرتفع بعد التداخل التاجي عبر الجلد (PCI) | |
|---|---|
| سوابق خثار دعامة (على الرغم من علاج مضاد للصفيحات كافٍ) | |
| زرع دعامة في الشريان التاجي الأخير السالك المتبقي | |
| مرض منتشر في الشرايين التاجية (وخاصة لدى مرضى الداء السكري) | |
| مرض كلوي مزمن: كرياتينين ≥133 µmol/L (CrCl <60 ml/min) | |
| زرع ≥3 دعامات | |
| علاج ≥3 آفات تاجية | |
| علاج تفرع بدعامتين | |
| الطول الإجمالي للدعامات >60 mm | |
| علاج CTO (Chronic Total Occlusion) | |
| متلازمة الشريان التاجي المزمنة والرجفان الأذيني | الفئة |
|---|---|
في المرضى المصابين بـ AF وCCS بعد PCI (خطر إقفاري منخفض)، يُوصى بما يلي:
|
I |
في المرضى المصابين بـ AF وCCS بعد PCI (خطر إقفاري مرتفع)، يُوصى بما يلي:
|
IIa |
NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), CCS - Chronic coronary syndrome, PCI – Percutaneous coronary intervention
| مدة العلاج المضاد للصفيحات بعد ACS مع الرجفان الأذيني | الفئة |
|---|---|
| في المرضى المستقرين بعد ACS مع AF، لا يُوصى بالعلاج المضاد للصفيحات بعد أكثر من 12 شهرًا. | III |
ACS – Acute coronary syndrome
| العلاج المضاد للخثار في ACS وCCS والرجفان الأذيني | الفئة |
|---|---|
| تُعد NOAC (وليس warfarin) العلاجَ المضادَ للتخثر المفضل بالمشاركة مع العلاج المضاد للصفيحات. | I |
| تُخفَّض جرعات NOAC وفق معايير خفض الجرعة القياسية الخاصة بـ NOAC. | I |
| أثناء العلاج بـ (warfarin + علاج مضاد للصفيحات)، يمكن النظر في استهداف INR 2–2.5. | IIa |
| أثناء علاج warfarin (دون علاج مضاد للصفيحات)، يُوصى باستهداف INR 2–3. | I |
| مثبط P2Y12 المفضل بالمشاركة مع العلاج المضاد للتخثر هو clopidogrel (وليس ticagrelor أو prasugrel). | IIa |
ACS – Acute coronary syndrome, CCS - Chronic coronary syndrome, NOAC – Non-vitamin K oral anticoagulants (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
جميع المرضى التاليين:
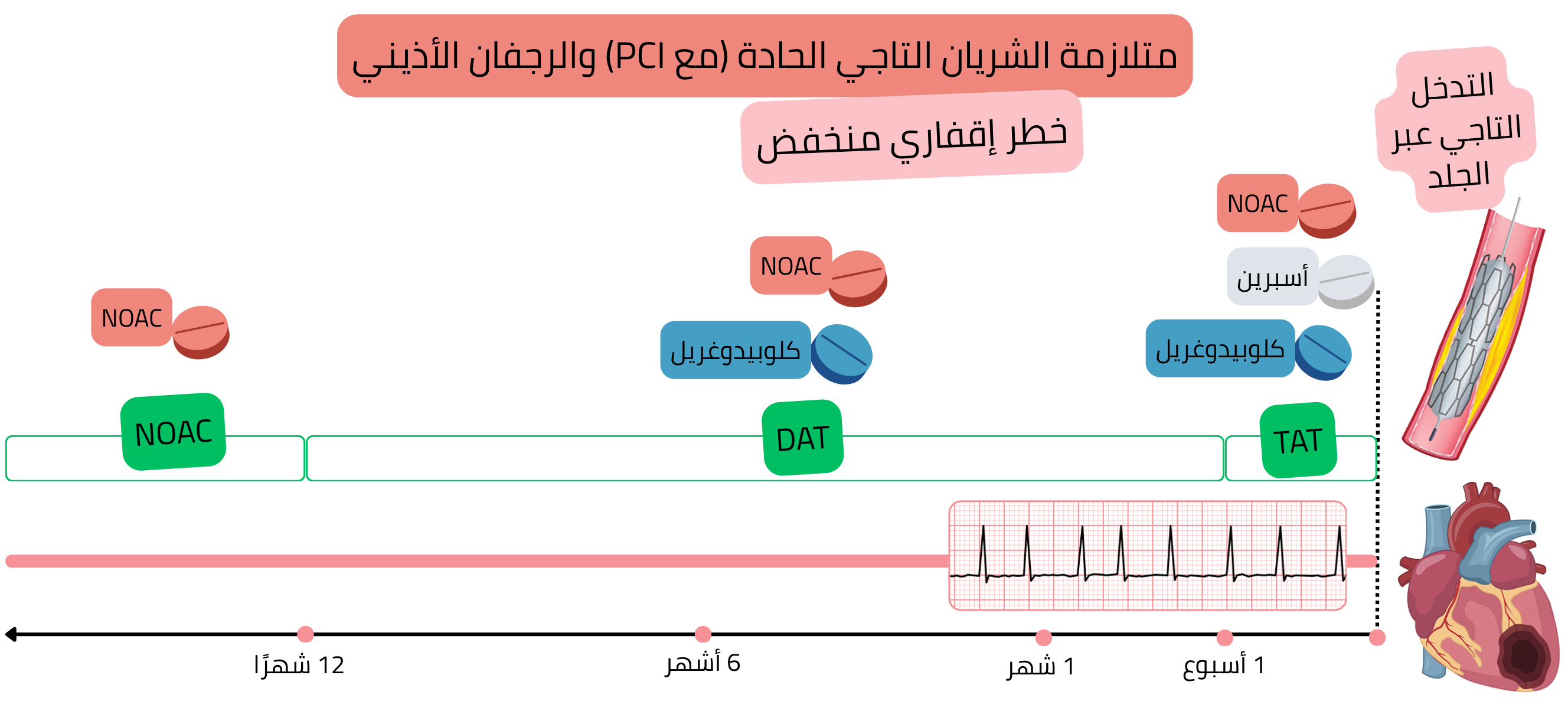
ACS بعد PCI (خطر إقفاري منخفض)
مثال: مريض لديه AF (على NOAC) أُصيب باحتشاء (STEMI أو NSTEMI)، وتم نقله إلى مركز قلبي حيث أُجري PCI مع زرع دعامة واحدة في الشريان المنعطف.
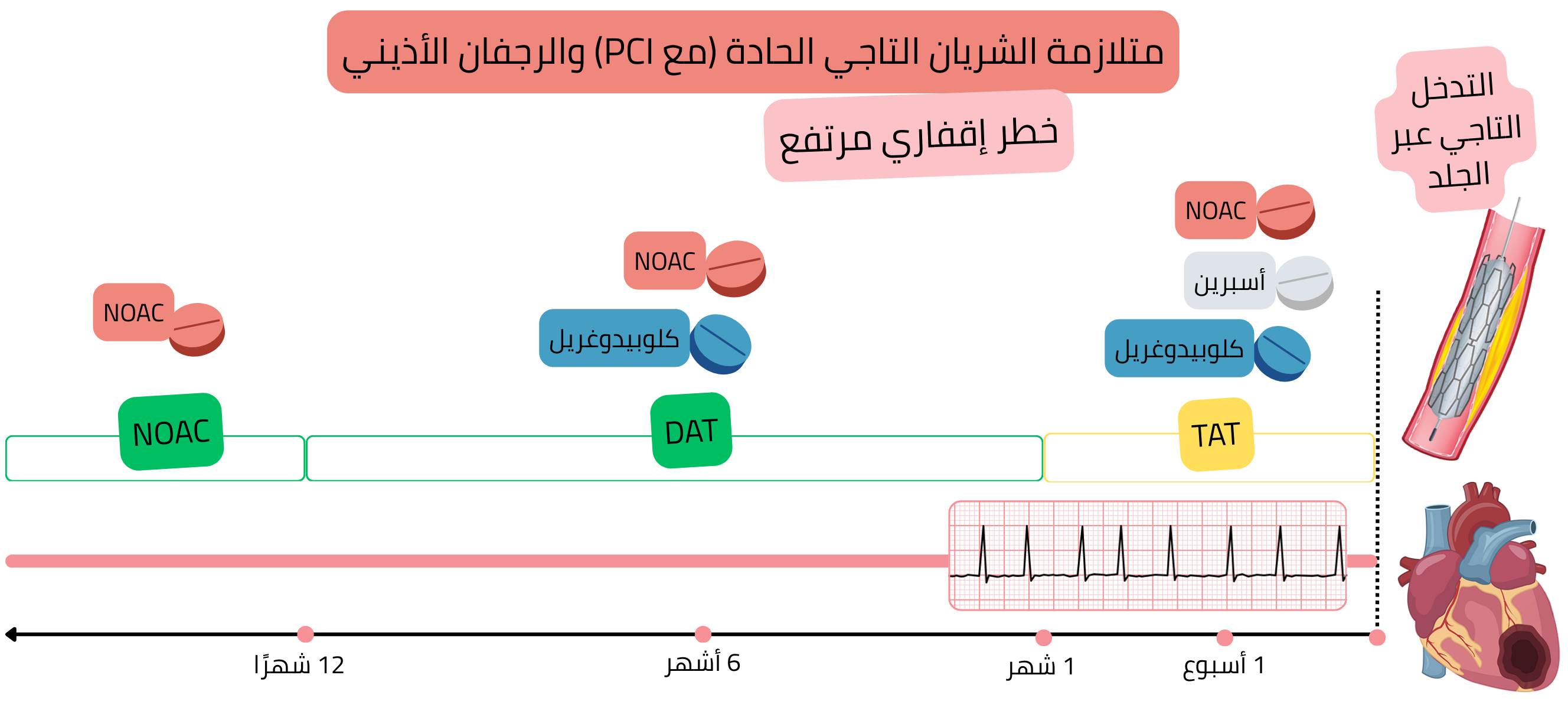
ACS بعد PCI (خطر إقفاري مرتفع)
مثال: مريض لديه AF أُصيب باحتشاء (STEMI أو NSTEMI)، وتم نقله إلى مركز قلبي حيث أُجري PCI مع زرع 3 دعامات.
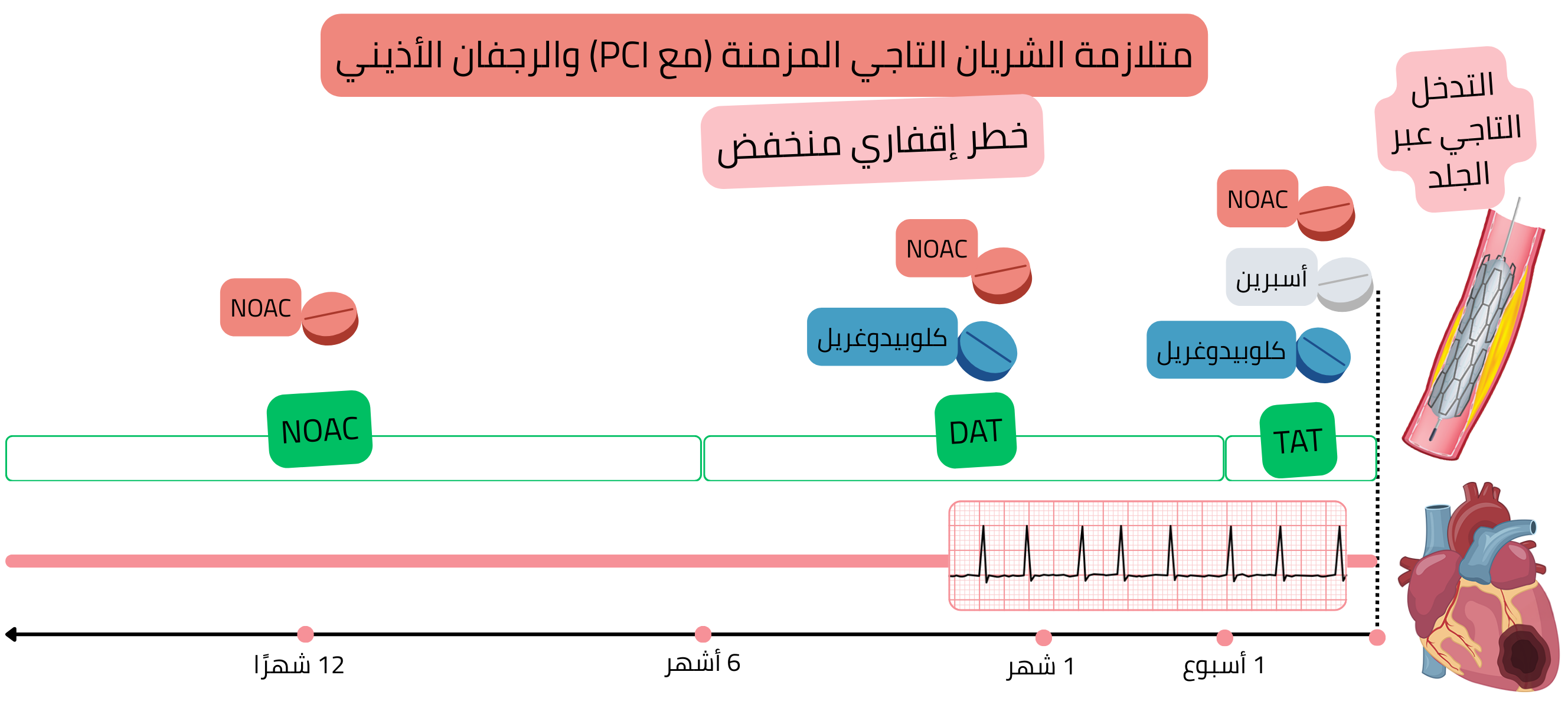
CCS بعد PCI (خطر إقفاري منخفض)
مثال: مريض لديه AF (على NOAC) لديه ذبحة صدرية مستقرة وتضيّق تاجي مهم (>70 %) في تصوير الشرايين التاجية بالتصوير المقطعي المحوسب؛ أُجري PCI مع زرع دعامة واحدة في الشريان التاجي الأيمن.
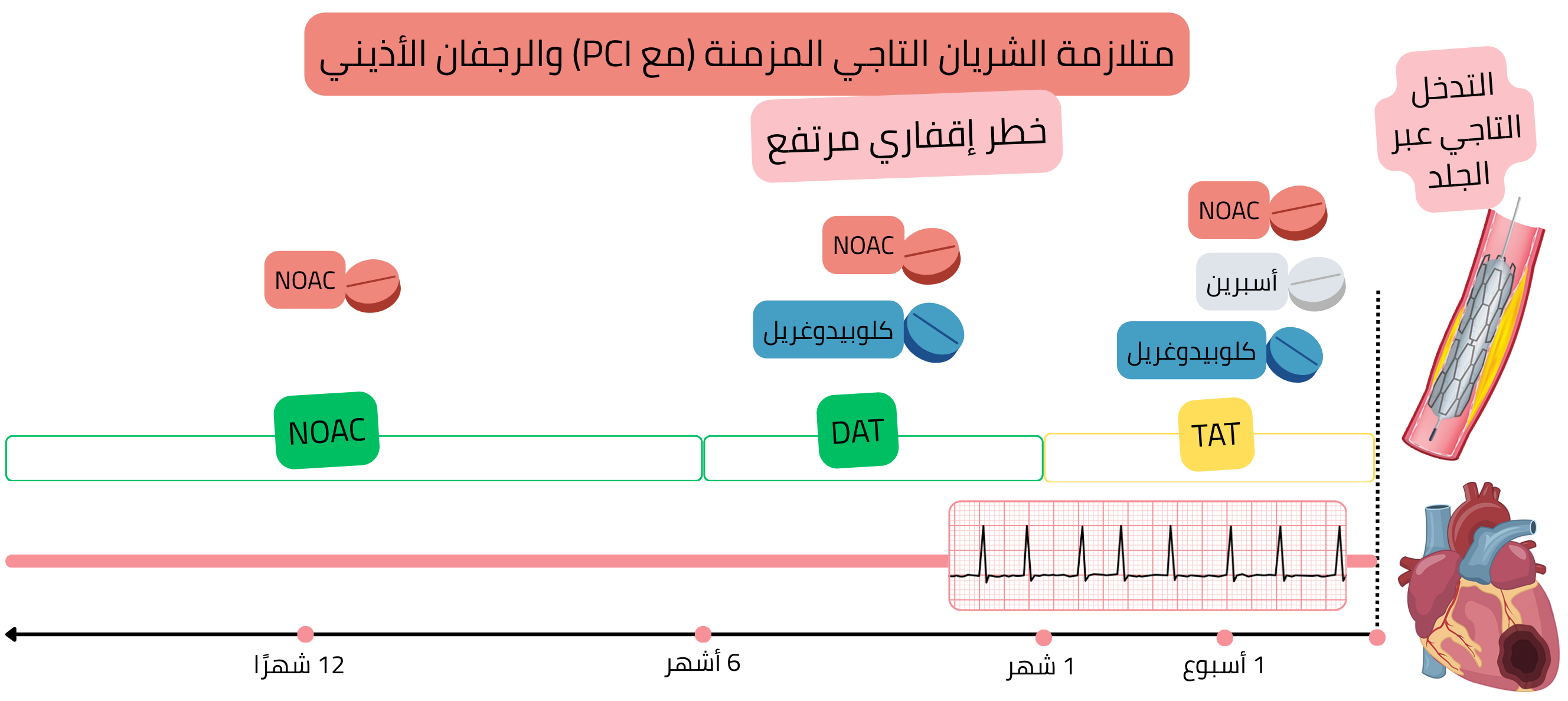
CCS بعد PCI (خطر إقفاري مرتفع)
مثال: مريض لديه AF (على NOAC) لديه ذبحة صدرية مستقرة؛ أظهر تصوير الشرايين التاجية 3 تضيّقات شديدة (>70 %)، وتم زرع 3 دعامات أثناء PCI.
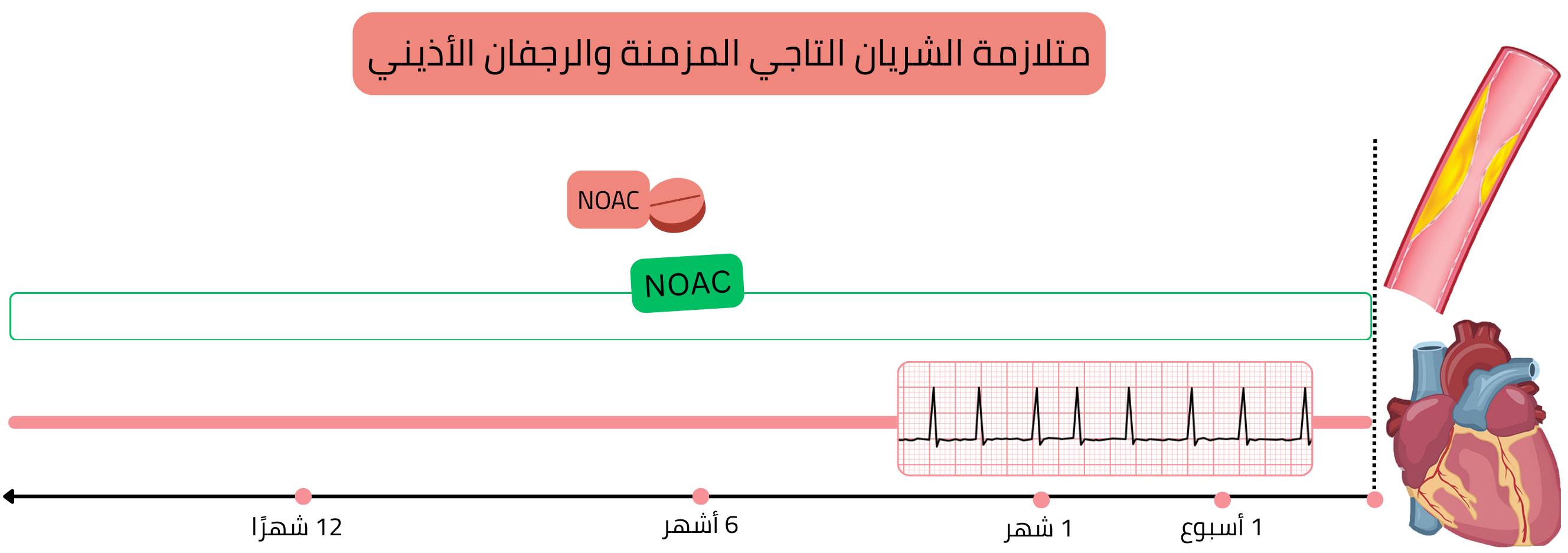
CCS مستقرة
مثال: مريض لديه AF (على NOAC) لديه CCS مع تضيّق تاجي غير مهم (<50 %)، ولا يوجد استطباب لإجراء PCI.
بعد PCI، يُقيَّم خطر النزف باستخدام مقياس ARC-HBR (Academic Research Consortium – High Bleeding Risk).
| درجة ARC-HBR (خطر النزف) |
|---|
المعايير الرئيسية (يكفي معيار واحد)
|
المعايير الثانوية (يلزم ≥2)
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban). eGFR = estimated Glomerular Filtration Rate. NSAIDs - non-steroidal anti-inflammatory drugs
| خطر النزف وفق درجة ARC-HBR وتقصير مدة العلاج المضاد للخثار بعد PCI | ||
|---|---|---|
| درجة ARC-HBR | خطر نزف كبير (خلال سنة واحدة بعد PCI) |
العلاج المضاد للخثار بعد PCI |
| إيجابي (≥ 1 معيار رئيسي أو ≥ 2 معيارين ثانويين) |
4 – 9 % |
|
| سلبي | 1 – 3 % |
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. DAT - Dual Antithrombotic Therapy. TAT - Triple Antithrombotic Therapy.
هذه الإرشادات غير رسمية ولا تمثل إرشادات رسمية صادرة عن أي جمعية مهنية في أمراض القلب. وهي مخصصة لأغراض تعليمية وإعلامية فقط.
