

Chronisches Koronarsyndrom (CCS)
Akutes Koronarsyndrom (ACS)
Myokardinfarkt Typ 1
Myokardinfarkt Typ 2
Revaskularisation ist die Wiederherstellung des Blutflusses über eine Stenose oder Okklusion einer Koronararterie. Methoden der Revaskularisation sind:
ACS ist ein akuter kritischer Zustand, der eine VHF-Episode auslösen oder verschlechtern kann.
Die Inzidenz eines neu auftretenden VHF innerhalb von 24 Stunden nach ACS beträgt 2–23 %.
10–15 % der Patienten mit VHF werden wegen koronarer Herzkrankheit einer PCI unterzogen.
Tachykardes VHF (Kammerfrequenz >100/min) kann einen Myokardinfarkt Typ 2 verursachen.
Patienten mit ACS und VHF benötigen eine kombinierte antithrombotische Therapie:
| Antithrombotische Therapie (Terminologie) beim Koronarsyndrom und Vorhofflimmern | |||
|---|---|---|---|
| Begriff | Definition | Häufigste Kombination | Häufigste Anwendung |
| SAPT (Single Antiplatelet Therapy) |
1 Thrombozytenaggregationshemmer | Aspirin | Prävention bei CCS bei Patienten ohne VHF |
| DAPT (Dual Antiplatelet Therapy) |
2 Thrombozytenaggregationshemmer | Aspirin + Clopidogrel | 6 Monate nach PCI mit Stent bei Patienten ohne VHF |
| DAT (Dual Antithrombotic Therapy) |
Antikoagulation + Thrombozytenaggregationshemmung | NOAK + Clopidogrel | 12 Monate nach PCI bei Patienten mit VHF |
| TAT (Triple Antithrombotic Therapy) |
Antikoagulation + DAPT | NOAK + Aspirin + Clopidogrel |
Erste Woche nach PCI bei Patienten mit VHF (unter NOAK) |
NOAK – Nicht-Vitamin-K-abhängiges orales Antikoagulans, P2Y12 – P2Y12-Adenosindiphosphat(ADP)-Rezeptor-Inhibitor (z. B. Clopidogrel, Prasugrel, Ticagrelor), CCS – Chronisches Koronarsyndrom, PCI – Perkutane Koronarintervention (Koronarangioplastie mit Stent)
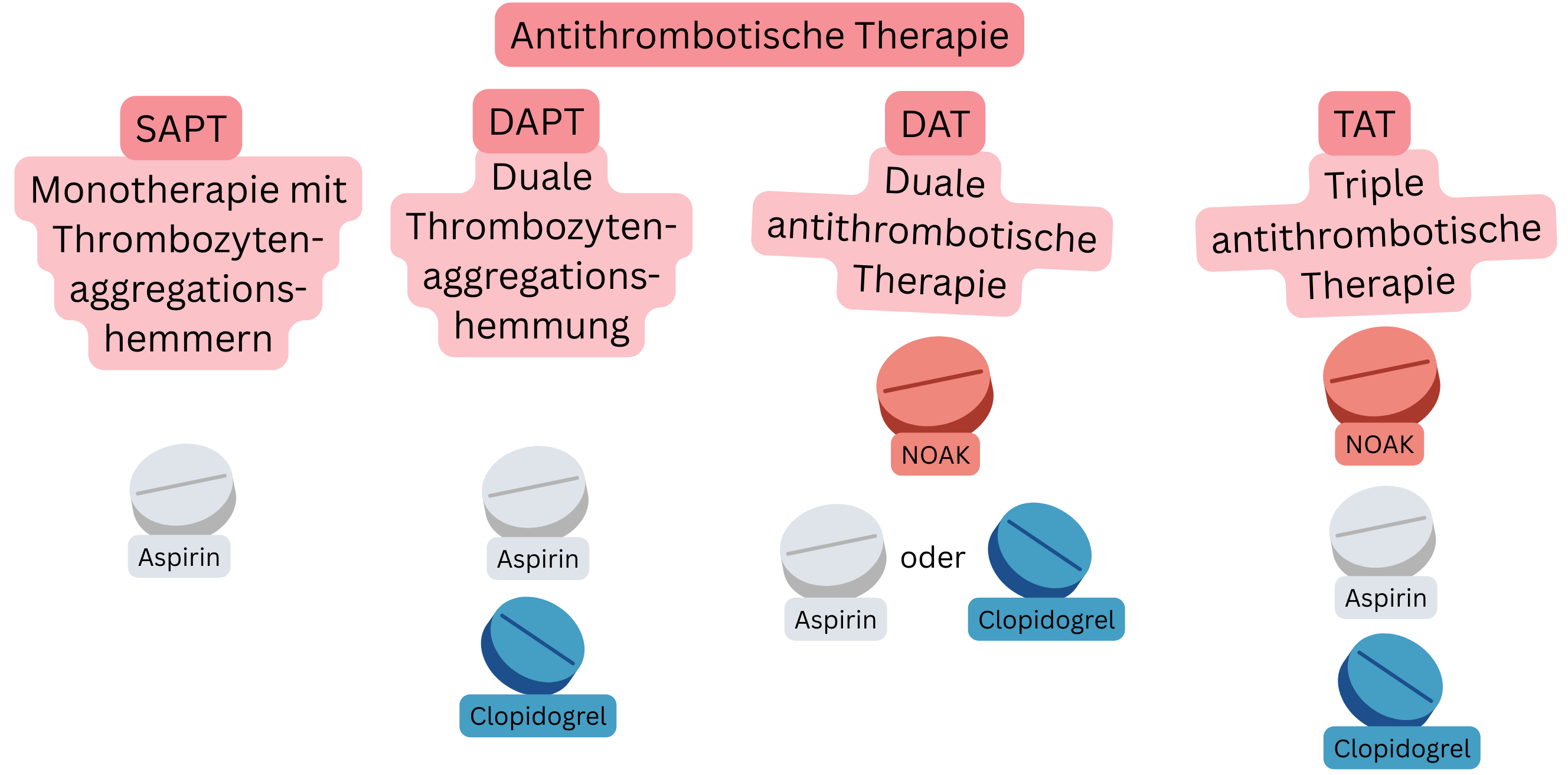
ACS nach PCI erfordert eine Thrombozytenaggregationshemmung; daher benötigen Patienten mit VHF (bei Indikation zur Antikoagulation) und ACS nach PCI:
Bei ACS und VHF werden NOAK (nicht Warfarin) als Antikoagulationstherapie bevorzugt.
Der bevorzugte P2Y12-Inhibitor ist Clopidogrel (nicht Ticagrelor und Prasugrel).
Die Kombination einer Antikoagulation (Warfarin oder NOAK) mit (Ticagrelor oder Prasugrel) wird nicht empfohlen,
Während DAT (Warfarin + Thrombozytenaggregationshemmung)
Bevorzugte DAT bei VHF nach ACS oder nach PCI ist:
Während TAT und DAT werden Protonenpumpenhemmer (Pantoprazol) zur Prävention gastrointestinaler Blutungen empfohlen.
Bei Patienten mit VHF und stabilem CCS wird eine alleinige Antikoagulation empfohlen (nicht DAT).
| Antikoagulation und Thrombozytenaggregationshemmung bei Vorhofflimmern | Klasse |
|---|---|
| Bei Kombinationstherapie (OAK + Thrombozytenaggregationshemmung) werden NOAK (nicht Warfarin) als OAK aufgrund geringerer Blutungsrate und besserer Thromboembolieprävention bevorzugt. | I |
| Wenn der Patient (Rivaroxaban + Thrombozytenaggregationshemmung) erhält, kann zur Reduktion des Blutungsrisikos eine Dosisreduktion von Rivaroxaban 20 mg → 15 mg einmal täglich erwogen werden. | IIa |
| Wenn der Patient (Dabigatran + Thrombozytenaggregationshemmung) erhält, kann zur Reduktion des Blutungsrisikos eine Dosisreduktion von Dabigatran 150 mg → 110 mg zweimal täglich erwogen werden. | IIa |
| Wenn der Patient (Warfarin + Thrombozytenaggregationshemmung) erhält, kann zur Reduktion des Blutungsrisikos ein INR-Zielwert von 2–2,5 erwogen werden. | IIa |
OAK - Orale Antikoagulation, NOAK – Nicht-Vitamin-K-abhängige orale Antikoagulanzien (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
| Akutes Koronarsyndrom und Vorhofflimmern | Klasse |
|---|---|
Bei Patienten mit VHF und ACS nach PCI (niedriges ischämisches Risiko) wird Folgendes empfohlen:
|
I |
Bei Patienten mit VHF und ACS nach PCI (hohes ischämisches Risiko) wird Folgendes empfohlen:
|
IIa |
NOAK – Nicht-Vitamin-K-abhängige orale Antikoagulanzien (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), ACS – Akutes Koronarsyndrom, PCI – Perkutane Koronarintervention
| Hohes ischämisches Risiko nach perkutaner Koronarintervention (PCI) | |
|---|---|
| Stentthrombose in der Anamnese (trotz adäquater Thrombozytenaggregationshemmung) | |
| Stentimplantation in der letzten verbleibenden offenen Koronararterie | |
| Diffuse koronare Herzkrankheit (insbesondere bei Patienten mit Diabetes mellitus) | |
| Chronische Nierenerkrankung Kreatinin ≥133 µmol/L (CrCl <60 ml/min) | |
| Implantation von ≥3 Stents | |
| Behandlung von ≥3 Koronarläsionen | |
| Behandlung einer Bifurkation mit 2 Stents | |
| Gesamte Stentlänge >60 mm | |
| Behandlung einer CTO (Chronic Total Occlusion) | |
| Chronisches Koronarsyndrom und Vorhofflimmern | Klasse |
|---|---|
Bei Patienten mit VHF und CCS nach PCI (niedriges ischämisches Risiko) wird Folgendes empfohlen:
|
I |
Bei Patienten mit VHF und CCS nach PCI (hohes ischämisches Risiko) wird Folgendes empfohlen:
|
IIa |
NOAK – Nicht-Vitamin-K-abhängige orale Antikoagulanzien (Dabigatran, Rivaroxaban, Apixaban, Edoxaban), CCS - Chronisches Koronarsyndrom, PCI – Perkutane Koronarintervention
| Dauer der Thrombozytenaggregationshemmung nach ACS bei Vorhofflimmern | Klasse |
|---|---|
| Bei stabilen Patienten nach ACS mit VHF wird eine Thrombozytenaggregationshemmung über 12 Monate hinaus nicht empfohlen. | III |
ACS – Akutes Koronarsyndrom
| Antithrombotische Therapie bei ACS, CCS und Vorhofflimmern | Klasse |
|---|---|
| NOAK (nicht Warfarin) sind die bevorzugte Antikoagulation in Kombination mit einer Thrombozytenaggregationshemmung. | I |
| NOAK-Dosen werden gemäß den standardisierten Kriterien zur NOAK-Dosisreduktion reduziert. | I |
| Während der Therapie mit (Warfarin + Thrombozytenaggregationshemmung) kann ein INR-Zielwert von 2–2,5 erwogen werden. | IIa |
| Während der Warfarintherapie (ohne Thrombozytenaggregationshemmung) wird ein INR-Zielwert von 2–3 empfohlen. | I |
| Der bevorzugte P2Y12-Inhibitor in Kombination mit einer Antikoagulation ist Clopidogrel (nicht Ticagrelor oder Prasugrel). | IIa |
ACS – Akutes Koronarsyndrom, CCS - Chronisches Koronarsyndrom, NOAK – Nicht-Vitamin-K-abhängige orale Antikoagulanzien (Dabigatran, Rivaroxaban, Apixaban, Edoxaban)
Alle folgenden Patienten:
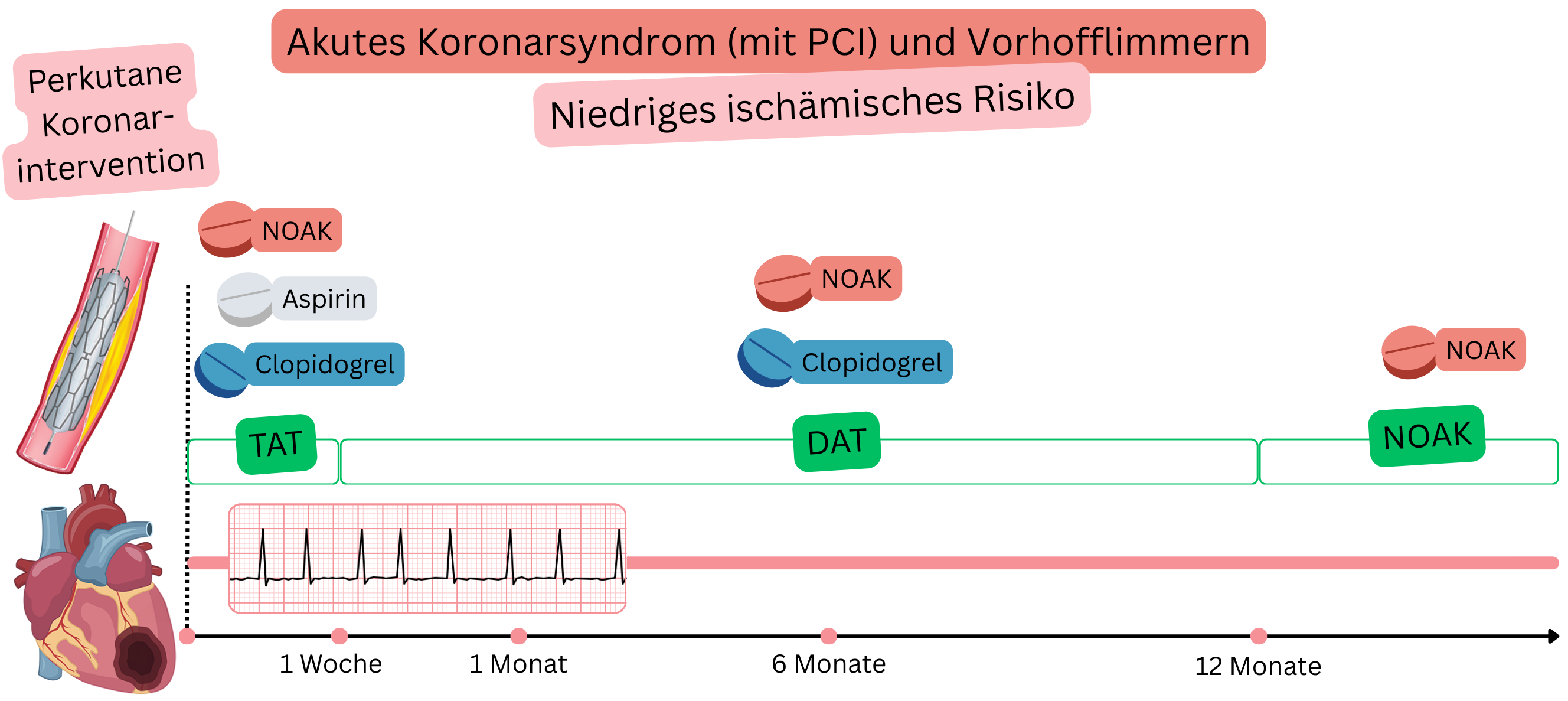
ACS nach PCI (niedriges ischämisches Risiko)
Beispiel: Ein Patient mit VHF (unter NOAK) erlitt einen Infarkt (STEMI oder NSTEMI), wurde in ein Herzzentrum verlegt, wo eine PCI mit Implantation von 1 Stent in die A. circumflexa durchgeführt wurde.
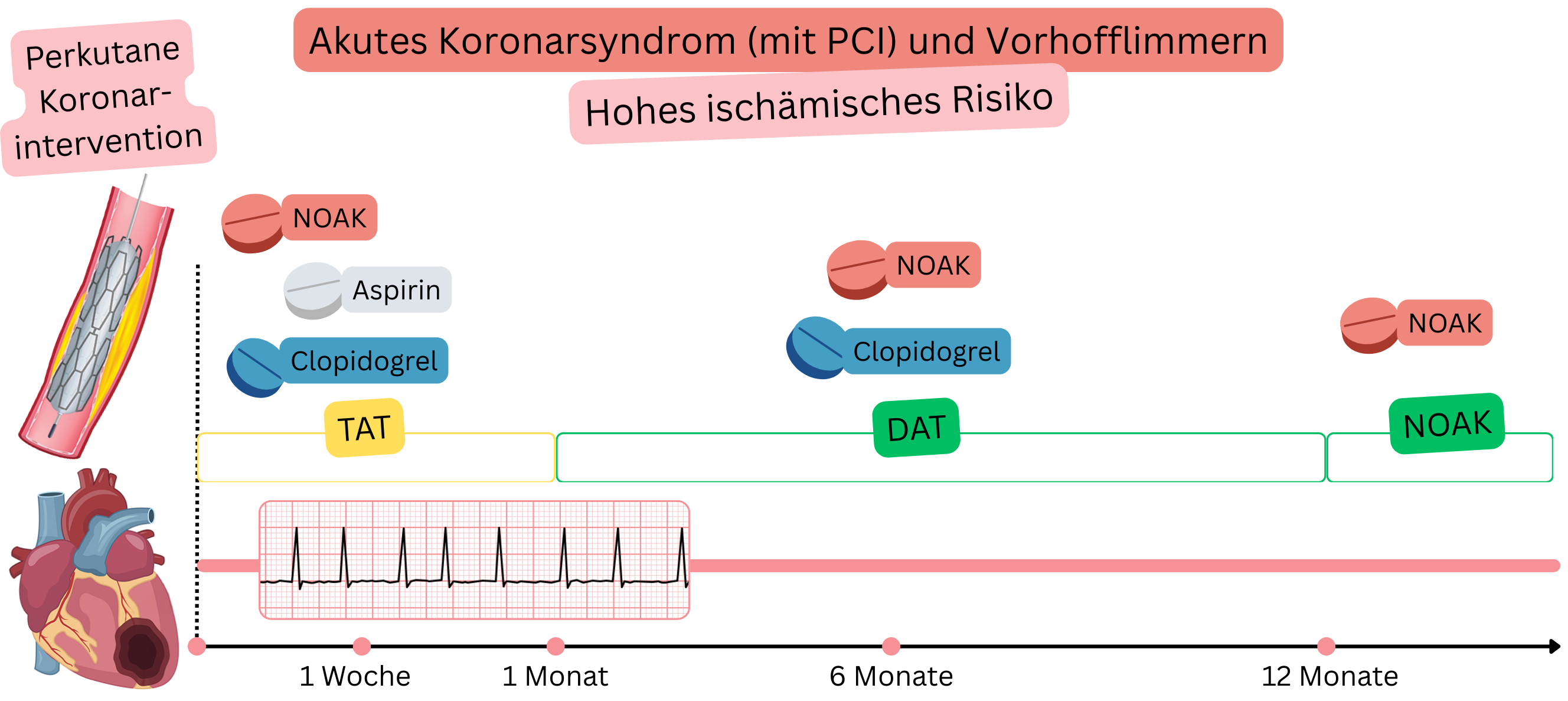
ACS nach PCI (hohes ischämisches Risiko)
Beispiel: Ein Patient mit VHF erlitt einen Infarkt (STEMI oder NSTEMI), wurde in ein Herzzentrum verlegt, wo eine PCI mit Implantation von 3 Stents durchgeführt wurde.
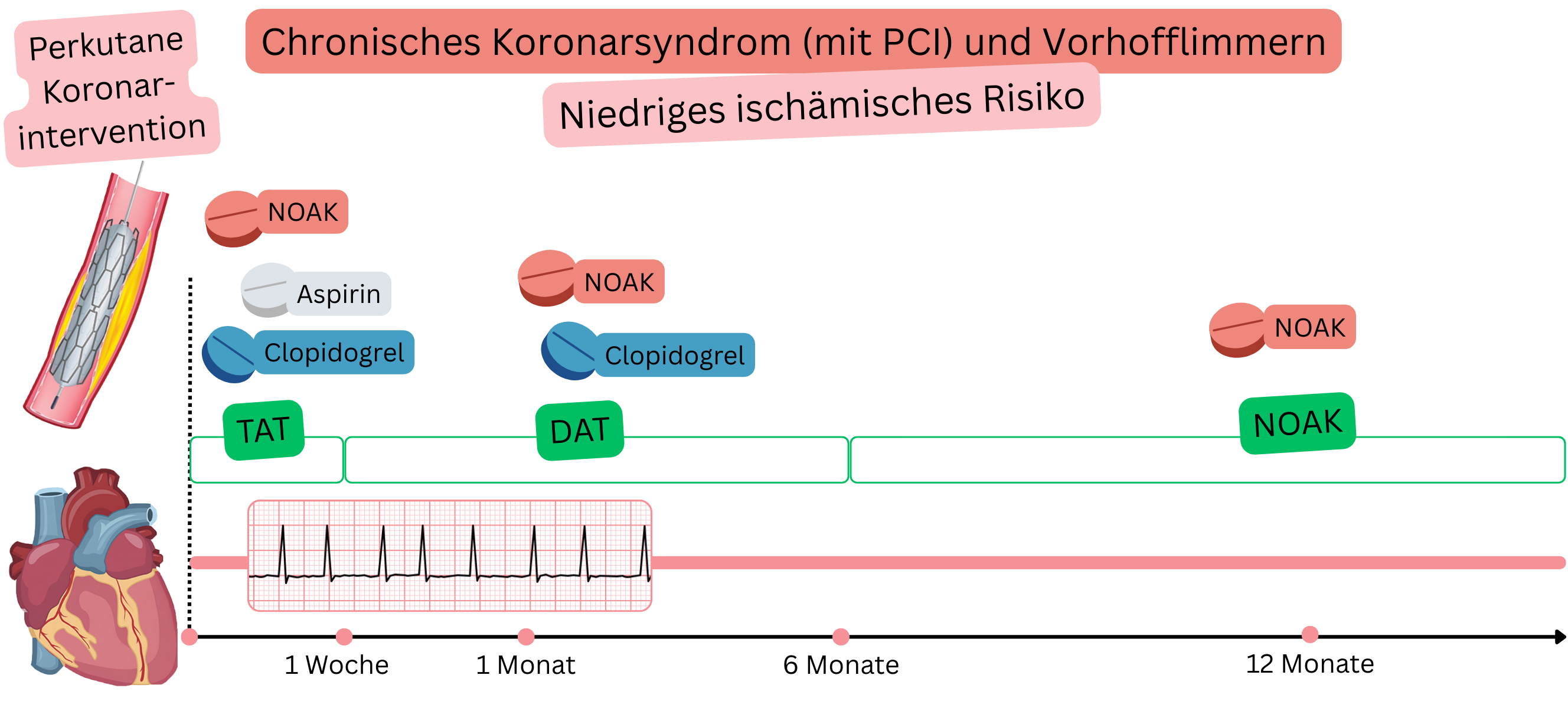
CCS nach PCI (niedriges ischämisches Risiko)
Beispiel: Ein Patient mit VHF (unter NOAK) hatte stabile Angina pectoris und eine signifikante koronare Stenose (>70 %) in der CT-Koronarangiographie; eine PCI wurde mit Implantation von 1 Stent in die rechte Koronararterie durchgeführt.
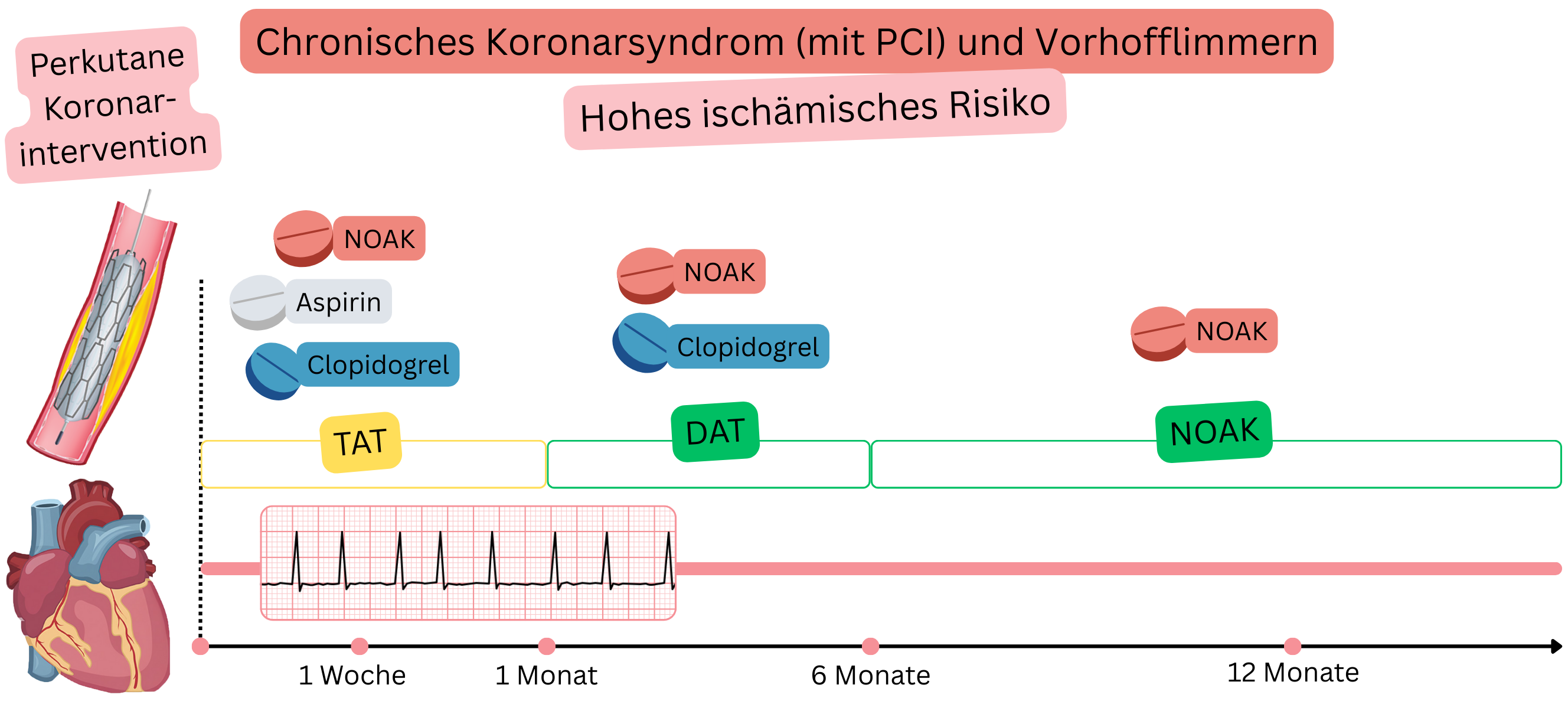
CCS nach PCI (hohes ischämisches Risiko)
Beispiel: Ein Patient mit VHF (unter NOAK) hatte stabile Angina pectoris; die Koronarangiographie zeigte 3 schwere Stenosen (>70 %), und während der PCI wurden 3 Stents implantiert.
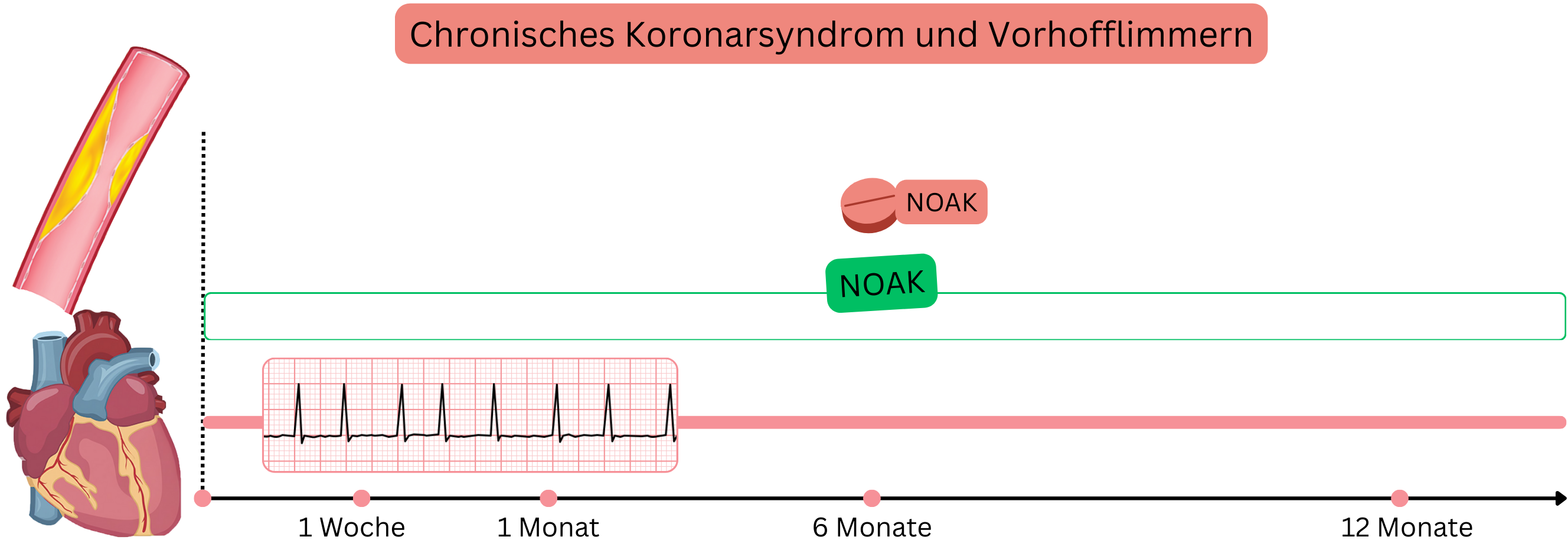
Stabiles CCS
Beispiel: Ein Patient mit VHF (unter NOAK) hat CCS mit nicht-signifikanter koronarer Stenose (<50 %), keine Indikation zur PCI.
Bei Patienten nach PCI wird das Blutungsrisiko mit dem ARC-HBR-Score (Academic Research Consortium – High Bleeding Risk) beurteilt.
| ARC-HBR-Score (Blutungsrisiko) |
|---|
Hauptkriterien (1 ist ausreichend)
|
Nebenkriterien (≥2 erforderlich)
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Perkutane Koronarintervention. NOAK – Nicht-Vitamin-K-abhängige orale Antikoagulanzien (Dabigatran, Rivaroxaban, Apixaban, Edoxaban). eGFR = geschätzte glomeruläre Filtrationsrate. NSAR - nichtsteroidale Antirheumatika
| Blutungsrisiko gemäß ARC-HBR-Score und Verkürzung der antithrombotischen Therapie nach PCI | ||
|---|---|---|
| ARC-HBR-Score | Risiko schwerer Blutungen (innerhalb von 1 Jahr nach PCI) |
Antithrombotische Therapie nach PCI |
| Positiv (≥ 1 Hauptkriterium oder ≥ 2 Nebenkriterien) |
4 – 9 % |
|
| Negativ | 1 – 3 % |
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Perkutane Koronarintervention. DAT - Duale antithrombotische Therapie. TAT - Triple antithrombotische Therapie.
Diese Leitlinien sind inoffiziell und stellen keine offiziellen Leitlinien dar, die von einer kardiologischen Fachgesellschaft herausgegeben wurden. Sie dienen ausschließlich zu Bildungs- und Informationszwecken.
