

Sindrome coronarica cronica (CCS)

Sindrome coronarica acuta (ACS)
Infarto miocardico di tipo 1
Infarto miocardico di tipo 2
La rivascolarizzazione è il ripristino del flusso ematico attraverso una stenosi o un’occlusione di un’arteria coronaria. I metodi di rivascolarizzazione includono:
La ACS è una condizione critica acuta che può scatenare o peggiorare un episodio di FA.
L’incidenza di FA di nuova insorgenza entro 24 ore dopo ACS è 2–23 %.
Il 10–15 % dei pazienti con FA viene sottoposto a PCI per coronaropatia.
La FA tachicardica (frequenza ventricolare >100/min) può causare infarto miocardico di tipo 2.
I pazienti con ACS e FA richiedono terapia antitrombotica combinata:
| Terapia antitrombotica (Terminologia) nella sindrome coronarica e nella fibrillazione atriale | |||
|---|---|---|---|
| Termine | Definizione | Combinazione più comune | Impiego più comune |
| SAPT (Terapia antiaggregante singola) |
1 farmaco antiaggregante | Aspirina | Prevenzione nella CCS in pazienti senza FA |
| DAPT (Doppia terapia antiaggregante) |
2 farmaci antiaggreganti | Aspirina + clopidogrel | 6 mesi dopo PCI con stent in pazienti senza FA |
| DAT (Doppia terapia antitrombotica) |
Terapia anticoagulante + terapia antiaggregante | NOAC + clopidogrel | 12 mesi dopo PCI in pazienti con FA |
| TAT (Tripla terapia antitrombotica) |
Terapia anticoagulante + DAPT | NOAC + Aspirina + clopidogrel |
Prima settimana dopo PCI in pazienti con FA (in terapia con NOAC) |
NOAC – anticoagulante orale non antagonista della vitamina K, P2Y12 – inibitore del recettore P2Y12 dell’adenosina difosfato (ADP) (ad es. clopidogrel, prasugrel, ticagrelor), CCS – sindrome coronarica cronica, PCI – intervento coronarico percutaneo (angioplastica coronarica con stent)

La ACS dopo PCI richiede terapia antiaggregante; pertanto, i pazienti con FA (se necessitano di terapia anticoagulante) e ACS dopo PCI richiedono:
Nella ACS e nella FA, i NOAC (non warfarin) sono preferiti come terapia anticoagulante.
L’inibitore P2Y12 preferito è il clopidogrel (non ticagrelor e prasugrel).
La combinazione di terapia anticoagulante (warfarin o NOAC) con (ticagrelor o prasugrel) non è raccomandata,
Durante DAT (warfarin + terapia antiaggregante)
La DAT preferita nella FA dopo ACS o dopo PCI è:
Durante TAT e DAT, gli inibitori di pompa protonica (pantoprazolo) sono raccomandati per la prevenzione del sanguinamento gastrointestinale.
Nei pazienti con FA e CCS stabile, è raccomandata la sola terapia anticoagulante (non DAT).
| Anticoagulazione e terapia antiaggregante nella fibrillazione atriale | Classe |
|---|---|
| Nella terapia di combinazione (OAC + terapia antiaggregante), i NOAC (non warfarin) sono preferiti come OAC per il minor rischio di sanguinamento e la migliore prevenzione del tromboembolismo. | I |
| Se il paziente assume (rivaroxaban + terapia antiaggregante), la riduzione della dose di rivaroxaban 20 mg → 15 mg una volta al giorno può essere presa in considerazione per ridurre il rischio di sanguinamento. | IIa |
| Se il paziente assume (dabigatran + terapia antiaggregante), la riduzione della dose di dabigatran 150 mg → 110 mg due volte al giorno può essere presa in considerazione per ridurre il rischio di sanguinamento. | IIa |
| Se il paziente assume (warfarin + terapia antiaggregante), un INR target 2–2,5 può essere preso in considerazione per ridurre il rischio di sanguinamento. | IIa |
OAC - anticoagulazione orale, NOAC – anticoagulante orale non antagonista della vitamina K (dabigatran, rivaroxaban, apixaban, edoxaban)
| Sindrome coronarica acuta e fibrillazione atriale | Classe |
|---|---|
Nei pazienti con FA e ACS dopo PCI (basso rischio ischemico), è raccomandato quanto segue:
|
I |
Nei pazienti con FA e ACS dopo PCI (alto rischio ischemico), è raccomandato quanto segue:
|
IIa |
NOAC – anticoagulanti orali non antagonisti della vitamina K (dabigatran, rivaroxaban, apixaban, edoxaban), ACS – sindrome coronarica acuta, PCI – intervento coronarico percutaneo
| Alto rischio ischemico dopo intervento coronarico percutaneo (PCI) | |
|---|---|
| Anamnesi di trombosi dello stent (nonostante adeguata terapia antiaggregante) | |
| Impianto di stent nell’ultima arteria coronaria pervia residua | |
| Coronaropatia diffusa (in particolare nei pazienti con diabete mellito) | |
| Malattia renale cronica creatinina ≥133 µmol/L (CrCl <60 ml/min) | |
| Impianto di ≥3 stent | |
| Trattamento di ≥3 lesioni coronariche | |
| Trattamento di una biforcazione con 2 stent | |
| Lunghezza totale degli stent >60 mm | |
| Trattamento di CTO (occlusione totale cronica) | |
| Sindrome coronarica cronica e fibrillazione atriale | Classe |
|---|---|
Nei pazienti con FA e CCS dopo PCI (basso rischio ischemico), è raccomandato quanto segue:
|
I |
Nei pazienti con FA e CCS dopo PCI (alto rischio ischemico), è raccomandato quanto segue:
|
IIa |
NOAC – anticoagulanti orali non antagonisti della vitamina K (dabigatran, rivaroxaban, apixaban, edoxaban), CCS - sindrome coronarica cronica, PCI – intervento coronarico percutaneo
| Durata della terapia antiaggregante dopo ACS con fibrillazione atriale | Classe |
|---|---|
| Nei pazienti stabili dopo ACS con FA, la terapia antiaggregante non è raccomandata oltre 12 mesi. | III |
ACS – sindrome coronarica acuta
| Terapia antitrombotica nella ACS, CCS e fibrillazione atriale | Classe |
|---|---|
| I NOAC (non warfarin) sono la terapia anticoagulante preferita in combinazione con terapia antiaggregante. | I |
| Le dosi dei NOAC vengono ridotte secondo i criteri standard di riduzione della dose dei NOAC. | I |
| Durante il trattamento con (warfarin + terapia antiaggregante), un INR target 2–2,5 può essere preso in considerazione. | IIa |
| Durante la terapia con warfarin (senza terapia antiaggregante), è raccomandato un INR target 2–3. | I |
| L’inibitore P2Y12 preferito in combinazione con terapia anticoagulante è il clopidogrel (non ticagrelor o prasugrel). | IIa |
ACS – sindrome coronarica acuta, CCS - sindrome coronarica cronica, NOAC – anticoagulanti orali non antagonisti della vitamina K (dabigatran, rivaroxaban, apixaban, edoxaban)
Tutti i seguenti pazienti:

ACS dopo PCI (Basso rischio ischemico)
Esempio: un paziente con FA (in terapia con NOAC) ha avuto un infarto (STEMI o NSTEMI), è stato trasferito in un centro cardiologico dove è stata eseguita una PCI con impianto di 1 stent nell’arteria circonflessa.
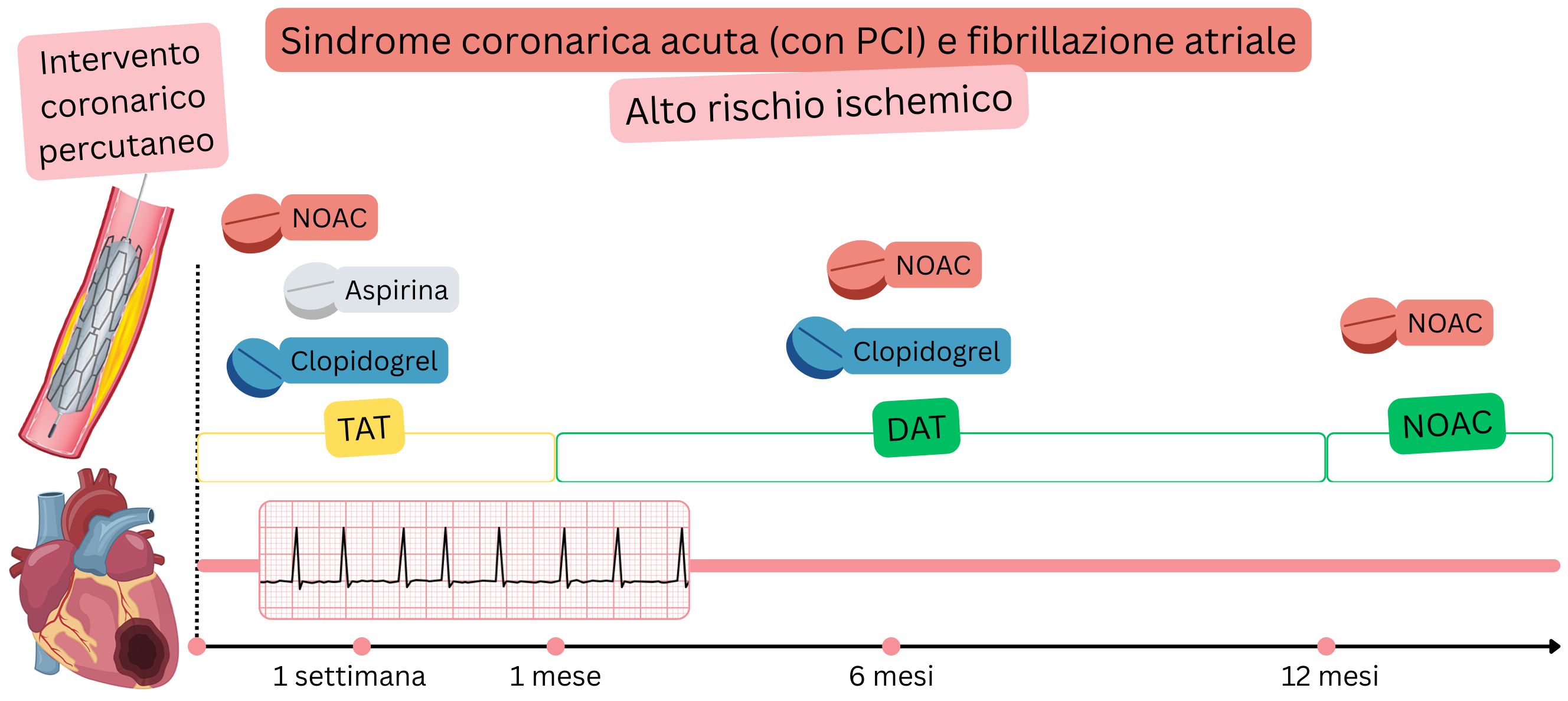
ACS dopo PCI (Alto rischio ischemico)
Esempio: un paziente con FA ha avuto un infarto (STEMI o NSTEMI), è stato trasferito in un centro cardiologico dove è stata eseguita una PCI con impianto di 3 stent.

CCS dopo PCI (Basso rischio ischemico)
Esempio: un paziente con FA (in terapia con NOAC) ha angina pectoris stabile e stenosi coronarica significativa (>70 %) all’angiografia coronarica TC; è stata eseguita una PCI con impianto di 1 stent nella coronaria destra.

CCS dopo PCI (Alto rischio ischemico)
Esempio: un paziente con FA (in terapia con NOAC) ha angina pectoris stabile; la coronarografia ha mostrato 3 stenosi severe (>70 %), e durante la PCI sono stati impiantati 3 stent.

CCS stabile
Esempio: un paziente con FA (in terapia con NOAC) ha CCS con stenosi coronarica non significativa (<50 %), non indicata a PCI.
Nei pazienti dopo PCI, il rischio emorragico viene valutato utilizzando lo score ARC-HBR (Academic Research Consortium – High Bleeding Risk).
| Score ARC-HBR (Rischio emorragico) |
|---|
Criteri maggiori (1 è sufficiente)
|
Criteri minori (richiesti ≥2)
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. NOAC – Non-vitamin K Oral Anticoagulant (Dabigatran, Rivaroxaban, Apixaban, Edoxaban). eGFR = estimated Glomerular Filtration Rate. NSAIDs - non-steroidal anti-inflammatory drugs
| Rischio emorragico secondo lo score ARC-HBR e accorciamento della terapia antitrombotica dopo PCI | ||
|---|---|---|
| Score ARC-HBR | Rischio di sanguinamento maggiore (entro 1 anno dopo PCI) |
Terapia antitrombotica dopo PCI |
| Positivo (≥ 1 criterio maggiore o ≥ 2 criteri minori) |
4 – 9 % |
|
| Negativo | 1 – 3 % |
|
ARC-HBR - Academic Research Consortium – High Bleeding Risk. PCI - Percutaneous coronary intervention. DAT - Dual Antithrombotic Therapy. TAT - Triple Antithrombotic Therapy.
Queste linee guida sono non ufficiali e non rappresentano linee guida formali emesse da alcuna società professionale di cardiologia. Sono destinate esclusivamente a scopi educativi e informativi.
