

Ремоделирование предсердий является следствием предсердной кардиомиопатии,
В ремоделированных предсердиях формируются электрические изменения, создающие субстрат для фибрилляции предсердий (ФП).
Электрические изменения преимущественно возникают в зонах перехода одной анатомической структуры в другую:
Для инициации и поддержания эпизода ФП необходимы два компонента:
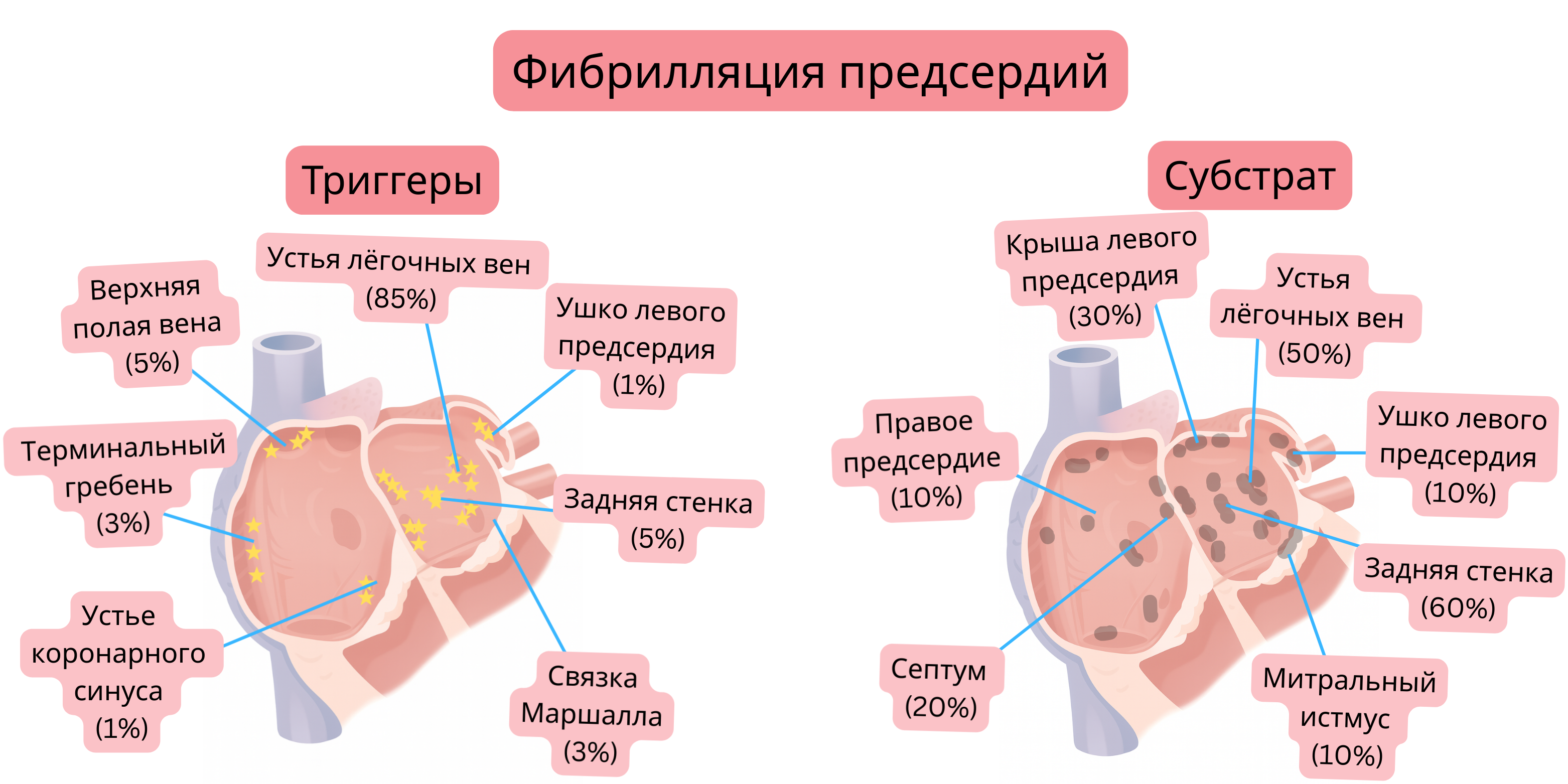
Триггер
Субстрат
Инициация и длительность эпизода ФП зависят от сложного взаимодействия триггера, субстрата и вегетативной модуляции.
Какая именно предсердная экстрасистола или сальва активирует субстрат и как долго будет продолжаться эпизод ФП, крайне вариабельно. Это зависит главным образом от:
При пароксизмальной ФП преобладает триггер
При персистирующей ФП преобладает субстрат
Триггер и субстрат
ФП начинается как пароксизмальная; эпизоды ФП обычно самостоятельно прекращаются в течение 24 часов.
В 90% случаев пароксизмальной ФП триггер (обычно также субстрат) локализован в области устьев легочных вен.
| Триггеры фибрилляции предсердий (локализация) | ||
|---|---|---|
| Анатомическая область | Основная анатомия | Частота (%) |
| Устья легочных вен | Миокардиальные муфты, распространяющиеся на 1–4 см вглубь легочных вен (особенно верхних легочных вен) | 85–90 % |
| Задняя стенка левого предсердия | Задняя стенка левого предсердия и антрумы легочных вен имеют общее эмбриологическое происхождение. Эта ткань обладает иными электрофизиологическими свойствами по сравнению с остальным миокардом предсердий. | 5–10 % |
| Верхняя полая вена | Миокардиальные муфты в области перехода правого предсердия в верхнюю полую вену | 2–5 % |
| Криста терминалис | Гребень между гладкой и трабекулярной частями правого предсердия | 1–3 % |
| Связка Маршалла | Остаток эмбриональной левой верхней полой вены; эпикардиальный тракт, соединяющий коронарный синус с областью левых легочных вен. | 1–3 % |
| Устье коронарного синуса | Миокардиальные муфты в зоне перехода коронарного синуса в правое предсердие. | 1–3 % |
| Ушко левого предсердия | Небольшое выпячивание, расположенное антеролатерально на левом предсердии. Нормальный объем ушка 5–10 мл; при ФП — 10–20 мл. | 1–3 % |
В 90% случаев пароксизмальной ФП триггер, часто в сочетании с субстратом, локализован в области устьев легочных вен.
| Триггеры в легочных венах при фибрилляции предсердий (локализация) | ||
|---|---|---|
| Легочная вена | Частота | Примечание |
| Левая верхняя | 45–50 % | Наиболее частый и наиболее агрессивный источник триггера. Часто имеет общее устье (carina) с левой нижней легочной веной. |
| Правая верхняя | 30–35 % | Второй по частоте источник. Анатомическая близость к синусовому узлу и верхней полой вене. |
| Левая нижняя | 10–15 % | Частый триггер при анатомическом варианте «общий ствол». |
| Правая нижняя | 5–10 % | Наименее частый источник триггера |
Анатомические варианты легочных вен встречаются часто и являются важным фактором при планировании аблации ФП.
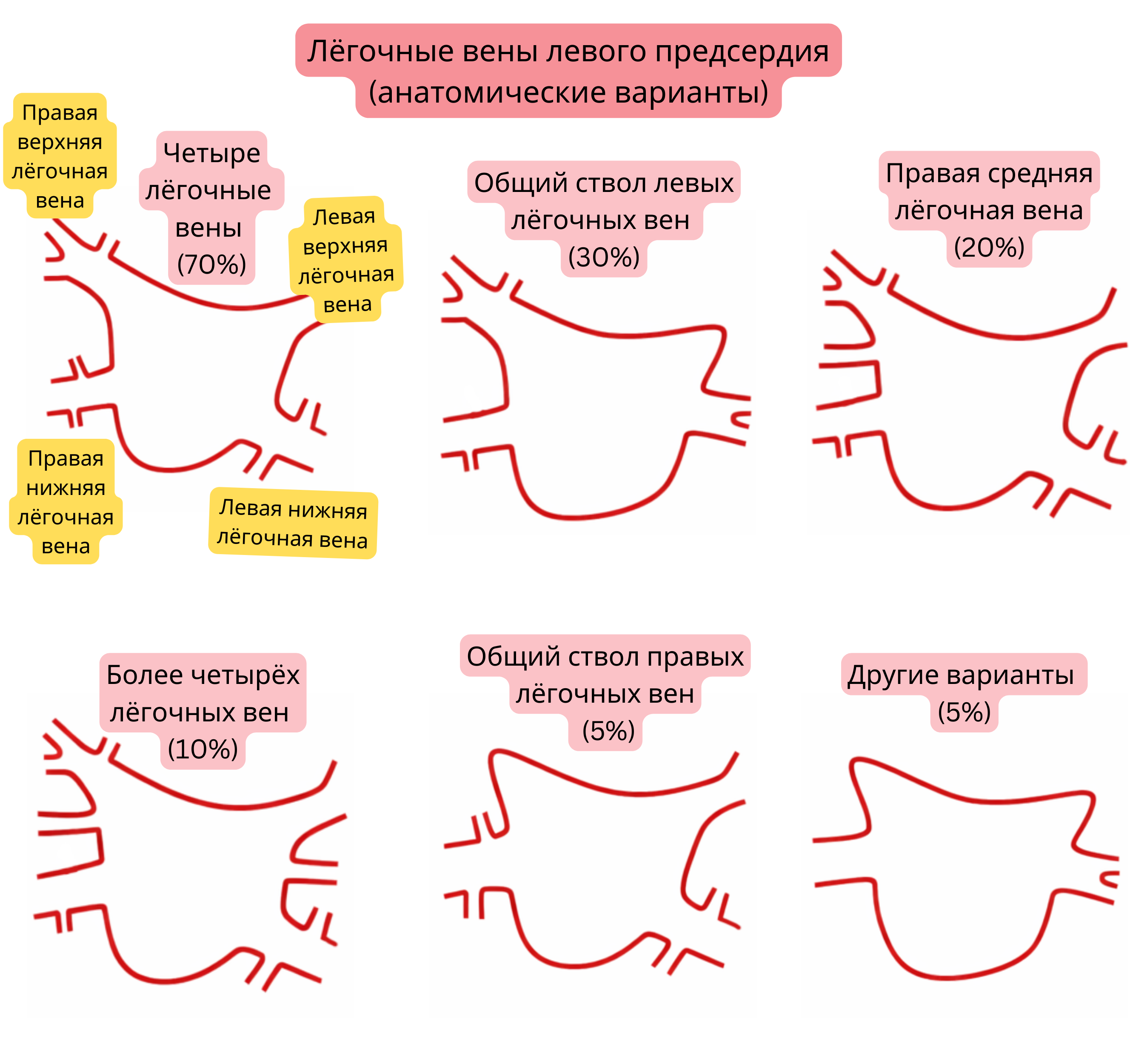
| Анатомические варианты легочных вен в левом предсердии | |
|---|---|
| Анатомический вариант | Частота |
| Типичная анатомия (4 отдельные легочные вены) | 60–70 % |
| Общий ствол левых легочных вен | 20–30 % |
| Правая средняя легочная вена (добавочная) | 15–25 % |
| Более 4 легочных вен (добавочные) | 5–10 % |
| Общий ствол правых легочных вен | <5 % |
| Ранняя бифуркация легочных вен | 10–15 % |
Триггер и субстрат
| Субстрат фибрилляции предсердий (локализация) | ||
|---|---|---|
| Анатомическая область | Основная анатомия | Частота (%) |
| Задняя стенка левого предсердия | Ограничена легочными венами. Наиболее частая зона фиброза. | 60–70 % |
| Устья легочных вен | Миокардиальные муфты, распространяющиеся на 1–4 см вглубь легочных вен (особенно верхних легочных вен) | 50–60 % |
| Крыша левого предсердия | Область, соединяющая верхние легочные вены. | 30–40 % |
| Межпредсердная перегородка | Область овальной ямки и пучка Бахмана. | 20–30 % |
| Ушко левого предсердия | Трабекулярный миокард ушка может формировать субстрат. | 10–20 % |
| Правое предсердие | Субстрат по частоте:
|
10–20 % |
| Митральный истмус | Зона между левой нижней легочной веной и митральным кольцом. Критическая область для развития перимитрального трепетания. 30–50% атипичных трепетаний левого предсердия проходят через митральный истмус. | 10–20 % |
Данные рекомендации являются неофициальными и не представляют собой официальные рекомендации, выпущенные каким-либо профессиональным кардиологическим обществом. Они предназначены исключительно для образовательных и информационных целей.
