

Il rimodellamento atriale è una conseguenza della cardiomiopatia atriale,
Negli atri rimodellati si sviluppano alterazioni elettriche che creano il substrato per la fibrillazione atriale (FA).
Le alterazioni elettriche insorgono principalmente nei siti in cui una struttura anatomica si continua in un’altra:
Un episodio di FA richiede due componenti per l’inizio e il mantenimento:
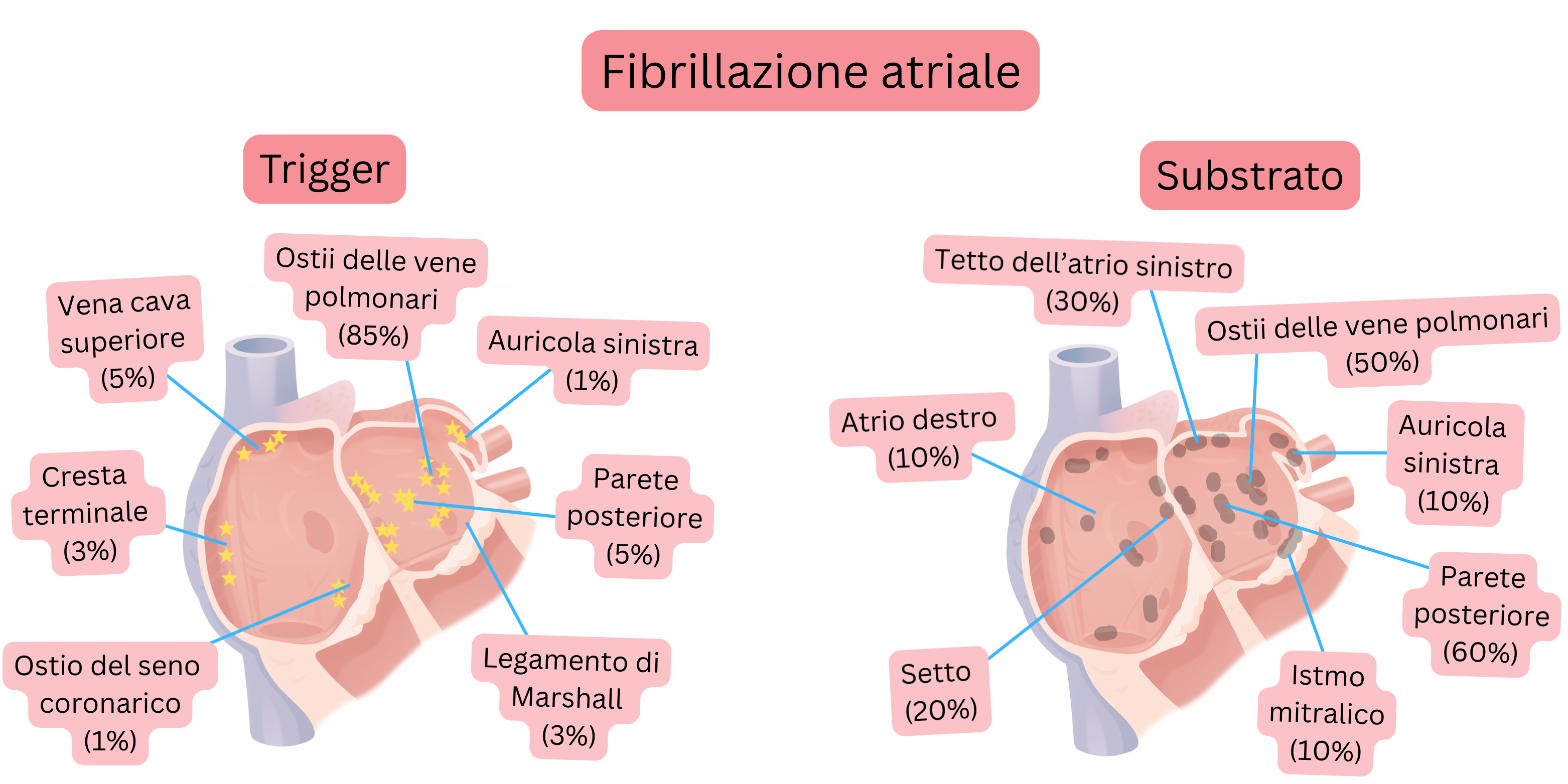
Trigger
Substrato
L’inizio e la durata di un episodio di FA dipendono dalla complessa interazione tra trigger, substrato e modulazione autonoma.
Quale extrasistole atriale o quale salva attivi il substrato e per quanto tempo persista l’episodio di FA è estremamente variabile. Dipende principalmente da:
Nella FA parossistica prevale il trigger
Nella FA persistente prevale il substrato
Trigger e substrato
La FA inizia come parossistica; gli episodi di FA generalmente si interrompono spontaneamente entro 24 ore.
Nel 90% dei casi di FA parossistica il trigger (solitamente anche il substrato) è localizzato nella regione degli osti delle vene polmonari.
| Trigger della fibrillazione atriale (localizzazione) | ||
|---|---|---|
| Sede anatomica | Anatomia di base | Prevalenza (%) |
| Osti delle vene polmonari | Manicotti miocardici che si estendono per 1–4 cm all’interno delle vene polmonari (soprattutto le vene polmonari superiori) | 85–90 % |
| Parete posteriore dell’atrio sinistro | La parete posteriore dell’atrio sinistro e gli antri delle vene polmonari condividono un’origine embriologica comune. Questo tessuto presenta proprietà elettrofisiologiche differenti rispetto al restante miocardio atriale. | 5–10 % |
| Vena cava superiore | Manicotti miocardici alla giunzione tra atrio destro e vena cava superiore | 2–5 % |
| Crista terminalis | Rilievo tra la porzione liscia e quella trabecolata dell’atrio destro | 1–3 % |
| Legamento di Marshall | Residuo della vena cava superiore sinistra embrionale; tratto epicardico che connette il seno coronarico con la regione delle vene polmonari sinistre. | 1–3 % |
| Ostio del seno coronarico | Manicotti miocardici nella transizione del seno coronarico nell’atrio destro. | 1–3 % |
| Auricola sinistra | Piccola estroflessione localizzata anterolateralmente sull’atrio sinistro. Il volume standard è 5–10 ml; in FA 10–20 ml. | 1–3 % |
Nel 90% dei casi di FA parossistica il trigger, spesso in combinazione con un substrato, è localizzato nella regione degli osti delle vene polmonari.
| Trigger nelle vene polmonari nella fibrillazione atriale (localizzazione) | ||
|---|---|---|
| Vena polmonare | Prevalenza | Nota |
| Superiore sinistra | 45–50 % | Fonte di trigger più frequente e più aggressiva. Spesso condivide un ostio comune (carena) con la vena polmonare inferiore sinistra. |
| Superiore destra | 30–35 % | Seconda fonte per frequenza. Prossimità anatomica al nodo del seno e alla vena cava superiore. |
| Inferiore sinistra | 10–15 % | Trigger frequente in presenza della variante anatomica “tronco comune”. |
| Inferiore destra | 5–10 % | Fonte di trigger meno frequente |
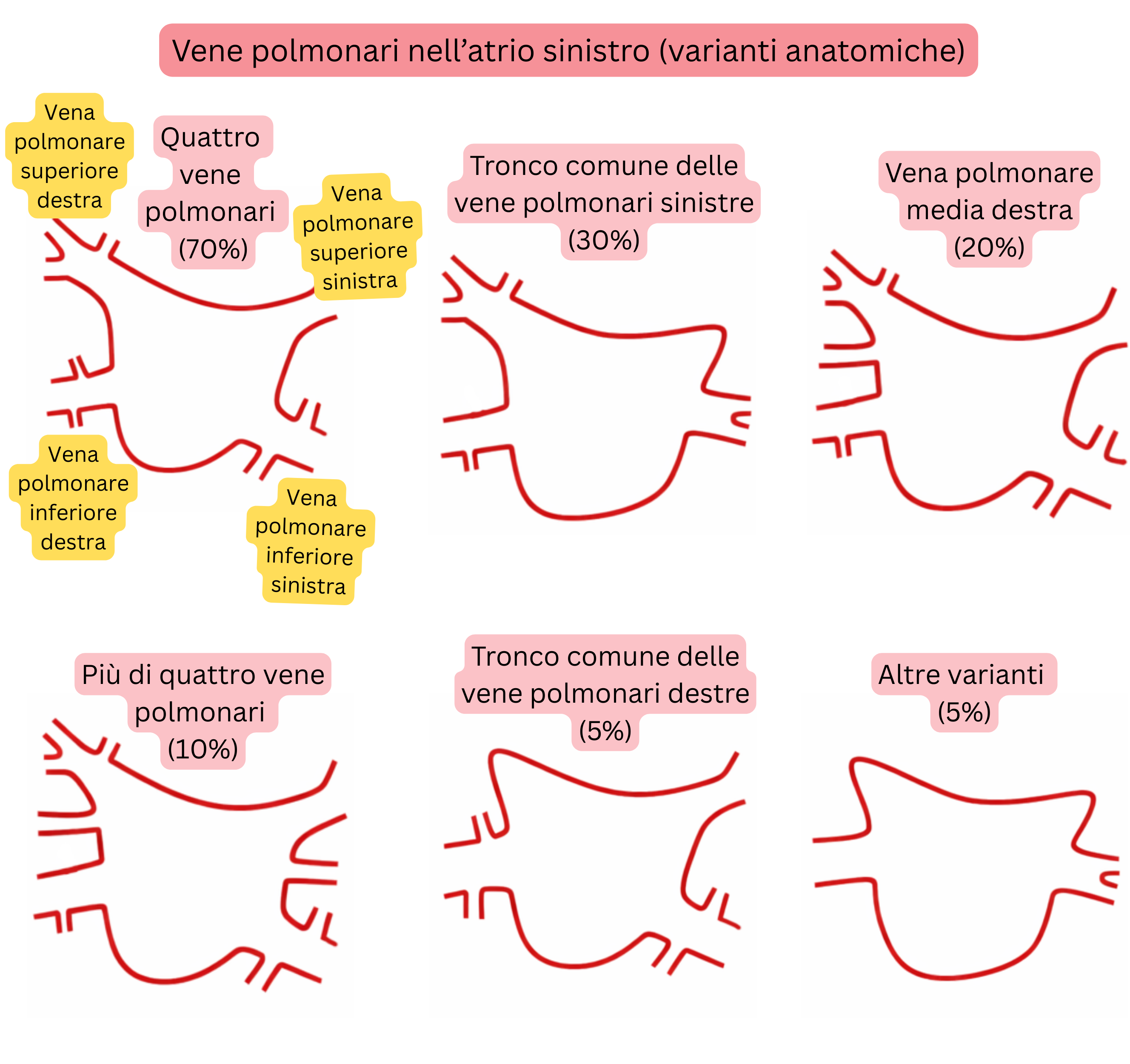
Le varianti anatomiche delle vene polmonari sono frequenti e rappresentano un fattore importante nella pianificazione dell’ablazione della FA.
| Varianti anatomiche delle vene polmonari nell’atrio sinistro | |
|---|---|
| Variante anatomica | Prevalenza |
| Anatomia tipica (4 vene polmonari separate) | 60–70 % |
| Tronco comune delle vene polmonari sinistre | 20–30 % |
| Vena polmonare media destra (accessoria) | 15–25 % |
| Più di 4 vene polmonari (accessorie) | 5–10 % |
| Tronco comune delle vene polmonari destre | <5 % |
| Biforcazione precoce delle vene polmonari | 10–15 % |
Trigger e substrato
| Substrato della fibrillazione atriale (localizzazione) | ||
|---|---|---|
| Sede anatomica | Anatomia di base | Prevalenza (%) |
| Parete posteriore dell’atrio sinistro | Delimitata dalle vene polmonari. Sede più frequente di fibrosi. | 60–70 % |
| Osti delle vene polmonari | Manicotti miocardici che si estendono per 1–4 cm all’interno delle vene polmonari (soprattutto le vene polmonari superiori) | 50–60 % |
| Tetto dell’atrio sinistro | Regione che connette le vene polmonari superiori. | 30–40 % |
| Setto interatriale | Regione attorno alla fossa ovale e al fascio di Bachmann. | 20–30 % |
| Auricola sinistra | La muscolatura trabecolata dell’auricola può rappresentare un substrato. | 10–20 % |
| Atrio destro | Substrato in base alla prevalenza:
|
10–20 % |
| Istmo mitralico | Zona tra la vena polmonare inferiore sinistra e l’anulus mitralico. Critica per lo sviluppo del flutter perimitralico. Il 30–50% dei flutter atriali sinistri atipici passa attraverso l’istmo mitralico. | 10–20 % |
Queste linee guida sono non ufficiali e non rappresentano linee guida formali emesse da alcuna società professionale di cardiologia. Sono destinate esclusivamente a scopi educativi e informativi.
