

El remodelado auricular es consecuencia de la miocardiopatía auricular,
En las aurículas remodeladas se desarrollan cambios eléctricos que crean el sustrato para la fibrilación auricular (FA).
Los cambios eléctricos surgen principalmente en los sitios donde una estructura anatómica transiciona a otra:
Un episodio de FA requiere dos componentes para su inicio y mantenimiento:

Desencadenante
Sustrato
El inicio y la duración de un episodio de FA dependen de la interacción compleja entre desencadenante, sustrato y modulación autonómica.
Qué extrasístole auricular o salva activa el sustrato y cuánto tiempo persiste el episodio de FA es extremadamente variable. Depende principalmente de:
En la FA paroxística predomina el desencadenante
En la FA persistente predomina el sustrato
Desencadenante y sustrato
La FA comienza como paroxística; los episodios de FA suelen terminar espontáneamente en un plazo de 24 horas.
El 90% de la FA paroxística tiene su desencadenante (habitualmente también el sustrato) en la región de los ostios de las venas pulmonares.
| Desencadenantes de la fibrilación auricular (localización) | ||
|---|---|---|
| Localización anatómica | Anatomía básica | Prevalencia (%) |
| Ostios de las venas pulmonares | Manguitos miocárdicos que se extienden 1–4 cm dentro de las venas pulmonares (especialmente las venas pulmonares superiores) | 85–90 % |
| Pared posterior de la aurícula izquierda | La pared posterior de la aurícula izquierda y los antra de las venas pulmonares comparten un origen embriológico común. Este tejido tiene propiedades electrofisiológicas diferentes en comparación con el resto del miocardio auricular. | 5–10 % |
| Vena cava superior | Manguitos miocárdicos en la unión de la aurícula derecha y la vena cava superior | 2–5 % |
| Crista terminalis | Cresta entre la parte lisa y la parte trabeculada de la aurícula derecha | 1–3 % |
| Ligamento de Marshall | Remanente de la vena cava superior izquierda embrionaria; tracto epicárdico que conecta el seno coronario con la región de las venas pulmonares izquierdas. | 1–3 % |
| Ostio del seno coronario | Manguitos miocárdicos en la transición del seno coronario hacia la aurícula derecha. | 1–3 % |
| Orejuela auricular izquierda | Pequeña evaginación localizada anterolateralmente en la aurícula izquierda. El volumen estándar de la orejuela es de 5–10 ml; en la fibrilación auricular 10–20 ml. | 1–3 % |
El 90% de la FA paroxística presenta un desencadenante, a menudo en combinación con un sustrato, localizado en la región de los ostios de las venas pulmonares.
| Desencadenantes en las venas pulmonares en la fibrilación auricular (localización) | ||
|---|---|---|
| Vena pulmonar | Prevalencia | Nota |
| Superior izquierda | 45–50 % | La fuente desencadenante más frecuente y más agresiva. A menudo comparte un ostio común (carina) con la vena pulmonar inferior izquierda. |
| Superior derecha | 30–35 % | Segunda fuente más frecuente. Proximidad anatómica al nodo sinusal y a la vena cava superior. |
| Inferior izquierda | 10–15 % | Desencadenante frecuente en presencia de la variante anatómica «tronco común». |
| Inferior derecha | 5–10 % | Fuente desencadenante menos frecuente |
Las variantes anatómicas de las venas pulmonares son frecuentes y representan un factor importante en la planificación de la ablación de la FA.
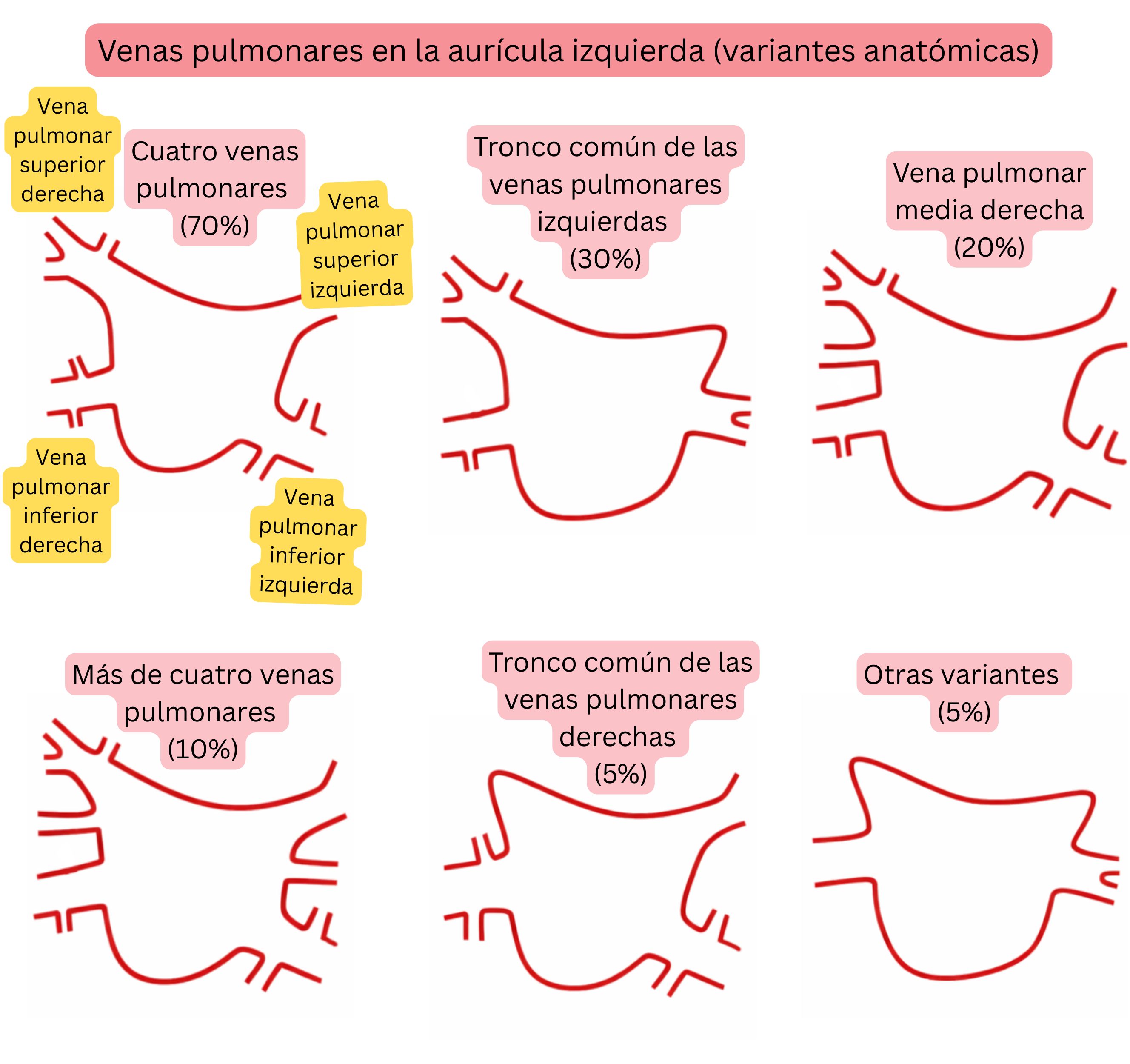
| Variantes anatómicas de las venas pulmonares en la aurícula izquierda | |
|---|---|
| Variante anatómica | Prevalencia |
| Anatomía típica (4 venas pulmonares separadas) | 60–70 % |
| Tronco común de las venas pulmonares izquierdas | 20–30 % |
| Vena pulmonar media derecha (accesoria) | 15–25 % |
| Más de 4 venas pulmonares (accesorias) | 5–10 % |
| Tronco común de las venas pulmonares derechas | <5 % |
| Bifurcación precoz de las venas pulmonares | 10–15 % |
Desencadenante y sustrato
| Sustrato de la fibrilación auricular (localización) | ||
|---|---|---|
| Localización anatómica | Anatomía básica | Prevalencia (%) |
| Pared posterior de la aurícula izquierda | Limitada por las venas pulmonares. Es el sitio más frecuente de fibrosis. | 60–70 % |
| Ostios de las venas pulmonares | Manguitos miocárdicos que se extienden 1–4 cm dentro de las venas pulmonares (especialmente las venas pulmonares superiores) | 50–60 % |
| Techo de la aurícula izquierda | Región que conecta las venas pulmonares superiores. | 30–40 % |
| Tabique interauricular | Región alrededor de la fosa oval y el haz de Bachmann. | 20–30 % |
| Orejuela auricular izquierda | La musculatura trabeculada de la orejuela puede representar un sustrato. | 10–20 % |
| Aurícula derecha | Sustrato según prevalencia:
|
10–20 % |
| Istmo mitral | Zona entre la vena pulmonar inferior izquierda y el anillo mitral. Crítico para el desarrollo de flutter perimitral. El 30–50% de los flutters auriculares izquierdos atípicos atraviesan el istmo mitral. | 10–20 % |
Estas guías son no oficiales y no representan guías formales emitidas por ninguna sociedad profesional de cardiología. Están destinadas únicamente a fines educativos e informativos.
