

Das atriale Remodeling ist eine Folge der atrialen Kardiomyopathie,
In remodelierten Vorhöfen entwickeln sich elektrische Veränderungen, die das Substrat für Vorhofflimmern (VHF) bilden.
Elektrische Veränderungen entstehen vor allem an Übergangsstellen zwischen unterschiedlichen anatomischen Strukturen:
Eine Episode von VHF erfordert für Initiierung und Aufrechterhaltung zwei Komponenten:
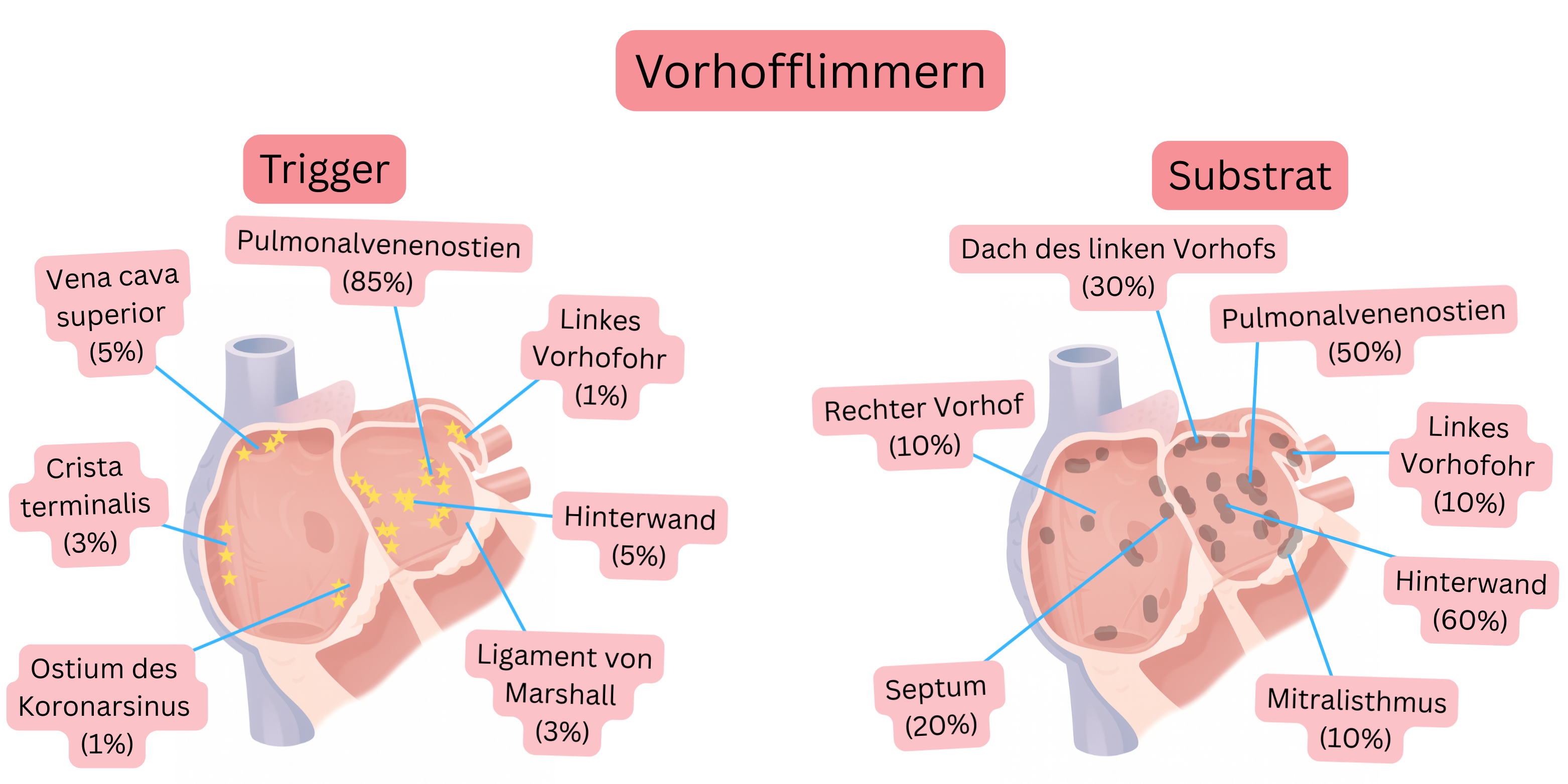
Trigger
Substrat
Initiierung und Dauer einer VHF-Episode hängen von der komplexen Interaktion zwischen Trigger, Substrat und autonomer Modulation ab.
Welche Vorhofextrasystole oder Salve das Substrat aktiviert und wie lange die VHF-Episode anhält, ist äußerst variabel. Dies hängt vor allem ab von:
Beim paroxysmalen VHF dominiert der Trigger
Beim persistierenden VHF dominiert das Substrat
Trigger und Substrat
VHF beginnt als paroxysmales VHF; Episoden terminieren in der Regel spontan innerhalb von 24 Stunden.
90 % des paroxysmalen VHF haben ihren Trigger (meist auch das Substrat) im Bereich der Pulmonalvenenostien.
| Trigger des Vorhofflimmerns (Lokalisation) | ||
|---|---|---|
| Anatomische Lokalisation | Grundlegende Anatomie | Prävalenz (%) |
| Pulmonalvenenostien | Myokardiale Sleeves, die sich 1–4 cm in die Pulmonalvenen hinein erstrecken (insbesondere die oberen Pulmonalvenen) | 85–90 % |
| Hinterwand des linken Vorhofs | Die Hinterwand des linken Vorhofs und die Pulmonalvenenantra haben einen gemeinsamen embryologischen Ursprung. Dieses Gewebe weist andere elektrophysiologische Eigenschaften auf als das übrige Vorhofmyokard. | 5–10 % |
| Vena cava superior | Myokardiale Sleeves am Übergang vom rechten Vorhof zur Vena cava superior | 2–5 % |
| Crista terminalis | Leiste zwischen glattem und trabekuliertem Anteil des rechten Vorhofs | 1–3 % |
| Ligament von Marshall | Überrest der embryonalen linken Vena cava superior; epikardialer Trakt zwischen Koronarsinus und Region der linken Pulmonalvenen | 1–3 % |
| Ostium des Koronarsinus | Myokardiale Sleeves am Übergang des Koronarsinus in den rechten Vorhof | 1–3 % |
| Linkes Vorhofohr | Kleine anterolateral gelegene Ausstülpung des linken Vorhofs. Normales Volumen 5–10 ml; bei VHF 10–20 ml. | 1–3 % |
90 % des paroxysmalen VHF weisen einen Trigger, häufig in Kombination mit einem Substrat, im Bereich der Pulmonalvenenostien auf.
| Trigger in den Pulmonalvenen bei Vorhofflimmern (Lokalisation) | ||
|---|---|---|
| Pulmonalvene | Prävalenz | Bemerkung |
| Links superior | 45–50 % | Häufigste und aggressivste Triggerquelle. Oft gemeinsames Ostium (Carina) mit der linken inferioren Pulmonalvene. |
| Rechts superior | 30–35 % | Zweithäufigste Quelle. Anatomische Nähe zum Sinusknoten und zur Vena cava superior. |
| Links inferior | 10–15 % | Häufiger Trigger bei anatomischer Variante „Common trunk“. |
| Rechts inferior | 5–10 % | Seltenste Triggerquelle |
Anatomische Varianten der Pulmonalvenen sind häufig und stellen einen wichtigen Faktor bei der Planung einer VHF-Ablation dar.
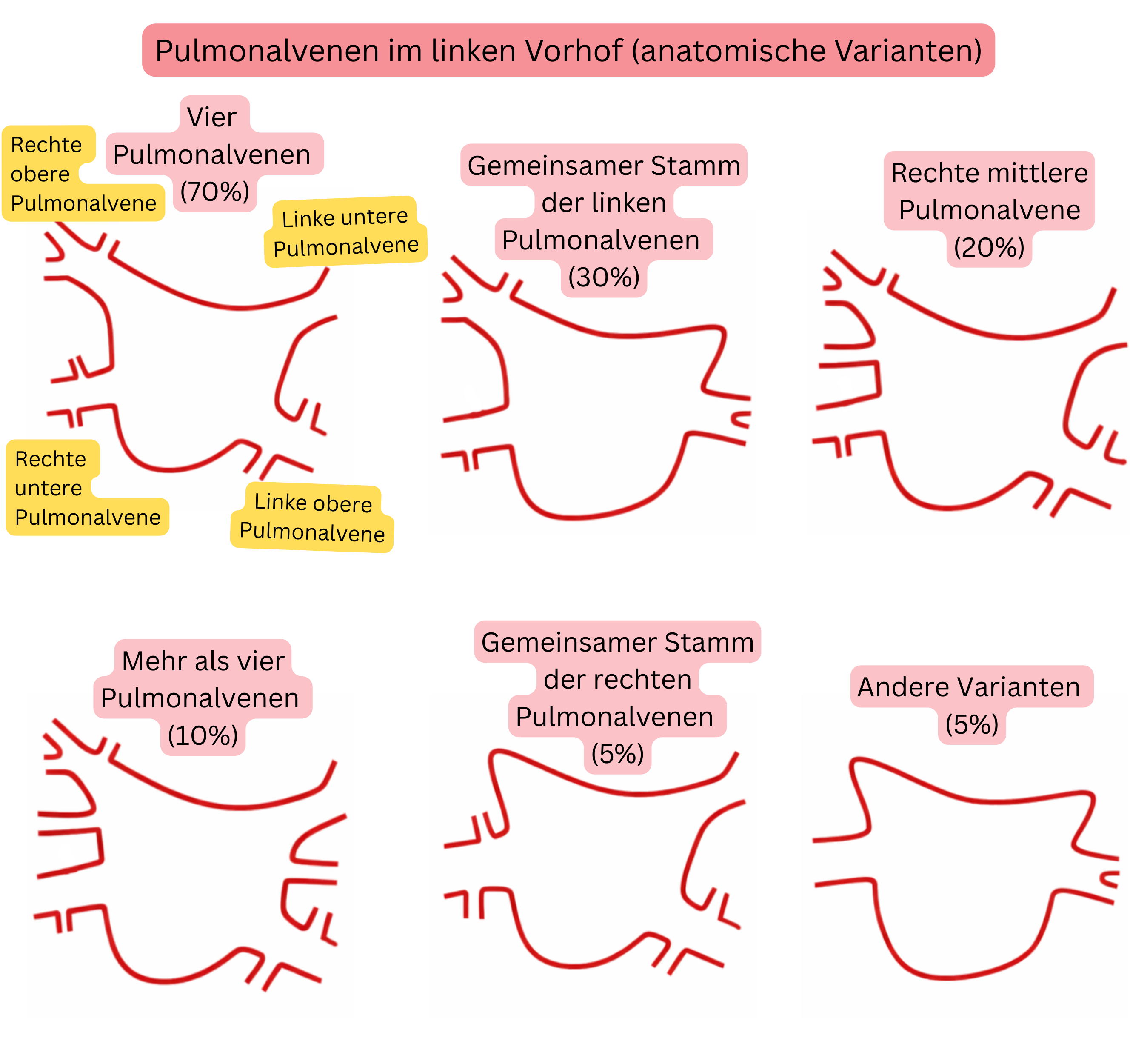
| Anatomische Varianten der Pulmonalvenen im linken Vorhof | |
|---|---|
| Anatomische Variante | Prävalenz |
| Typische Anatomie (4 separate Pulmonalvenen) | 60–70 % |
| Gemeinsamer Stamm der linken Pulmonalvenen | 20–30 % |
| Rechte mittlere Pulmonalvene (akzessorisch) | 15–25 % |
| Mehr als 4 Pulmonalvenen (akzessorisch) | 5–10 % |
| Gemeinsamer Stamm der rechten Pulmonalvenen | <5 % |
| Frühe Bifurkation der Pulmonalvenen | 10–15 % |
Trigger und Substrat
| Substrat des Vorhofflimmerns (Lokalisation) | ||
|---|---|---|
| Anatomische Lokalisation | Grundlegende Anatomie | Prävalenz (%) |
| Hinterwand des linken Vorhofs | Begrenzt durch die Pulmonalvenen. Häufigste Lokalisation fibrotischer Veränderungen. | 60–70 % |
| Pulmonalvenenostien | Myokardiale Sleeves, die sich 1–4 cm in die Pulmonalvenen erstrecken (insbesondere die oberen Pulmonalvenen) | 50–60 % |
| Dach des linken Vorhofs | Region zwischen den oberen Pulmonalvenen. | 30–40 % |
| Interatriales Septum | Region um die Fossa ovalis und das Bachmann-Bündel. | 20–30 % |
| Linkes Vorhofohr | Die trabekulierte Muskulatur des Vorhofohrs kann ein Substrat darstellen. | 10–20 % |
| Rechter Vorhof | Substratlokalisation nach Häufigkeit:
|
10–20 % |
| Mitralisthmus | Zone zwischen linker inferiorer Pulmonalvene und Mitralannulus. Kritisch für die Entstehung eines perimitralen Flatterns. 30–50 % der atypischen linksatrialen Flattern verlaufen über den Mitralisthmus. | 10–20 % |
Diese Leitlinien sind inoffiziell und stellen keine offiziellen Leitlinien dar, die von einer kardiologischen Fachgesellschaft herausgegeben wurden. Sie dienen ausschließlich zu Bildungs- und Informationszwecken.
