

Le remodelage atrial est une conséquence de la cardiomyopathie atriale,
Dans les oreillettes remodelées, des modifications électriques se développent et créent le substrat de la fibrillation atriale (FA).
Les modifications électriques apparaissent principalement aux sites de transition entre deux structures anatomiques :
Un épisode de FA nécessite deux composantes pour son initiation et son maintien :
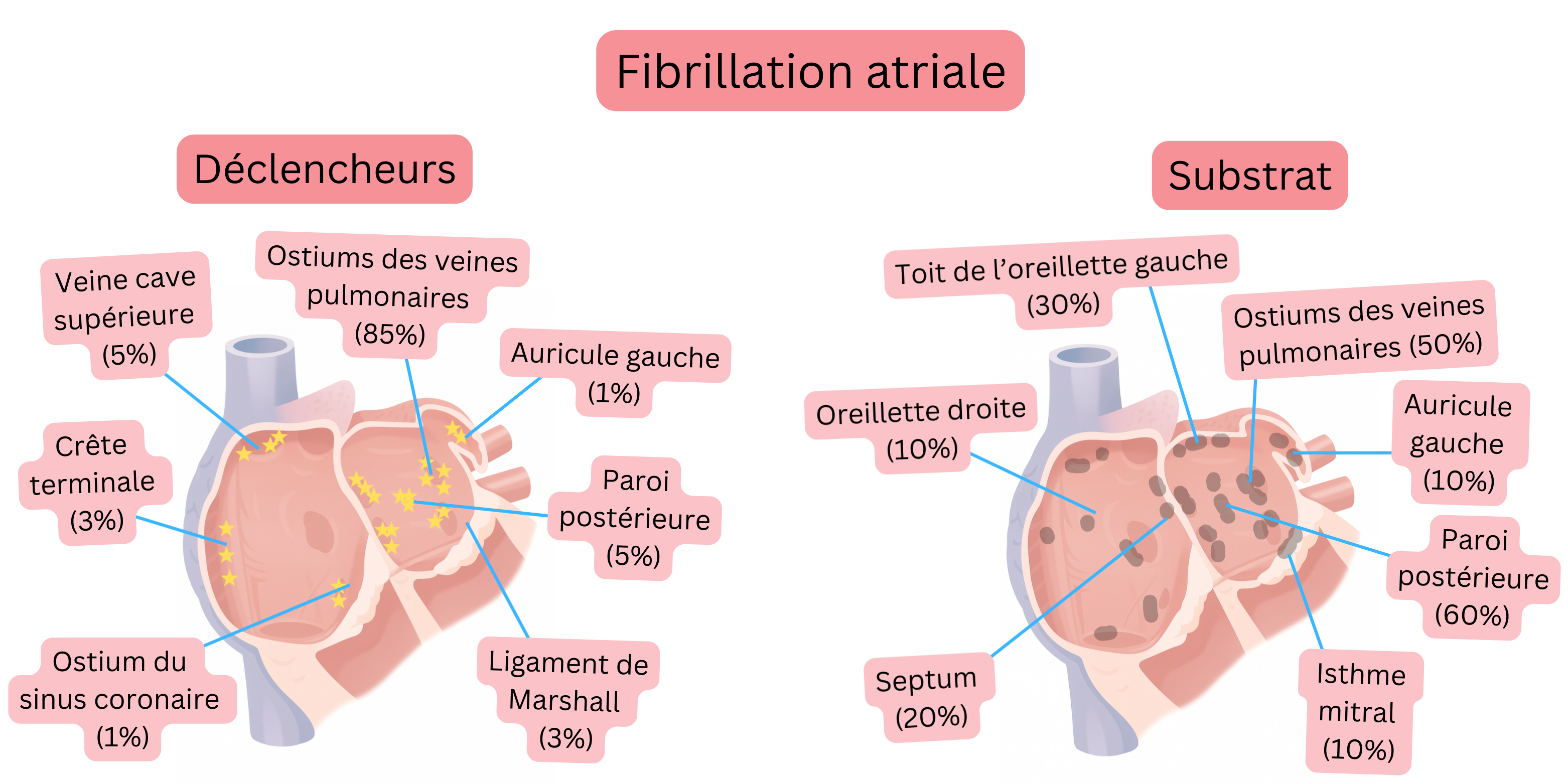
Déclencheur
Substrat
L’initiation et la durée d’un épisode de FA dépendent de l’interaction complexe entre le déclencheur, le substrat et la modulation autonome.
L’extrasystole atriale ou la salve qui active le substrat et la durée de persistance de l’épisode de FA sont extrêmement variables. Elles dépendent principalement :
Dans la FA paroxystique, le déclencheur prédomine
Dans la FA persistante, le substrat prédomine
Déclencheur et substrat
La FA débute sous forme paroxystique ; les épisodes de FA se terminent généralement spontanément en moins de 24 heures.
90% des FA paroxystiques ont leur déclencheur (souvent également le substrat) dans la région des ostiums des veines pulmonaires.
| Déclencheurs de la fibrillation atriale (localisation) | ||
|---|---|---|
| Site anatomique | Anatomie de base | Prévalence (%) |
| Ostiums des veines pulmonaires | Manchons myocardiques s’étendant sur 1–4 cm à l’intérieur des veines pulmonaires (en particulier les veines pulmonaires supérieures) | 85–90 % |
| Paroi postérieure de l’oreillette gauche | La paroi postérieure de l’oreillette gauche et les antrums des veines pulmonaires partagent une origine embryologique commune. Ce tissu présente des propriétés électrophysiologiques différentes du reste du myocarde atrial. | 5–10 % |
| Veine cave supérieure | Manchons myocardiques à la jonction entre l’oreillette droite et la veine cave supérieure | 2–5 % |
| Crista terminalis | Crête entre les parties lisse et trabéculée de l’oreillette droite | 1–3 % |
| Ligament de Marshall | Vestige de la veine cave supérieure gauche embryonnaire ; tractus épicardique reliant le sinus coronaire à la région des veines pulmonaires gauches. | 1–3 % |
| Ostium du sinus coronaire | Manchons myocardiques à la transition du sinus coronaire vers l’oreillette droite. | 1–3 % |
| Appendice auriculaire gauche | Petite poche située en position antérolatérale sur l’oreillette gauche. Le volume normal de l’appendice est de 5–10 ml ; en cas de FA 10–20 ml. | 1–3 % |
90% des FA paroxystiques présentent un déclencheur, souvent associé à un substrat, localisé dans la région des ostiums des veines pulmonaires.
| Déclencheurs dans les veines pulmonaires en cas de fibrillation atriale (localisation) | ||
|---|---|---|
| Veine pulmonaire | Prévalence | Remarque |
| Supérieure gauche | 45–50 % | Source déclenchante la plus fréquente et la plus agressive. Partage souvent un ostium commun (carina) avec la veine pulmonaire inférieure gauche. |
| Supérieure droite | 30–35 % | Deuxième source la plus fréquente. Proximité anatomique du nœud sinusal et de la veine cave supérieure. |
| Inférieure gauche | 10–15 % | Déclencheur fréquent en présence de la variante anatomique « tronc commun ». |
| Inférieure droite | 5–10 % | Source déclenchante la moins fréquente |
Les variantes anatomiques des veines pulmonaires sont fréquentes et constituent un facteur important dans la planification de l’ablation de la FA.
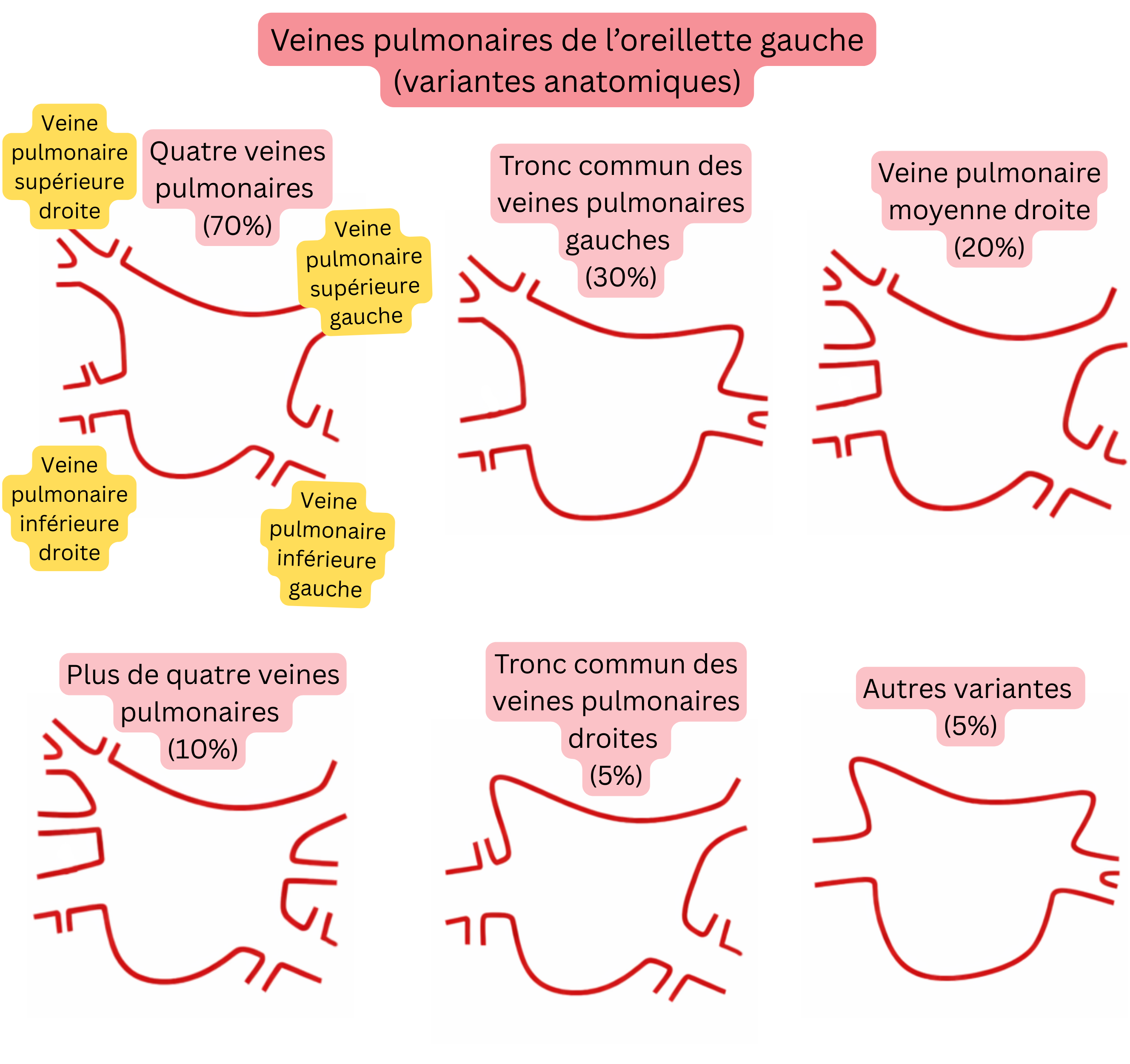
| Variantes anatomiques des veines pulmonaires dans l’oreillette gauche | |
|---|---|
| Variante anatomique | Prévalence |
| Anatomie typique (4 veines pulmonaires distinctes) | 60–70 % |
| Tronc commun des veines pulmonaires gauches | 20–30 % |
| Veine pulmonaire moyenne droite (accessoire) | 15–25 % |
| Plus de 4 veines pulmonaires (accessoires) | 5–10 % |
| Tronc commun des veines pulmonaires droites | <5 % |
| Bifurcation précoce des veines pulmonaires | 10–15 % |
Déclencheur et substrat
| Substrat de la fibrillation atriale (localisation) | ||
|---|---|---|
| Site anatomique | Anatomie de base | Prévalence (%) |
| Paroi postérieure de l’oreillette gauche | Limitée par les veines pulmonaires. Site le plus fréquent de fibrose. | 60–70 % |
| Ostiums des veines pulmonaires | Manchons myocardiques s’étendant sur 1–4 cm à l’intérieur des veines pulmonaires (en particulier les veines pulmonaires supérieures) | 50–60 % |
| Toit de l’oreillette gauche | Région reliant les veines pulmonaires supérieures. | 30–40 % |
| Septum interatrial | Région autour de la fosse ovale et du faisceau de Bachmann. | 20–30 % |
| Appendice auriculaire gauche | La musculature trabéculée de l’appendice peut constituer un substrat. | 10–20 % |
| Oreillette droite | Substrat selon la prévalence :
|
10–20 % |
| Isthme mitral | Zone entre la veine pulmonaire inférieure gauche et l’anneau mitral. Critique pour le développement du flutter périmitral. 30–50% des flutters atypiques de l’oreillette gauche traversent l’isthme mitral. | 10–20 % |
Ces recommandations sont non officielles et ne représentent pas des recommandations formelles émises par une société professionnelle de cardiologie. Elles sont destinées uniquement à des fins éducatives et informatives.
