分類:
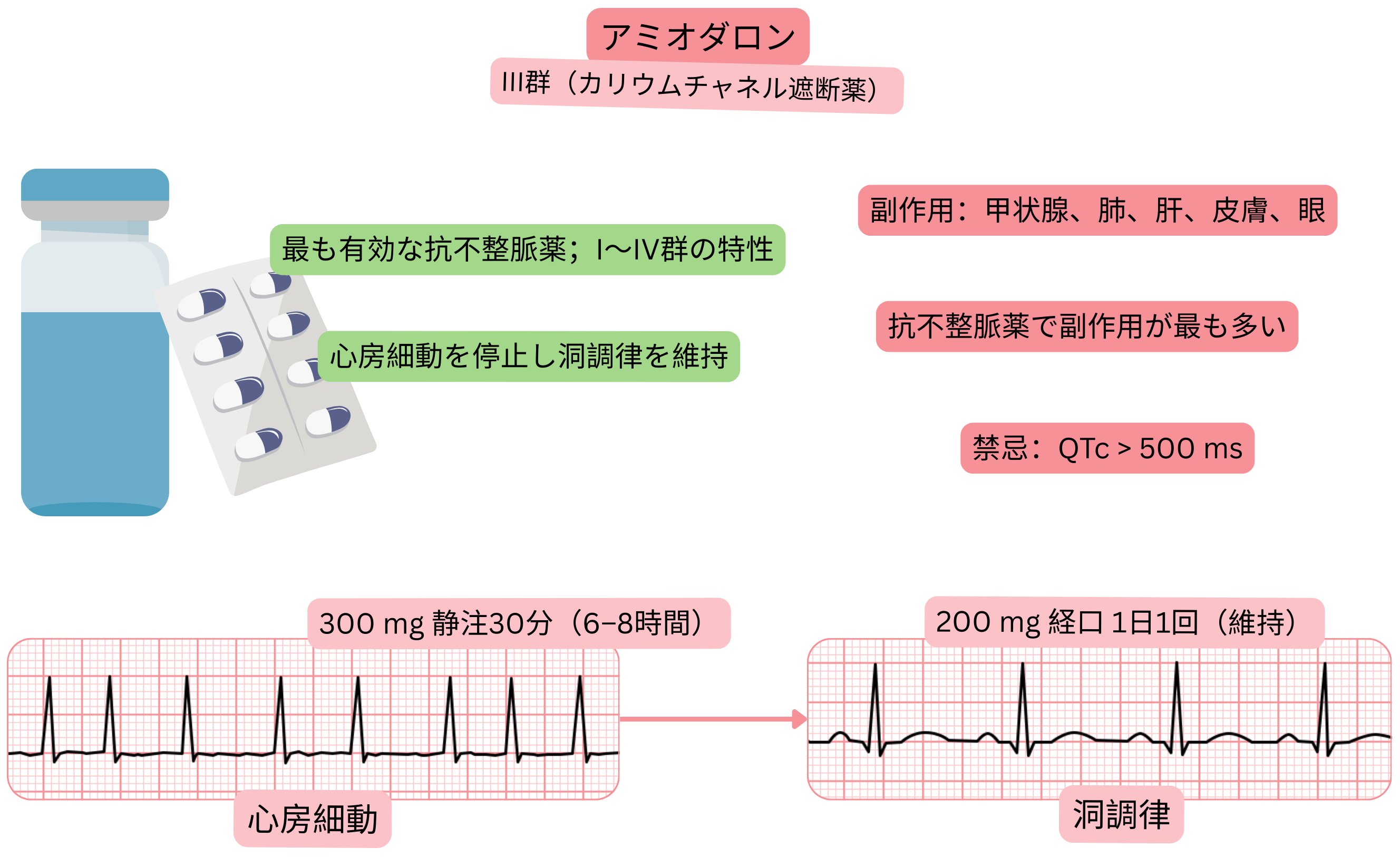
- クラス III ― カリウム(K⁺)チャネル遮断薬
- アミオダロン ― 最も有効な抗不整脈薬であるが、有害事象発現率が最も高い。
- ドロネダロン ― アミオダロンと類似するが、作用は弱く、有害事象は少ない。
- ソタロール ― 非選択的β遮断薬でもある。
- イブチリド ― 副伝導路を伴う心房細動の急性洞調律化に使用し得る。
作用機序:
- 最も有効な抗不整脈薬であるが、有害事象発現率が最も高い
- 主としてクラスIIIの特性を示すが、クラスI、II、IV作用も有する
- 心房・心室筋の有効不応期(ERP)を延長する
- 興奮性および自動能を低下させ、リエントリーを抑制する
- 洞結節を抑制し、房室結節伝導を延長する
- 刺激伝導系および作業心筋の伝導を抑制する
- 血管平滑筋に対し血管拡張作用を有する
- 逆使用依存性は最小限である
心房細動への作用:
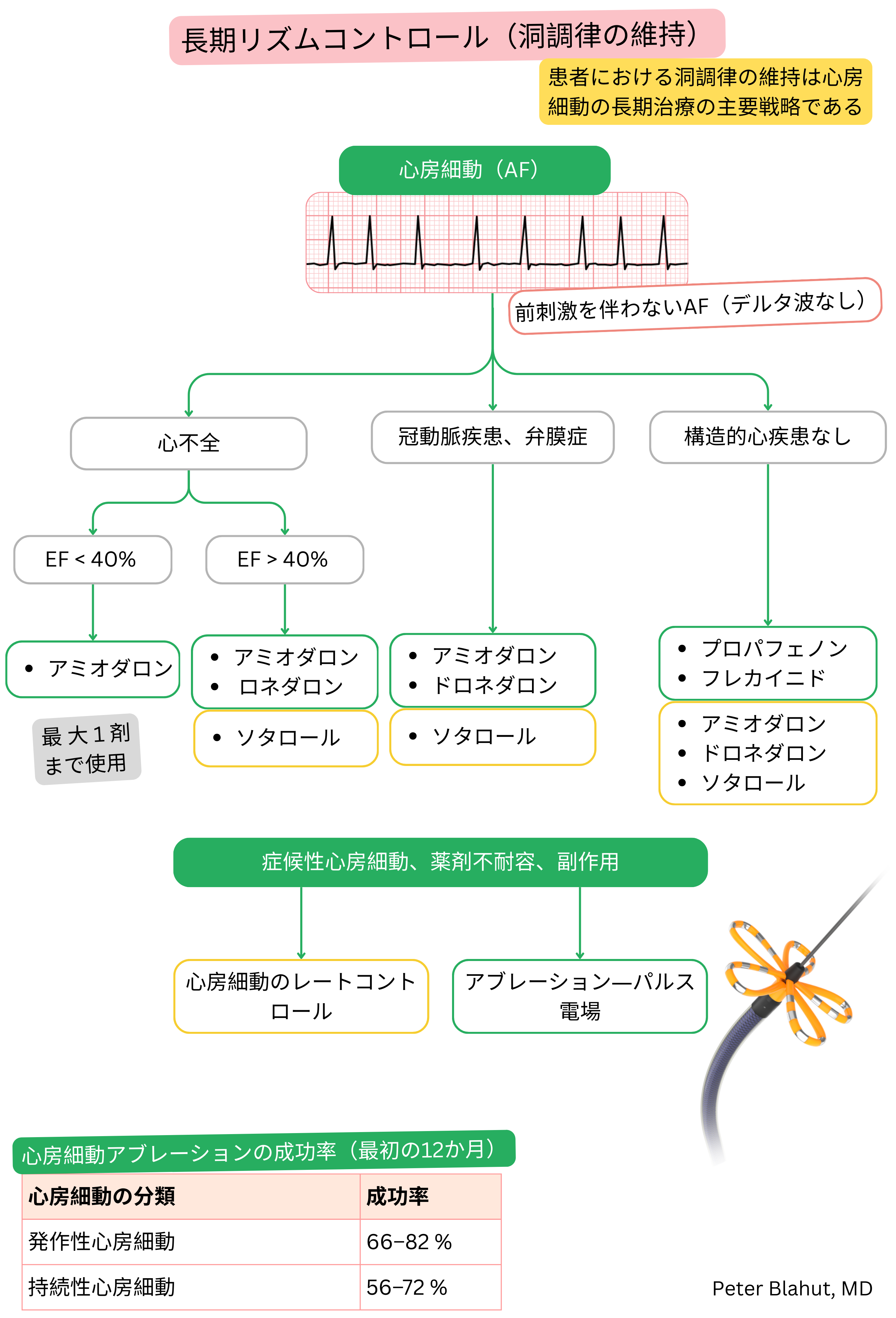
- 洞調律維持 ― 心房細動エピソードの再発を予防する
- 心房細動を洞調律へ除細動する ― 心房細動発作の停止および洞調律の回復
アミオダロンの分布容積
- アミオダロンは分布容積が大きく、
- 全身組織、特に脂肪に富む組織に蓄積し、その後徐々に放出される:
- 分布容積が大きいため、薬物動態は他の抗不整脈薬と大きく異なる。
|
アミオダロンの基本特性
|
| 特性 |
説明 |
| 作用発現 |
7–21日(経口投与) |
| 長期効果 |
約10 gの負荷(静脈内投与+経口投与)後にのみ明らかとなる |
| 半減期 |
約50日(経口投与) |
| 中止後の作用 |
2–3か月 |
| 用量調整の反映 |
遅れて出現する(数週) |
アミオダロン負荷(10 g)
- 長期経口アミオダロン療法の原則は、総累積投与量10 g投与後にのみ効果が明らかとなることである。
- 累積10 gが経口投与か静脈内投与かは問わない。
- 負荷は通常、入院下で静脈内投与(例:3 g)から開始し、その後在宅で経口投与(7 g)を継続する。
- アミオダロンの最大1日量は1200 mg(静脈内投与+経口投与)である。
- 慢性維持量は200 mg 1日1回である。
| アミオダロンと心房細動 |
| 商品名 |
|
Cordarone, Amiodaron, Amiohexal, Amiokordin, Aratac, Acrodarona
|
| 適応 |
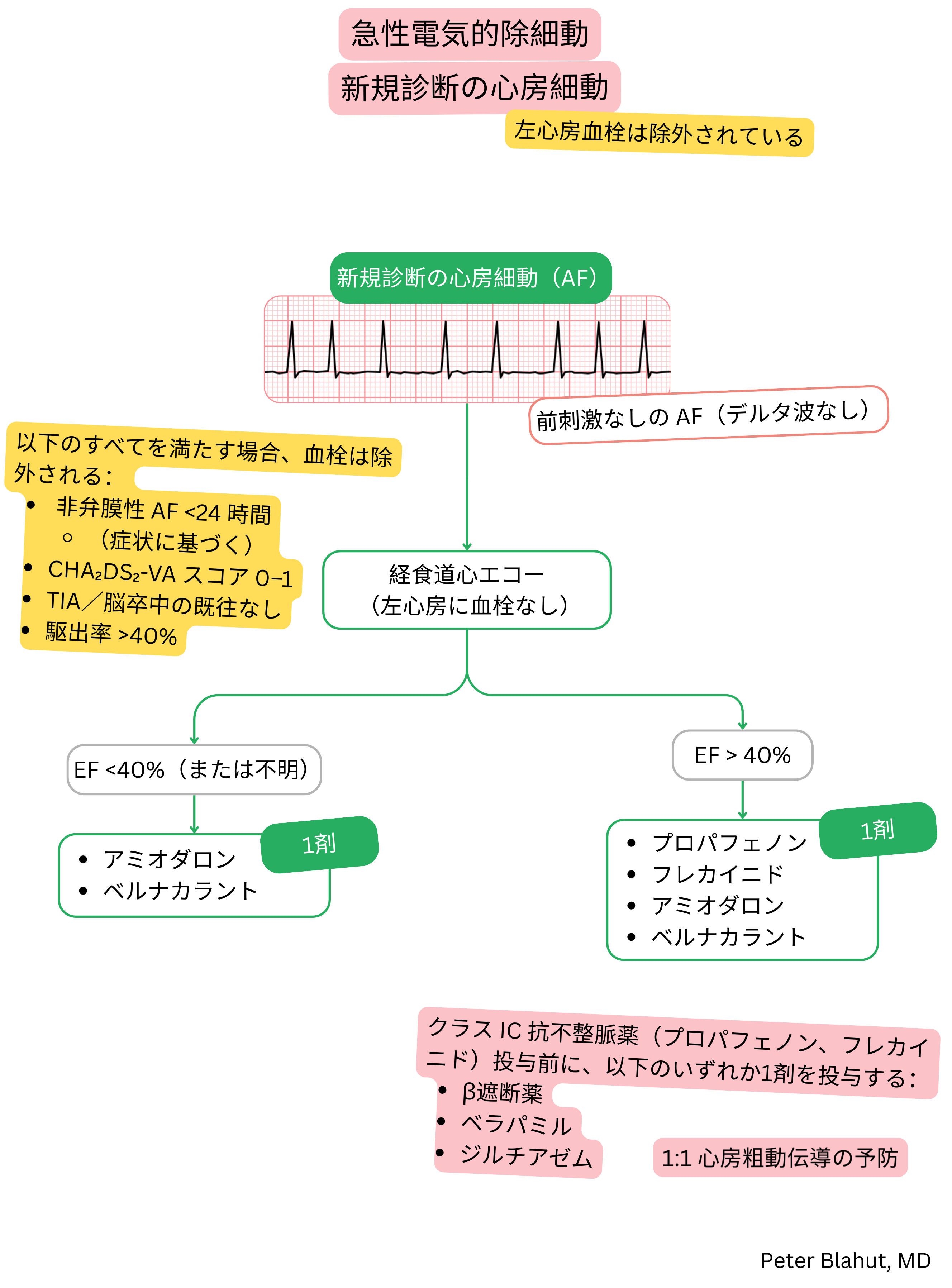
- 心房細動の急性洞調律化
- 洞調律維持
- 心房細動の電気的除細動前のアミオダロン負荷(10 g)
|
| 用量 |
- 心房細動の急性洞調律化(静脈内投与)
- 300 mgを30–60 分で静脈内投与する
- 続いて900–1200 mgを24 時間で持続静注する
- 長期治療への移行(除細動後)
- 総累積投与量10 gに達するまで200 mgを1日3回投与する
- 以後、200 mg 1日1回 ― 週7 日投与、または有害事象がある場合は週5 日投与
- 電気的除細動の準備(経口投与)
- 200 mgを2 週間、1日3回投与する
- 以後、200 mg 1日1回
- 総累積投与量 > 10 g後に除細動を施行し得る
- 長期治療(10 g負荷後)
- 200 mg 1日1回 ― 週7 日投与、または有害事象がある場合は週5 日投与
|
| 作用発現時間 |
- 6–8 時間(静脈内投与)
- 7–21 日(経口投与)― 通常、10 g負荷後
|
| 効果 |
洞調律化までの時間と成功率
- 6–8 時間 ― 44–80 %(静脈内投与)
- 7–21 日 ― 12–87 %(経口投与)― 通常、10 g負荷後
洞調律維持(発作性または持続性心房細動)1 年
|
| 作用持続時間 |
- 20–25 時間(静脈内ボーラス)
- 2 週 ― 2–3 か月(10 g負荷後の経口投与)
|
| 禁忌 |
- 副伝導路を伴う心房細動(心電図でデルタ波)
- 重度の電解質異常(特に低カリウム血症)
- 徐脈(< 50/分)
- 洞不全症候群(ペースメーカー未植込み)
- II度またはIII度房室ブロック(ペースメーカー未植込み)
- 低血圧(収縮期血圧 < 100 mmHg)
- QTc延長(> 500 ms)
- 妊娠(特に第1三半期)
- 授乳
- torsades de pointesの既往
- 甲状腺機能亢進症または甲状腺機能低下症(コントロール不良)
- 重度の呼吸不全
- アミオダロンに対するアレルギー
- ヨードに対するアレルギー
|
アミオダロン開始前および開始後の患者モニタリング:
- 開始前は、甲状腺、眼、肺、心、肝を中心に包括的に評価する
- 有害事象が出現した場合は中止または減量する
|
アミオダロン治療開始前および治療中の患者モニタリング
|
| 時期 |
観察項目 |
治療中止理由 |
| 開始前 |
心電図(QTc間隔、房室ブロック)
甲状腺機能(TSH、fT4)
肝機能検査(ALT、AST、GGT、ALP、ビリルビン)
電解質(Na、K、Mg)
胸部X線またはHRCT
スパイロメトリー
眼科的検査
診察(皮膚、神経学的所見)
|
QTc > 500 ms
II度またはIII度房室ブロック
肝機能検査異常
甲状腺機能低下症または甲状腺機能亢進症
重度の電解質異常(特に低カリウム血症)
肺線維症または間質性肺炎
|
| 6か月ごと |
心電図(QTc間隔、房室ブロック)
甲状腺機能(TSH、fT4)
肝機能検査(ALT、AST、GGT、ALP、ビリルビン)
電解質(Na、K、Mg)
診察(皮膚、神経学的所見)
|
QTc > 500 ms
II度またはIII度房室ブロック
咳嗽、呼吸困難、画像異常
肝機能検査異常
視覚障害(角膜沈着、視神経障害)
皮膚反応(青灰色変色、光線過敏)
重度の電解質異常(特に低カリウム血症)
|
| 12か月ごと |
眼科的検査
胸部X線またはHRCT
スパイロメトリー
診察(皮膚、神経学的所見)
|
咳嗽、呼吸困難、画像異常
視覚障害(角膜沈着、視神経障害)
皮膚反応(青灰色変色、光線過敏)
|
アミオダロンは組織蓄積により最も有効な抗不整脈薬である一方、有害事象発現率が最も高い。
- アミオダロンの12か月を超える投与は推奨されない。
有害事象 ― アミオダロン治療開始後1–2か月以降に出現し得る:
- 甲状腺:
- 甲状腺機能低下症(2–10 %)
- 甲状腺機能亢進症(1–10 %)
- 肺:
- 肺線維症(1–17 %)
- 間質性肺炎(5–10 %)
- ARDS(< 2 %)
- 肝:
- 肝酵素上昇(15–50 %)
- 肝炎(< 1 %)
- 肝壊死(< 1 %)
- 心:
- 低血圧(> 10 %)
- QT延長(1–10 %)
- 徐脈(2–5 %)
- torsades de pointes(< 1 %)
- 房室ブロック(< 1 %)
- 眼:
- 角膜沈着(98–99 %)
- 視神経障害(< 1 %)
- 霧視(1–10 %)
- 皮膚:
- 光線過敏(10–75 %)
- 皮膚の青灰色変色(8 %)
- Stevens–Johnson症候群(< 2 %)
- 神経学的:
- 運動失調、振戦、末梢神経障害(2–20 %)
- 倦怠感、不眠、めまい(1–10 %)
- 消化管:
- 悪心、便秘、食欲低下(5–10 %)
- 嘔吐(> 10 %)
- 下痢(< 2 %)
- 腎:
アミオダロンとドロネダロンはいずれもクラスIII抗不整脈薬であるが、性質が異なる。
- アミオダロンは洞調律維持により有効である一方、
- ドロネダロンは作用が弱いが、有害事象が少ない。
|
心房細動におけるアミオダロンとドロネダロンの比較
|
| 特性 |
アミオダロン |
ドロネダロン |
| 有効性(洞調律維持) |
1年で60–70 % |
1年で30–40 % |
| 作用発現 |
遅い(日–週、約10 g負荷後に十分な効果) |
速い(3–6時間) |
| 作用持続 |
中止後も2–3か月持続する |
12–24時間(休薬で消失する) |
| 適した患者 |
器質的心疾患を伴う場合も可 |
器質的心疾患がなく、駆出率が保たれている患者 |
| 心不全 |
使用し得る(HFrEFを含む) |
禁忌(NYHA III–IV、HFrEF < 40 %) |
| 組織蓄積 |
あり ― 脂肪組織、肺、眼、甲状腺 |
最小限 |
| 肺(毒性) |
肺線維症、間質性肺炎 |
肺毒性なし |
| 肝(毒性) |
軽度の肝毒性、肝酵素上昇 |
重症肝炎、肝不全の可能性 |
| 甲状腺(毒性) |
甲状腺機能低下症および甲状腺機能亢進症 |
甲状腺への影響なし |
| 眼(毒性) |
角膜沈着、視神経障害 |
眼毒性なし |
| 皮膚(毒性) |
光線過敏、青灰色皮膚変色 |
皮疹、そう痒 |