

Klassifikation:
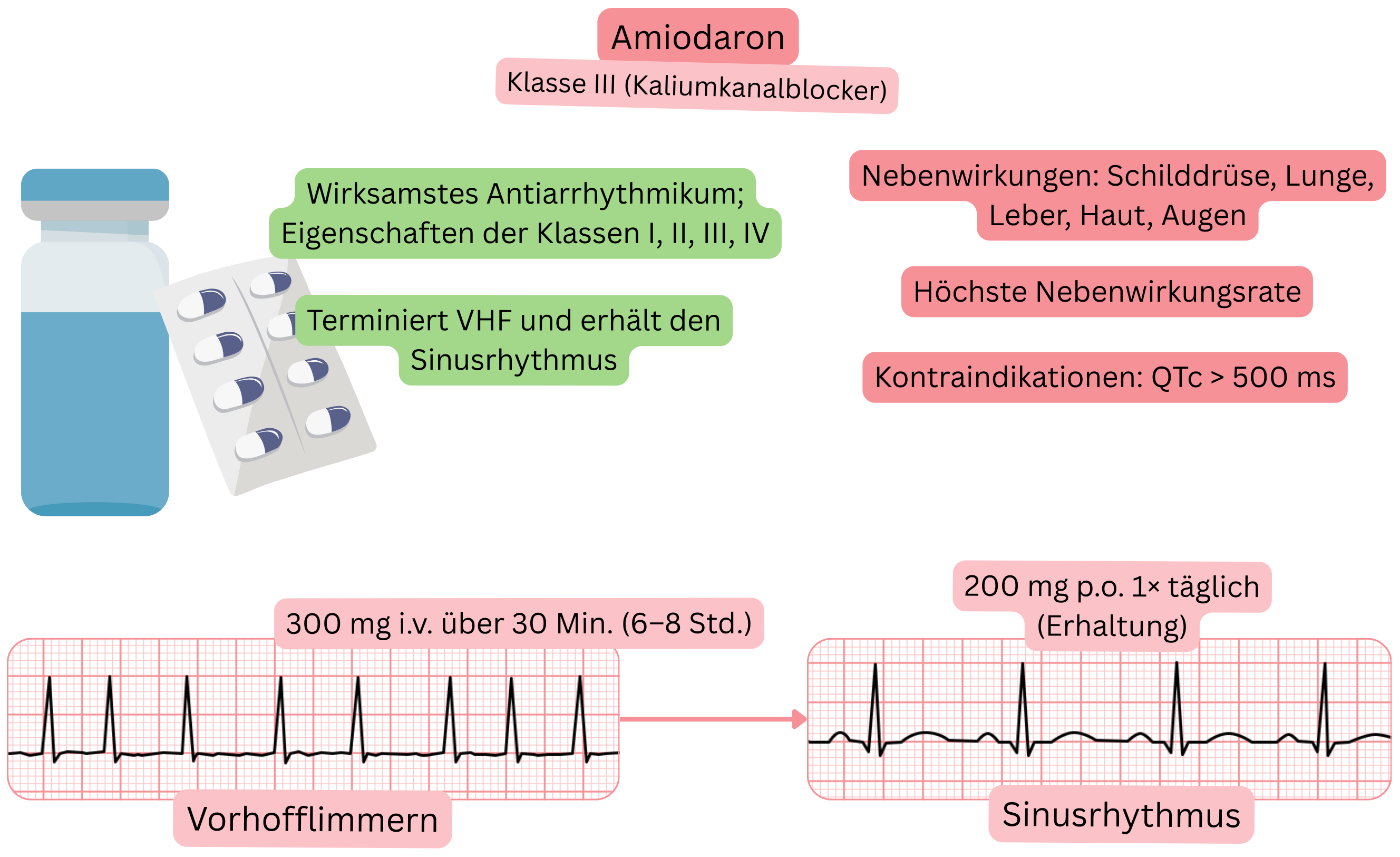
Wirkmechanismus:
Effekt bei VHF:
Verteilungsvolumen von Amiodaron
| Grundlegende Eigenschaften von Amiodaron | |
|---|---|
| Eigenschaft | Erläuterung |
| Wirkbeginn | 7–21 Tage (oral) |
| Langzeiteffekt | Wird erst nach Aufsättigung von ~10 g (intravenös + oral) deutlich |
| Halbwertszeit | ~50 Tage (oral) |
| Wirkung nach Absetzen | 2–3 Monate |
| Dosisanpassungen | Werden verzögert wirksam (Wochen) |
Amiodaron-Aufladung (10 g)
| Amiodaron und Vorhofflimmern (VHF) |
|---|
| Handelsnamen |
| Cordarone, Amiodaron, Amiohexal, Amiokordin, Aratac, Acrodarona |
| Indikationen |
|
| Dosierung |
|
| Wirkbeginn |
|
| Wirkung |
Zeit bis zur Konversion in den Sinusrhythmus und Erfolgsrate
|
| Wirkdauer |
|
| Kontraindikationen |
|
Patientenüberwachung vor und nach Beginn von Amiodaron:
| Patientenüberwachung vor und während einer Amiodarontherapie | ||
|---|---|---|
| Zeitpunkt | Zu kontrollieren | Grund für Therapieabbruch |
| Vor Beginn |
EKG (QTc-Intervall, AV-Block) Schilddrüsenfunktion (TSH, fT4) Leberwerte (ALT, AST, GGT, ALP, Bilirubin) Elektrolyte (Na, K, Mg) Thoraxröntgen oder HRCT Spirometrie Ophthalmologische Untersuchung Klinische Untersuchung (Haut, neurologischer Status) |
QTc > 500 ms AV-Block II. oder III. Grades Pathologische Leberwerte Hypothyreose oder Hyperthyreose Schwere Elektrolytstörungen (insbesondere Hypokaliämie) Lungenfibrose oder Pneumonitis |
| Alle 6 Monate |
EKG (QTc-Intervall, AV-Block) Schilddrüsenfunktion (TSH, fT4) Leberwerte (ALT, AST, GGT, ALP, Bilirubin) Elektrolyte (Na, K, Mg) Klinische Untersuchung (Haut, neurologischer Status) |
QTc > 500 ms AV-Block II. oder III. Grades Husten, Dyspnoe, radiologische Auffälligkeiten Pathologische Leberwerte Sehstörungen (Hornhautablagerungen, Optikusneuropathie) Hautreaktionen (blaugraue Verfärbung, Photosensitivität) Schwere Elektrolytstörungen (insbesondere Hypokaliämie) |
| Alle 12 Monate |
Ophthalmologische Untersuchung Thoraxröntgen oder HRCT Spirometrie Klinische Untersuchung (Haut, neurologischer Status) |
Husten, Dyspnoe, radiologische Auffälligkeiten Sehstörungen (Hornhautablagerungen, Optikusneuropathie) Hautreaktionen (blaugraue Verfärbung, Photosensitivität) |
Amiodaron ist das wirksamste Antiarrhythmikum, ist jedoch aufgrund der Gewebeakkumulation mit der höchsten Rate an Nebenwirkungen assoziiert.
Nebenwirkungen – können nach 1–2 Monaten Amiodarontherapie auftreten:
Amiodaron und Dronedaron gehören beide zu den Antiarrhythmika der Klasse III, unterscheiden sich jedoch in ihren Eigenschaften.
| Amiodaron vs. Dronedaron und Vorhofflimmern | ||
|---|---|---|
| Eigenschaft | Amiodaron | Dronedaron |
| Wirksamkeit (Erhalt des SR) | 60–70 % nach 1 Jahr | 30–40 % nach 1 Jahr |
| Wirkbeginn | Langsam (Tage–Wochen, volle Wirkung nach Aufsättigung von ~10 g) | Schneller (3–6 Stunden) |
| Wirkdauer | Persistiert 2–3 Monate nach Absetzen | 12–24 Stunden (verschwindet nach Dosis-Auslassung) |
| Geeigneter Patient | Auch bei struktureller Herzerkrankung | Patient ohne strukturelle Herzerkrankung und mit erhaltener Ejektionsfraktion |
| Herzinsuffizienz | Kann eingesetzt werden (inkl. HFrEF) | Kontraindiziert (NYHA III–IV, HFrEF < 40 %) |
| Gewebeakkumulation | Ja – Fettgewebe, Lunge, Auge, Schilddrüse | Minimal |
| Lunge (Toxizität) | Lungenfibrose, interstitielle Pneumonitis | Keine pulmonale Toxizität |
| Leber (Toxizität) | Leichte Hepatotoxizität, erhöhte Leberenzyme | Mögliche schwere Hepatitis, Leberversagen |
| Schilddrüse (Toxizität) | Hypothyreose und Hyperthyreose | Kein Effekt auf die Schilddrüse |
| Augen (Toxizität) | Hornhautablagerungen, Optikusneuropathie | Keine okulare Toxizität |
| Haut (Toxizität) | Photosensitivität, blaugraue Hautverfärbung | Hautausschlag, Pruritus |
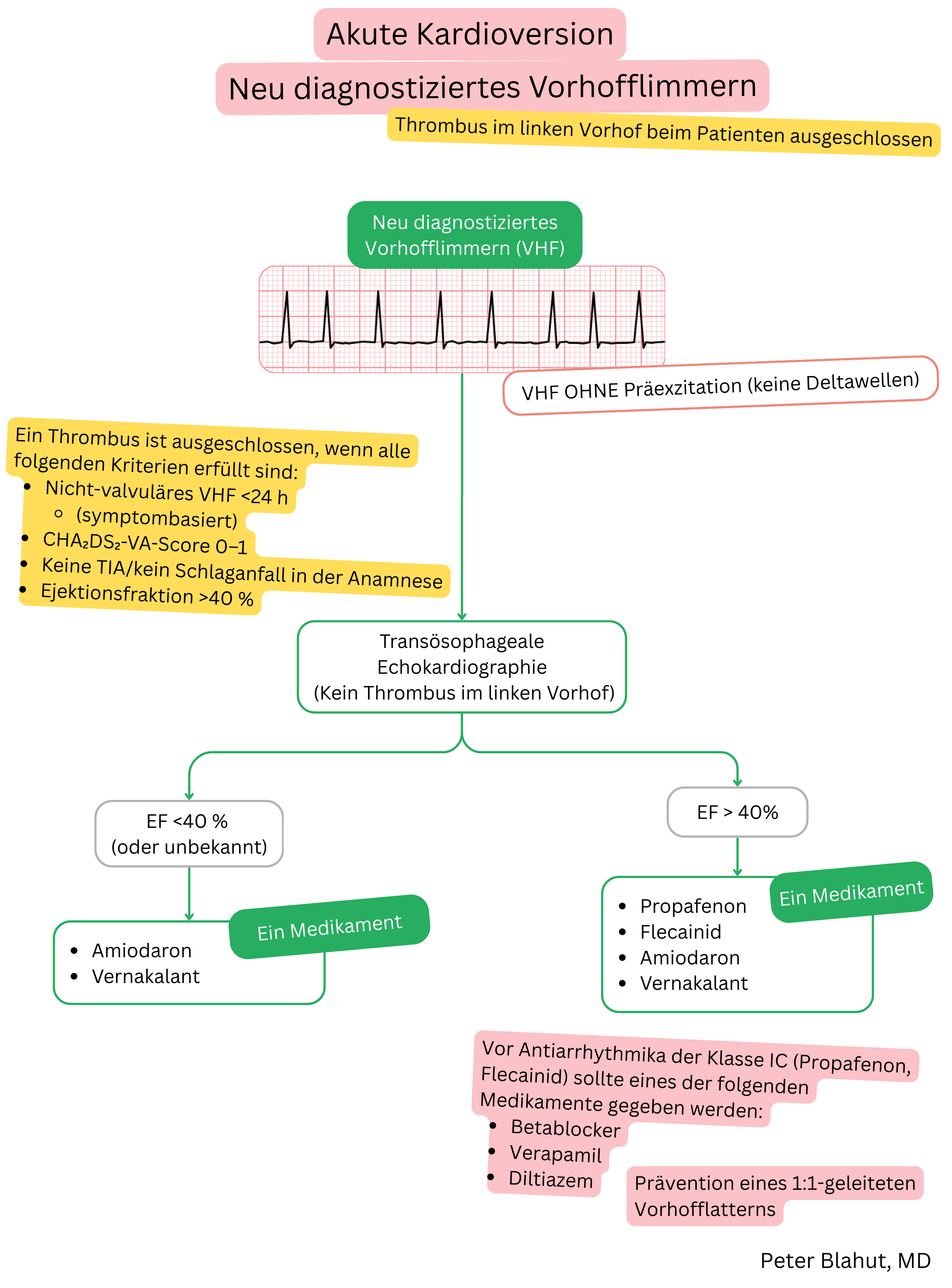
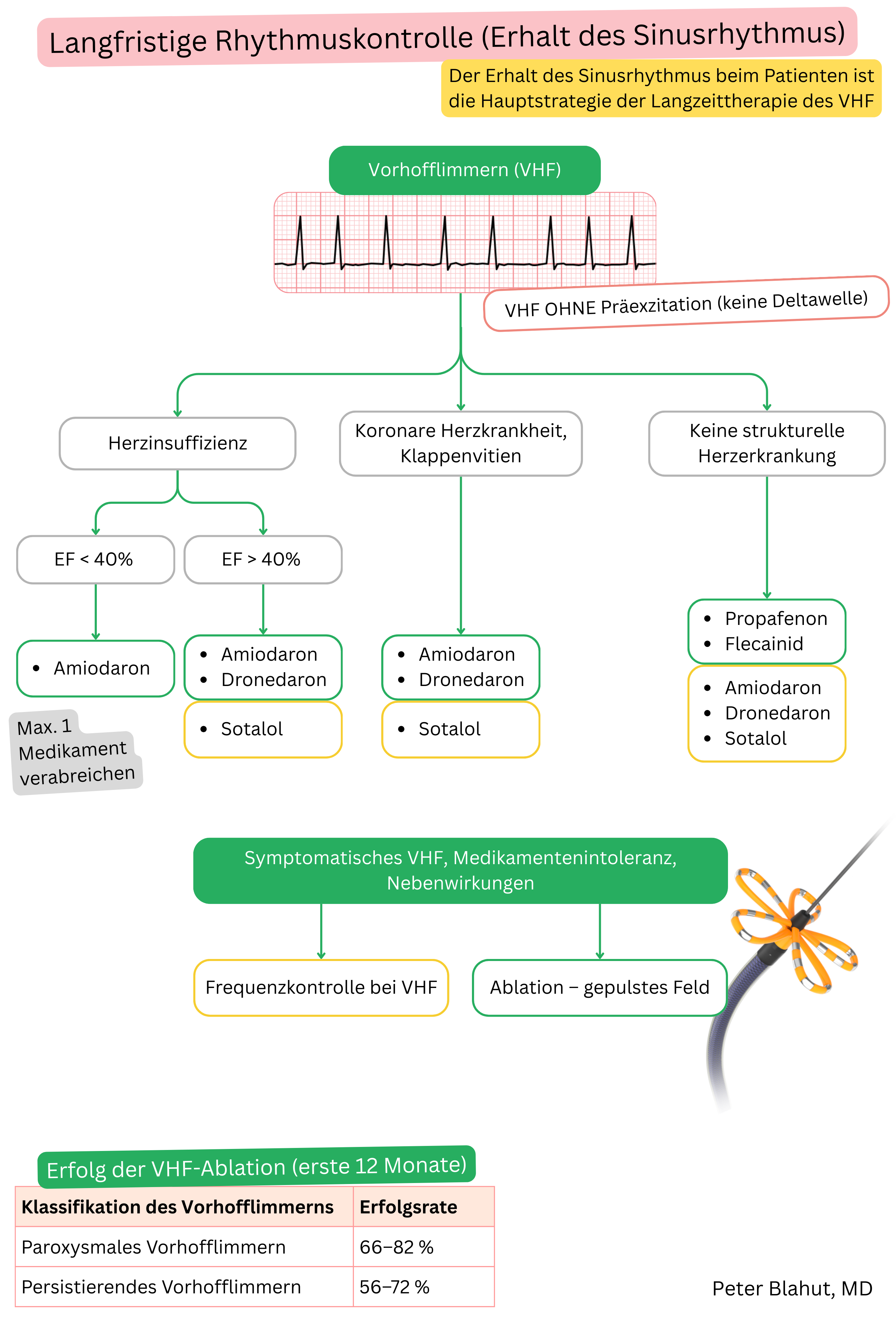
Diese Leitlinien sind inoffiziell und stellen keine offiziellen Leitlinien dar, die von einer kardiologischen Fachgesellschaft herausgegeben wurden. Sie dienen ausschließlich zu Bildungs- und Informationszwecken.
