

Classification :
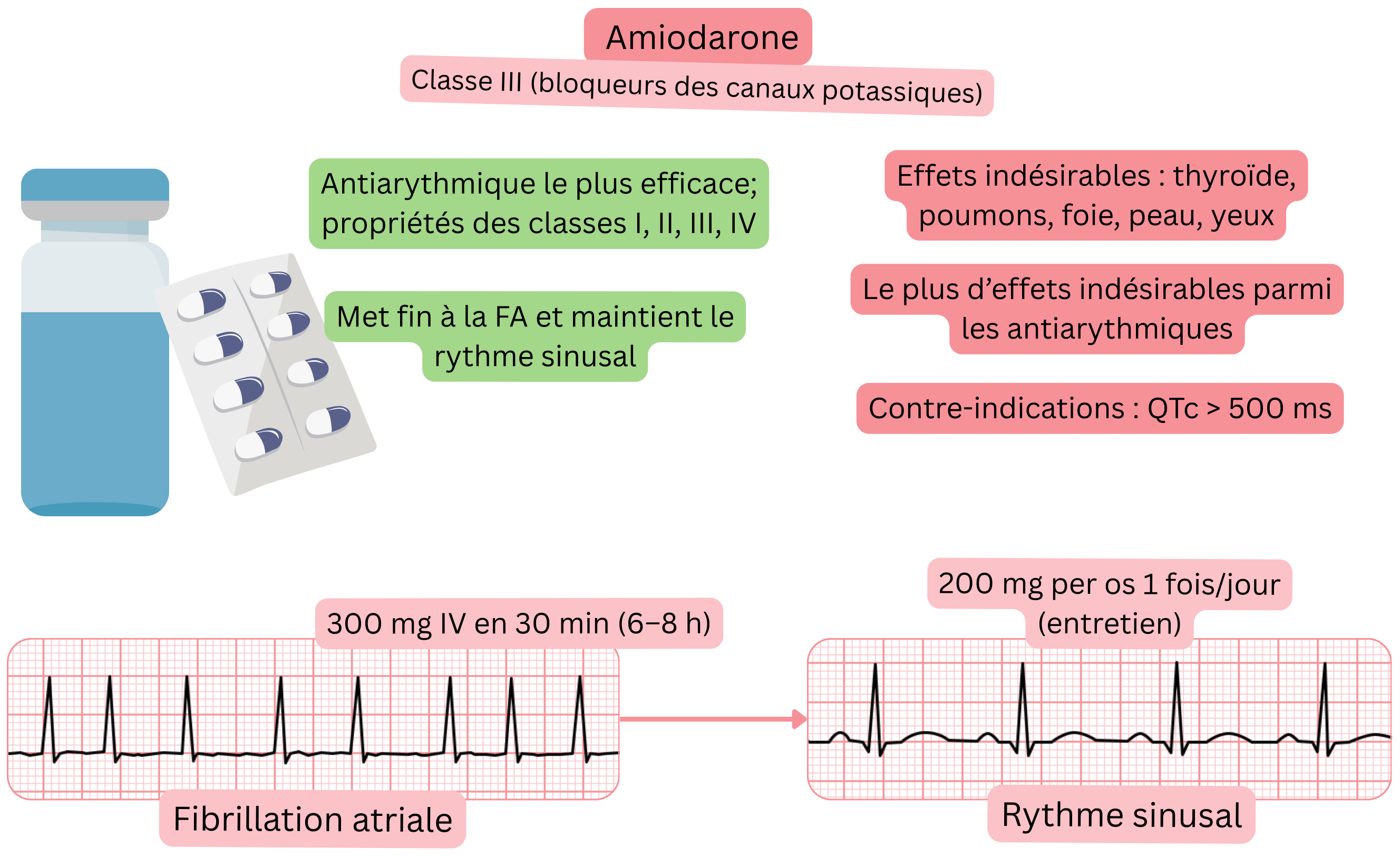
Mécanisme :
Effet sur la FA :
Volume de distribution de l’amiodarone
| Propriétés de base de l’amiodarone | |
|---|---|
| Propriété | Explication |
| Délai d’action | 7–21 jours (oral) |
| Effet à long terme | Ne devient apparent qu’après une dose de charge d’environ 10 g (intraveineux + oral) |
| Demi-vie | ~50 jours (oral) |
| Effet après arrêt | 2–3 mois |
| Ajustements posologiques | Deviennent apparents avec délai (semaines) |
Charge en amiodarone (10 g)
| Amiodarone et fibrillation atriale (FA) |
|---|
| Noms commerciaux |
| Cordarone, Amiodaron, Amiohexal, Amiokordin, Aratac, Acrodarona |
| Indications |
|
| Posologie |
|
| Délai d’action |
|
| Effet |
Délai de conversion en rythme sinusal et taux de succès
|
| Durée d’action |
|
| Contre-indications |
|
Surveillance du patient avant et après initiation de l’amiodarone :
| Surveillance du patient avant et pendant un traitement par amiodarone | ||
|---|---|---|
| Moment | Éléments à surveiller | Motif d’arrêt du traitement |
| Avant initiation |
ECG (intervalle QTc, bloc AV) Fonction thyroïdienne (TSH, fT4) Bilan hépatique (ALAT, ASAT, GGT, PAL, bilirubine) Électrolytes (Na, K, Mg) Radiographie thoracique ou HRCT Spirométrie Examen ophtalmologique Examen clinique (peau, statut neurologique) |
QTc > 500 ms Bloc AV du IIe ou IIIe degré Anomalies du bilan hépatique Hypothyroïdie ou hyperthyroïdie Troubles électrolytiques sévères (en particulier hypokaliémie) Fibrose pulmonaire ou pneumopathie interstitielle |
| Tous les 6 mois |
ECG (intervalle QTc, bloc AV) Fonction thyroïdienne (TSH, fT4) Bilan hépatique (ALAT, ASAT, GGT, PAL, bilirubine) Électrolytes (Na, K, Mg) Examen clinique (peau, statut neurologique) |
QTc > 500 ms Bloc AV du IIe ou IIIe degré Toux, dyspnée, anomalies radiographiques Anomalies du bilan hépatique Troubles visuels (dépôts cornéens, neuropathie optique) Réactions cutanées (décoloration bleu-gris, photosensibilité) Troubles électrolytiques sévères (en particulier hypokaliémie) |
| Tous les 12 mois |
Examen ophtalmologique Radiographie thoracique ou HRCT Spirométrie Examen clinique (peau, statut neurologique) |
Toux, dyspnée, anomalies radiographiques Troubles visuels (dépôts cornéens, neuropathie optique) Réactions cutanées (décoloration bleu-gris, photosensibilité) |
L’amiodarone est l’antiarythmique le plus efficace mais est associée au taux le plus élevé d’effets indésirables en raison de son accumulation tissulaire.
Effets indésirables – peuvent survenir après 1–2 mois de traitement par amiodarone :
L’amiodarone et la dronédarone appartiennent toutes deux à la classe III des antiarythmiques mais diffèrent par leurs propriétés.
| Amiodarone vs dronédarone et fibrillation atriale | ||
|---|---|---|
| Propriété | Amiodarone | Dronédarone |
| Efficacité (maintien du RS) | 60–70 % à 1 an | 30–40 % à 1 an |
| Délai d’action | Lent (jours–semaines, effet complet après charge d’environ 10 g) | Plus rapide (3–6 heures) |
| Durée d’action | Persiste 2–3 mois après l’arrêt | 12–24 heures (disparaît en cas d’oubli de dose) |
| Patient adapté | Aussi en cas de cardiopathie structurelle | Patient sans cardiopathie structurelle et avec fraction d’éjection préservée |
| Insuffisance cardiaque | Peut être utilisé (y compris HFrEF) | Contre-indiquée (NYHA III–IV, HFrEF < 40 %) |
| Accumulation tissulaire | Oui – tissu adipeux, poumons, œil, glande thyroïde | Minimale |
| Poumons (toxicité) | Fibrose pulmonaire, pneumopathie interstitielle | Aucune toxicité pulmonaire |
| Foie (toxicité) | Hépatotoxicité modérée, augmentation des enzymes hépatiques | Hépatite sévère possible, insuffisance hépatique |
| Thyroïde (toxicité) | Hypothyroïdie et hyperthyroïdie | Aucun effet sur la glande thyroïde |
| Yeux (toxicité) | Dépôts cornéens, neuropathie optique | Aucune toxicité oculaire |
| Peau (toxicité) | Photosensibilité, décoloration cutanée bleu-gris | Éruption cutanée, prurit |
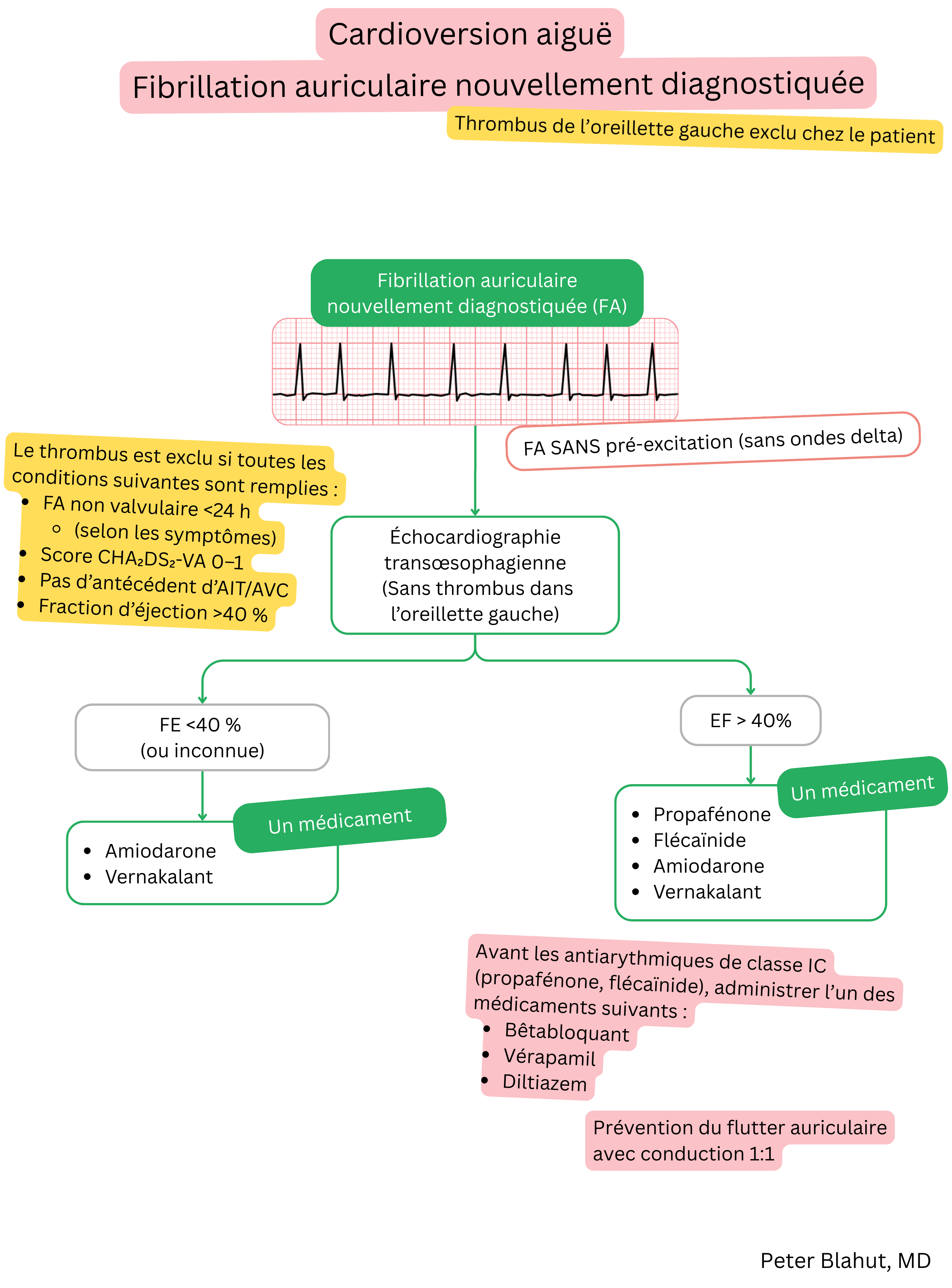
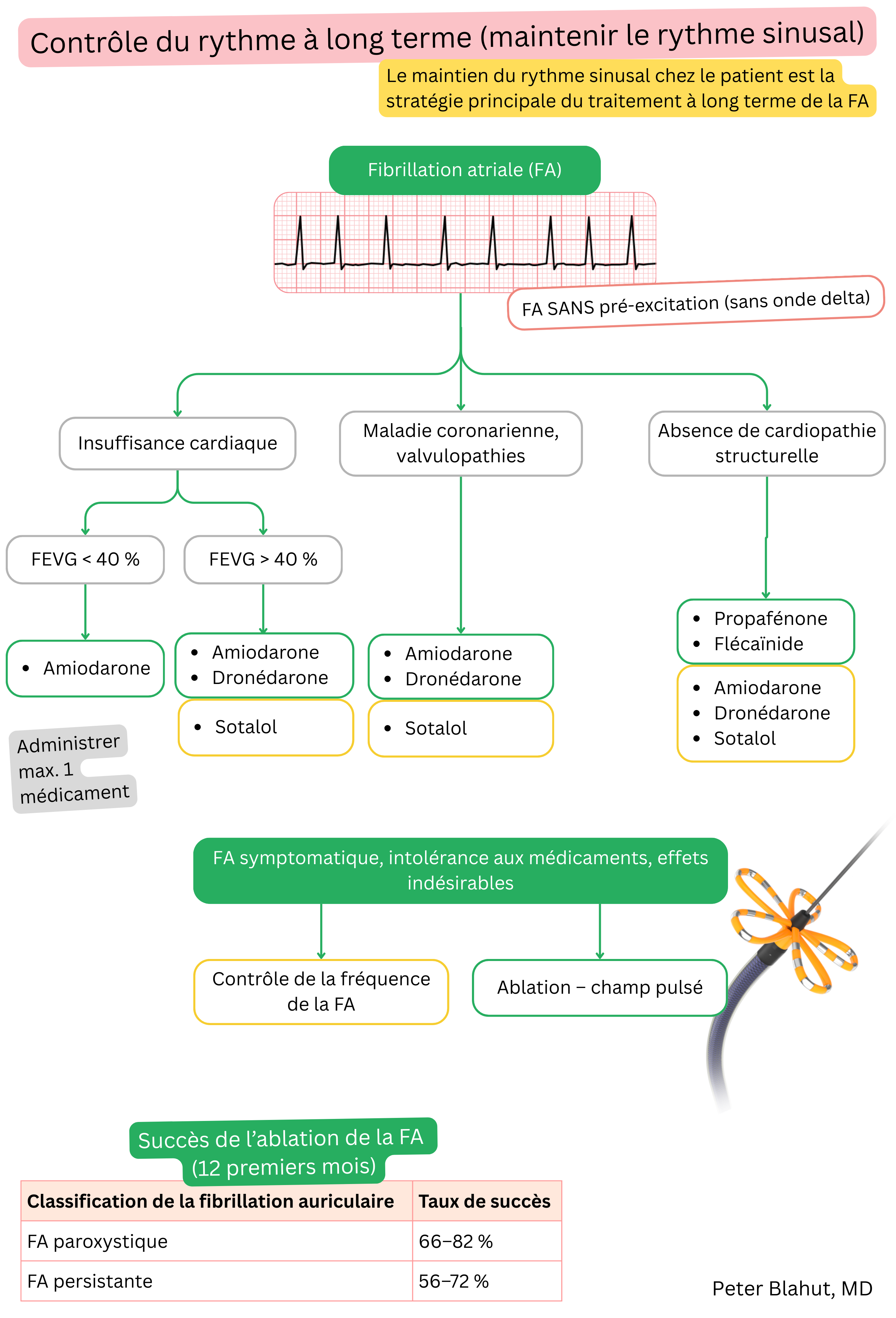
Ces recommandations sont non officielles et ne représentent pas des recommandations formelles émises par une société professionnelle de cardiologie. Elles sont destinées uniquement à des fins éducatives et informatives.
