

L’intérêt de la rythmologie pour les cardiopathies structurelles et les antiarythmiques de Classe IC
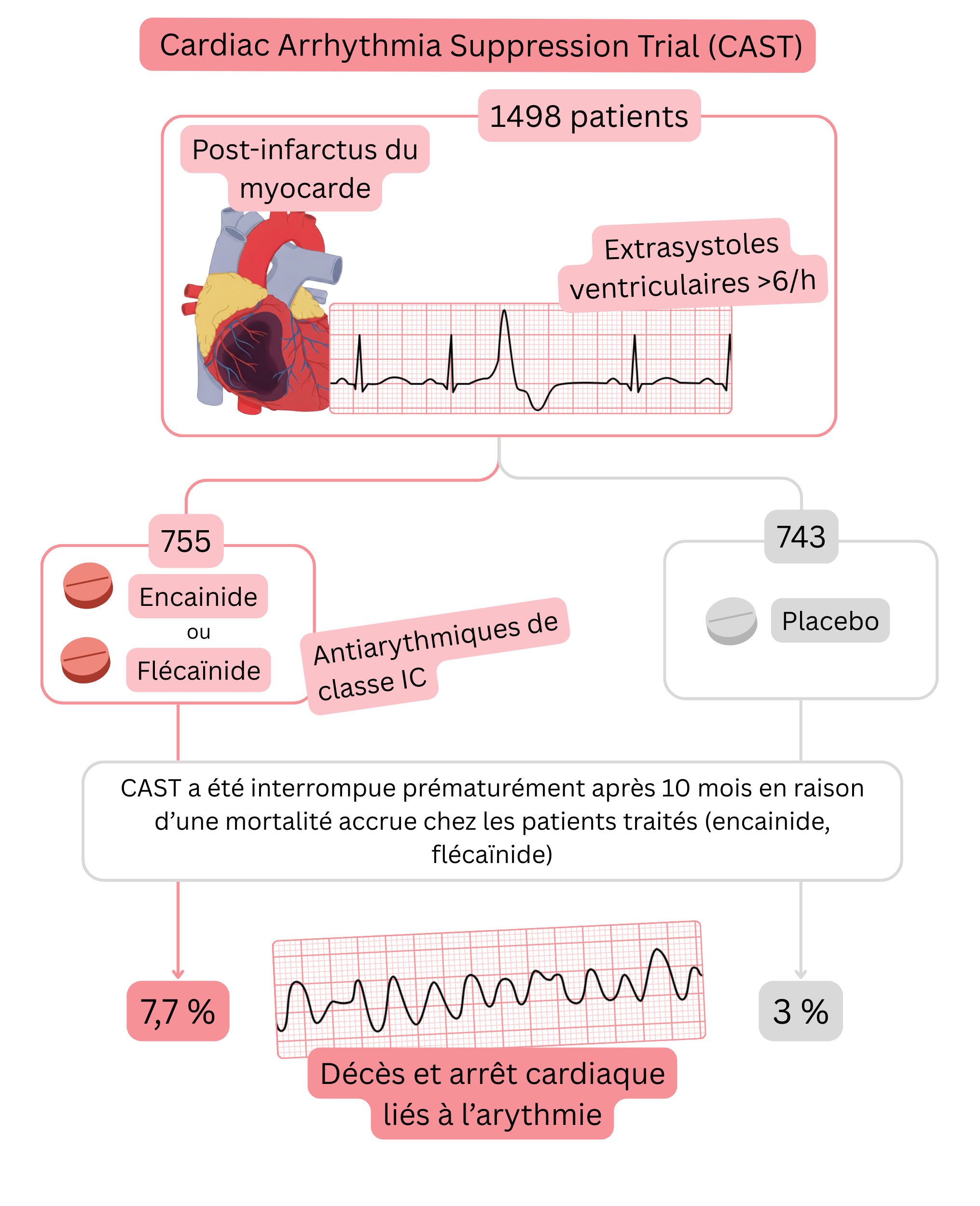
Essai CAST
Résumé de l’essai CAST :
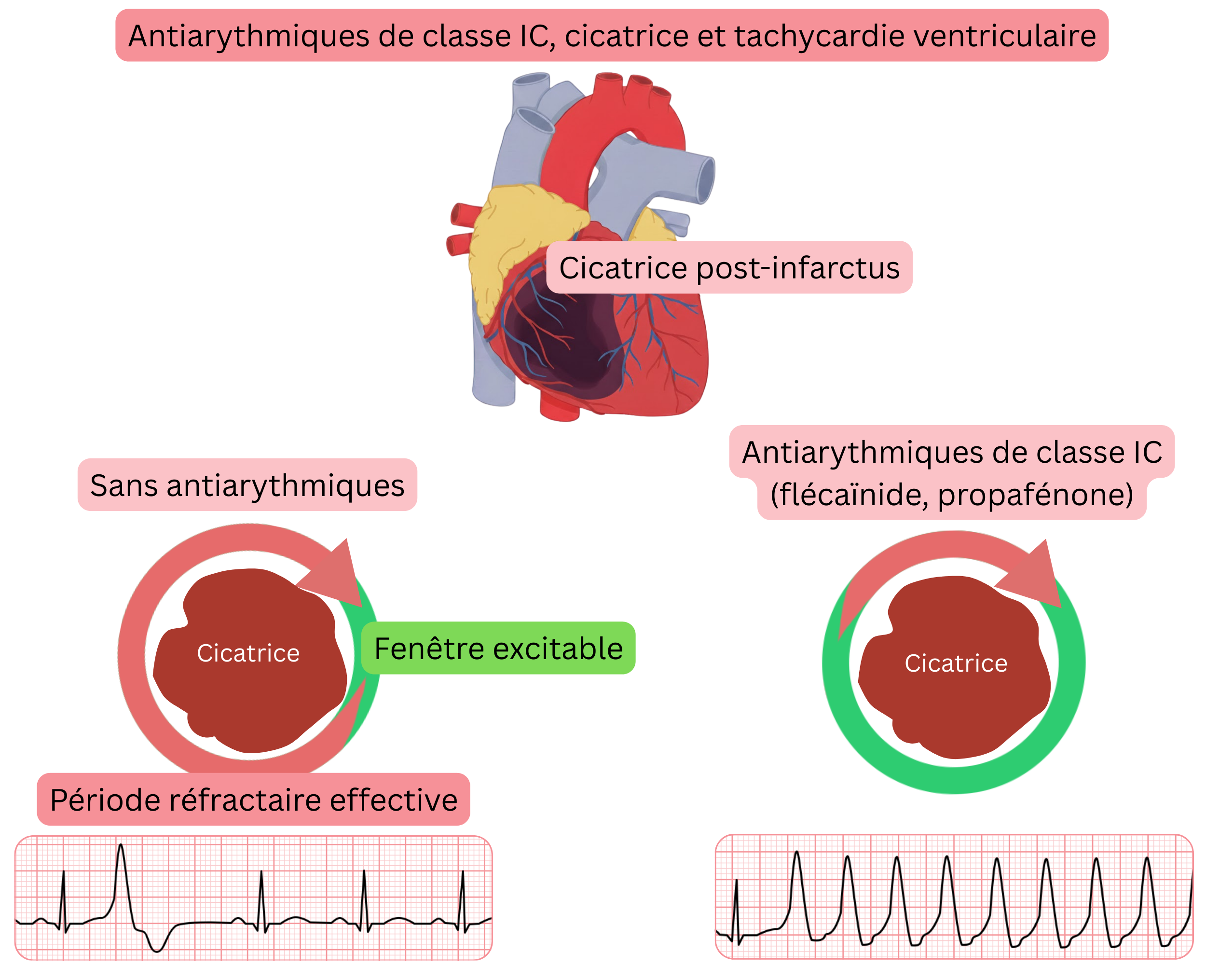
Mécanisme des arythmies ventriculaires dans l’essai CAST
Extension des conclusions de l’essai CAST à la pratique clinique
Cardiopathie structurelle
| Cardiopathie structurelle |
|---|
| Antécédent d’infarctus du myocarde |
| Maladie coronarienne |
| Fraction d’éjection (<40 %) |
| Hypertrophie ventriculaire gauche (>15 mm) |
| Cardiomyopathie (dilatée, hypertrophique, restrictive, infiltrative) |
| Valvulopathie – sténose ou insuffisance (modérée ou sévère) |
| Insuffisance cardiaque (NYHA II–IV, hospitalisation pour insuffisance cardiaque) |
| Statut post-chirurgie cardiaque |
Dans le tableau suivant, vous pouvez revoir les méthodes diagnostiques de base et les paramètres utilisés pour diagnostiquer une cardiopathie structurelle.
| Cardiopathie structurelle (diagnostic) | |
|---|---|
| Diagnostic | Examens |
| Antécédent d’infarctus du myocarde |
ECG : ondes Q pathologiques (≥ 40 ms, ≥ 25 % du QRS, ≥ 2 dérivations) Écho : anomalie segmentaire de cinétique (akinésie, dyskinésie) IRM : cicatrice (rehaussement tardif LGE positif) |
| Maladie coronarienne (IHD) |
Angioscanner coronaire : sténose > 50 % tronc commun, > 70 % autres grosses branches Épreuve d’effort : sous-décalage ST > 1 mm à l’effort = ischémie |
| Fraction d’éjection (< 40 %) |
Écho : FE < 40 % IRM : FE < 40 % |
| Hypertrophie ventriculaire gauche |
ECG : index de Sokolow–Lyon > 35 mm Écho : épaisseur pariétale > 15 mm |
| Cardiomyopathie |
Dilatée : LVEDD > 55 mm + FE < 40 % (écho/IRM) Hypertrophique : paroi VG ≥ 15 mm (écho/IRM) Restrictive : dilatation bi-auriculaire + dysfonction diastolique (E/e´ > 15) Infiltrative : écho – myocarde granité ; IRM – LGE diffus |
| Valvulopathie (sténose / insuffisance) | Écho : sténose ou insuffisance (modérée ou sévère) |
| Insuffisance cardiaque (NYHA II–IV) |
Clinique : dyspnée d’effort ou de repos, œdèmes, orthopnée, hospitalisations répétées Écho : FE < 40 % (HFrEF) ou dysfonction diastolique significative (HFpEF / HFmrEF) BNP > 35 pg/ml ou NT-proBNP > 125 pg/ml |
| Statut post-chirurgie cardiaque | Antécédents : chirurgie documentée (PAC, chirurgie valvulaire, cardiopathie congénitale) |
Dans le tableau suivant, vous pouvez revoir les investigations et les critères qui doivent être remplis pour l’administration sûre des antiarythmiques de Classe IC chez les patients présentant une fibrillation atriale (FA).
| Critères d’administration des antiarythmiques de Classe IC dans la fibrillation atriale | |
|---|---|
| Examen | Critères |
| ECG |
Absence d’ondes Q pathologiques (≥ 40 ms, ≥ 25 % du QRS, ≥ 2 dérivations) Absence d’hypertrophie : index de Sokolow–Lyon ≤ 35 mm (S en V1 + R en V5 ou V6) QRS < 120 ms (pas de bloc de branche) QTc selon le sexe : hommes < 450 ms, femmes < 470 ms |
| Échocardiographie |
Fraction d’éjection (FE) ≥ 40 % Épaisseur pariétale ≤ 15 mm Absence de dilatation : LVEDD < 55 mm, OG < 40 mm ou < 34 ml/m² Valves : au maximum insuffisance ou sténose légère |
| Épreuve d’effort |
Négative pour l’ischémie Absence d’arythmies induites Absence de chute de la pression artérielle systolique > 10 mmHg à l’effort |
| Coronarographie / angioscanner / IRM |
Indiquée en cas de suspicion clinique de cardiopathie ischémique ou de cardiomyopathie Une sténose coronaire significative, une cicatrice post-infarctus ou une cardiomyopathie doivent être exclues |
Ces recommandations sont non officielles et ne représentent pas des recommandations formelles émises par une société professionnelle de cardiologie. Elles sont destinées uniquement à des fins éducatives et informatives.
