

El interés de la arritmología en la cardiopatía estructural y los fármacos antiarrítmicos de Clase IC
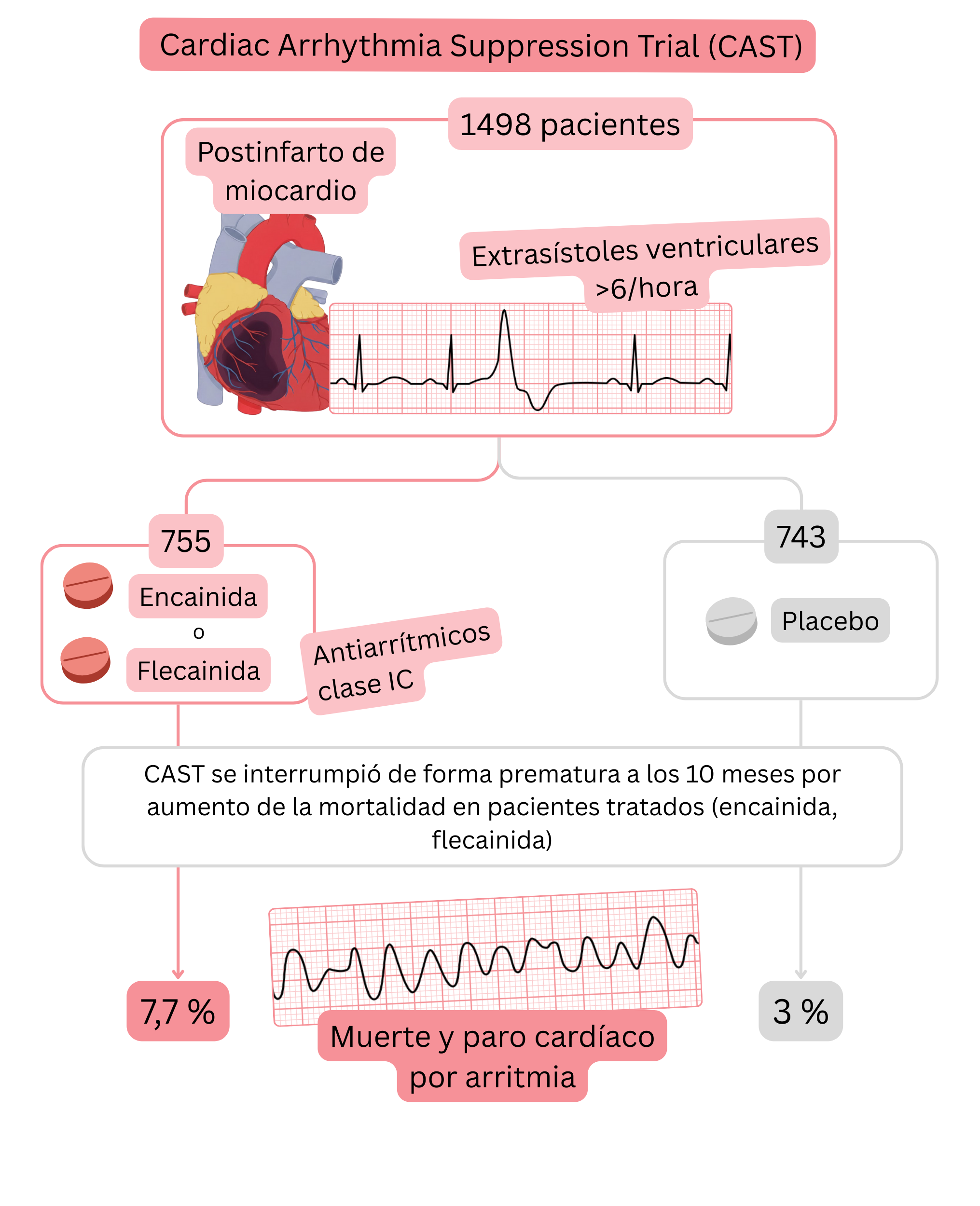
Ensayo CAST
Resumen del ensayo CAST:
Mecanismo de arritmia ventricular en el ensayo CAST
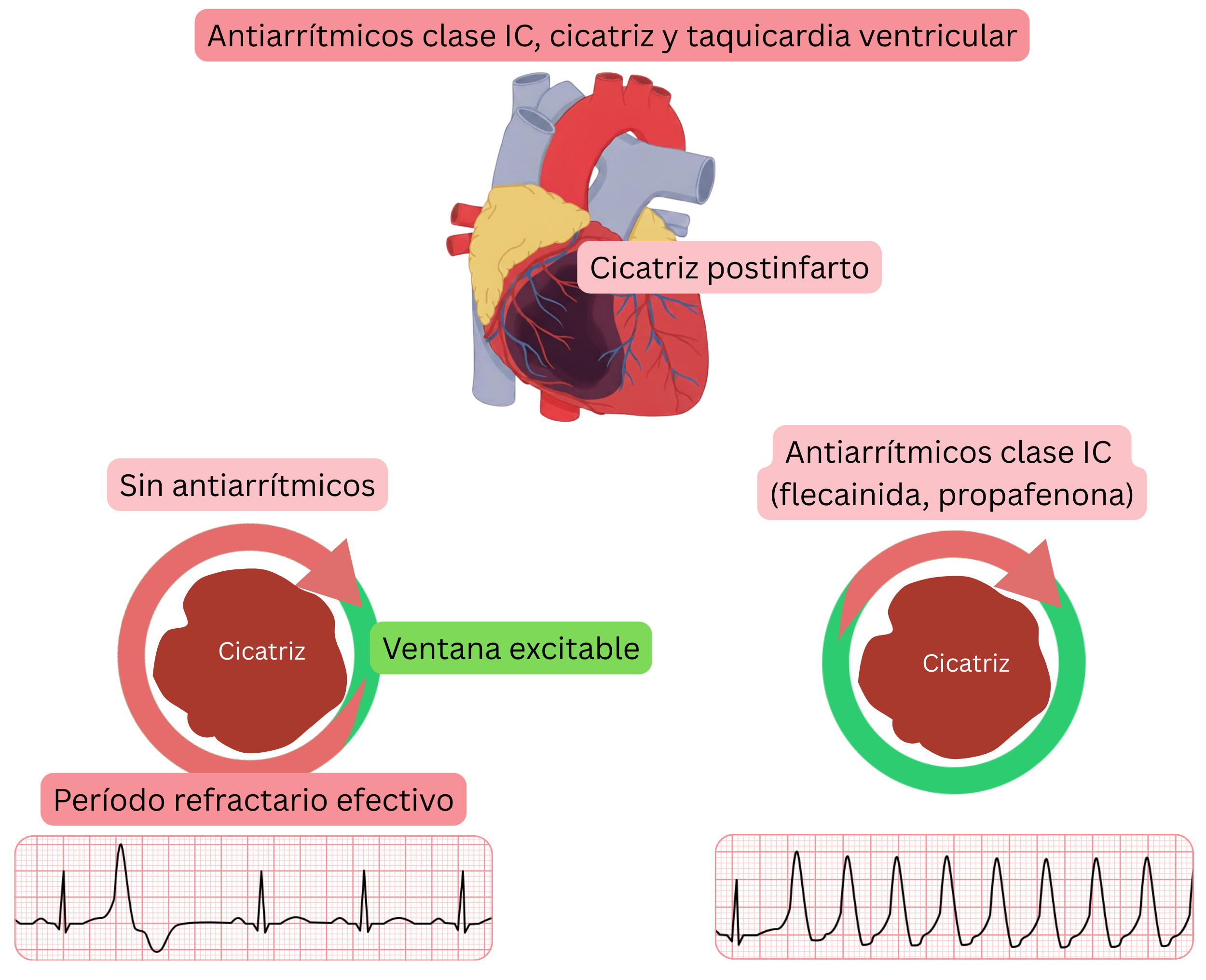
Extensión de las conclusiones del ensayo CAST a la práctica clínica
Cardiopatía estructural
| Cardiopatía estructural |
|---|
| Infarto de miocardio previo |
| Enfermedad coronaria |
| Fracción de eyección (<40 %) |
| Hipertrofia ventricular izquierda (>15 mm) |
| Miocardiopatía (dilatada, hipertrófica, restrictiva, infiltrativa) |
| Valvulopatía – estenosis o regurgitación (moderada o grave) |
| Insuficiencia cardíaca (NYHA II–IV, hospitalización por insuficiencia cardíaca) |
| Estado poscirugía cardíaca |
En la siguiente tabla, puede revisar los métodos diagnósticos y parámetros básicos utilizados para diagnosticar cardiopatía estructural.
| Cardiopatía estructural (diagnóstico) | |
|---|---|
| Diagnóstico | Diagnóstico |
| Infarto de miocardio previo |
ECG: ondas Q patológicas (≥ 40 ms, ≥ 25 % del QRS, ≥ 2 derivaciones) Ecocardiografía: alteración segmentaria de la contractilidad (acinesia, discinesia) RM: cicatriz (hallazgo positivo de RTG) |
| Enfermedad coronaria (IHD) |
Angiografía coronaria por TC: estenosis > 50 % en tronco común izquierdo, > 70 % en otras ramas principales Prueba de esfuerzo: descenso del ST > 1 mm durante el esfuerzo = isquemia |
| Fracción de eyección (< 40 %) |
Ecocardiografía: FE < 40 % RM: FE < 40 % |
| Hipertrofia ventricular izquierda |
ECG: índice de Sokolow–Lyon > 35 mm Ecocardiografía: grosor parietal > 15 mm |
| Miocardiopatía |
Dilatada: DDVI > 55 mm + FE < 40 % (eco/RM) Hipertrófica: pared del VI ≥ 15 mm (eco/RM) Restrictiva: dilatación biauricular + disfunción diastólica (E/e´ > 15) Infiltrativa: ecocardiografía – miocardio moteado; RM – RTG difuso |
| Valvulopatía (estenosis / regurgitación) | Ecocardiografía: estenosis o regurgitación (moderada o grave) |
| Insuficiencia cardíaca (NYHA II–IV) |
Clínica: disnea con el esfuerzo o en reposo, edema, ortopnea, hospitalizaciones recurrentes Ecocardiografía: FE < 40 % (IC-FEr) o disfunción diastólica significativa (IC-FEc / IC-FElr) BNP > 35 pg/ml o NT-proBNP > 125 pg/ml |
| Estado poscirugía cardíaca | Antecedentes: cirugía documentada (CABG, cirugía valvular, defecto congénito) |
En la siguiente tabla, puede revisar las exploraciones y criterios que deben cumplirse para la administración segura de fármacos antiarrítmicos de Clase IC en pacientes con fibrilación auricular (FA).
| Criterios para la administración de fármacos antiarrítmicos de Clase IC en la fibrilación auricular | |
|---|---|
| Exploración | Criterios |
| ECG |
Sin ondas Q patológicas (≥ 40 ms, ≥ 25 % del QRS, ≥ 2 derivaciones) Sin hipertrofia: índice de Sokolow–Lyon ≤ 35 mm (S en V1 + R en V5 o V6) QRS < 120 ms (sin bloqueo de rama) QTc según sexo: varones < 450 ms, mujeres < 470 ms |
| Ecocardiografía |
Fracción de eyección (FE) ≥ 40 % Grosor parietal ≤ 15 mm Sin dilatación: DDVI < 55 mm, AI < 40 mm o < 34 ml/m² Válvulas: como máximo regurgitación o estenosis leves |
| Prueba de esfuerzo |
Negativa para isquemia Sin arritmias inducidas Sin descenso de la presión arterial sistólica > 10 mmHg durante el ejercicio |
| CAG / CTA / RM |
Indicadas ante sospecha clínica de cardiopatía isquémica o miocardiopatía Deben excluirse estenosis coronaria significativa, cicatriz posinfarto o miocardiopatía |
Estas guías son no oficiales y no representan guías formales emitidas por ninguna sociedad profesional de cardiología. Están destinadas únicamente a fines educativos e informativos.
