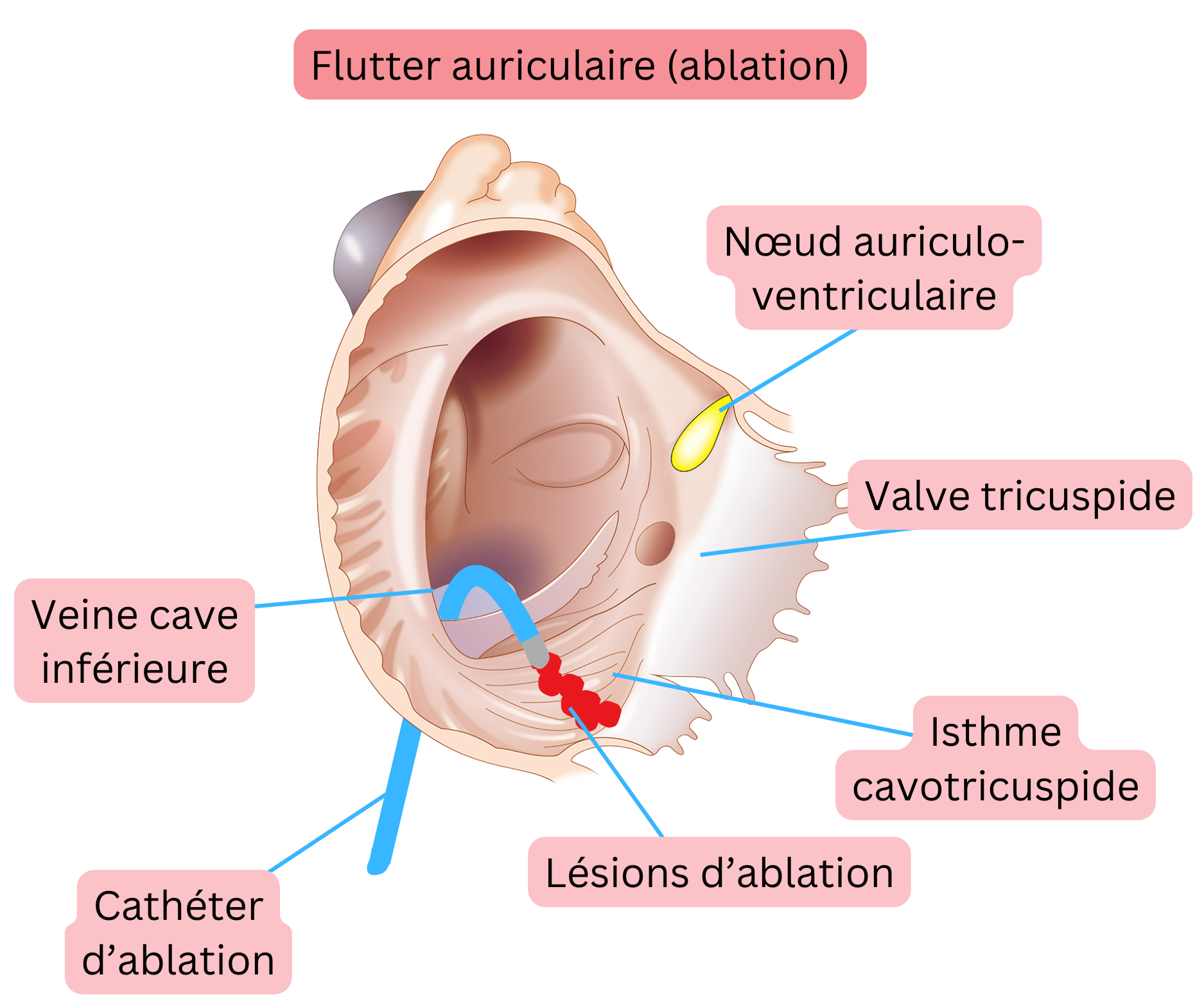
Le flutter atrial (AFl) partage les mêmes facteurs de risque que la fibrillation atriale (FA). Dans des oreillettes remodelées, le plus souvent dans l’oreillette droite, un circuit de réentrée se développe le long duquel l’impulsion électrique peut circuler, le plus souvent à une fréquence de 240–300/min.
Pour que l’impulsion commence à circuler dans un circuit de réentrée, un facteur déclenchant est nécessaire ; les plus fréquents sont :
- extrasystole atriale
- FA (épisode court)
20 % des patients atteints de FA présentent également un AFl (typique ou atypique).
Chez 50 % des patients atteints d’AFl, une FA se développe ultérieurement.
Le risque thromboembolique dans l’AFl est identique à celui de la FA :
- ainsi, le traitement anticoagulant dans l’AFl est instauré comme dans la FA, selon le score CHA2DS2-VA.
L’AFl est classé selon la localisation du circuit de réentrée et le sens de rotation de l’impulsion en :
- AFl typique
- AFl typique antihoraire (CCW – Counter-Clockwise)
- AFl typique horaire (CW – Clockwise)
- AFl atypique
L’AFl est présent chez 1 % de la population, dont :
- AFl typique antihoraire (80 %)
- AFl typique horaire (10 %)
- AFl atypique (10 %)
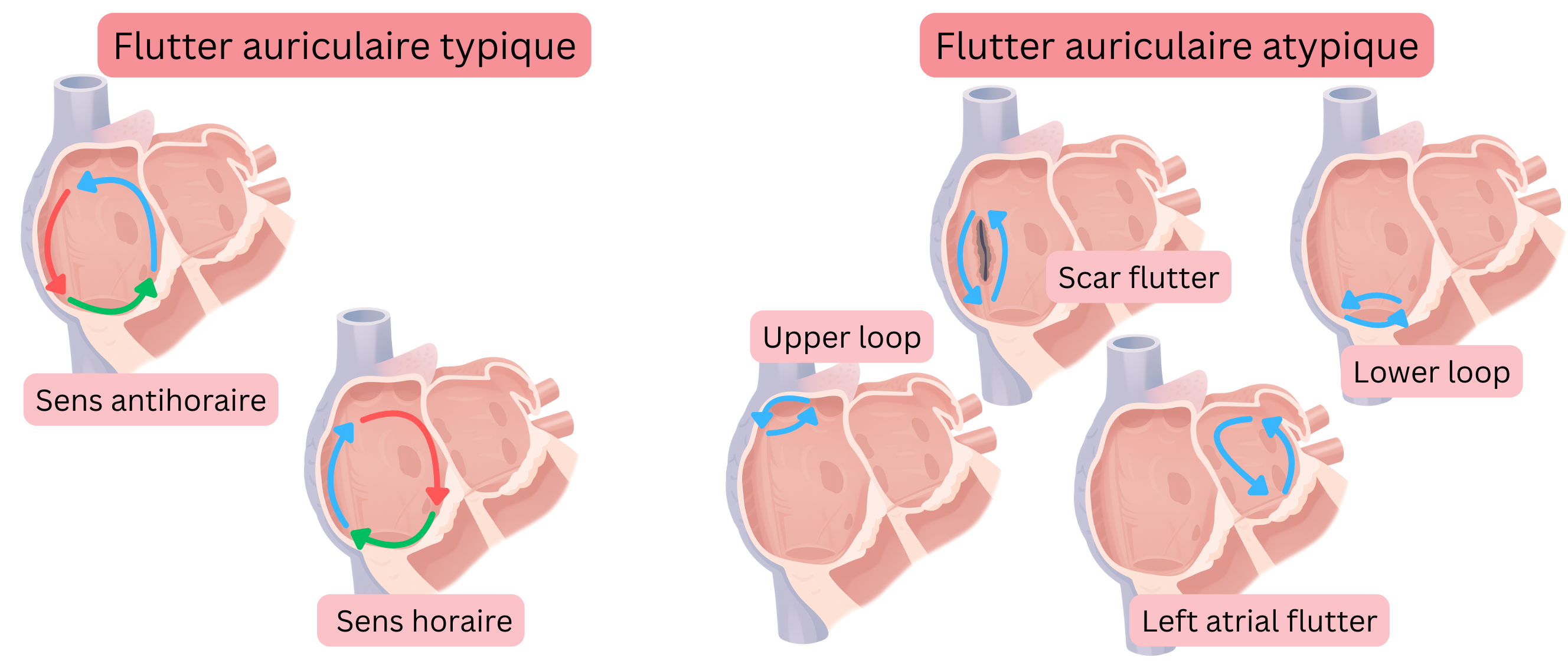
L’AFl typique signifie que le circuit de réentrée est situé dans l’oreillette droite et évolue comme suit :
- Descend le long de la paroi libre de l’oreillette droite (en avant de la crista terminalis)
- Traverse l’isthme cavotricuspide (CTI)
- Remonte le long du septum interauriculaire
- Puis traverse le toit de l’oreillette droite pour revenir à la paroi libre de l’oreillette droite.
- Le diamètre du circuit de réentrée est d’environ 3 cm, correspondant à une longueur de trajet d’environ 9 cm.
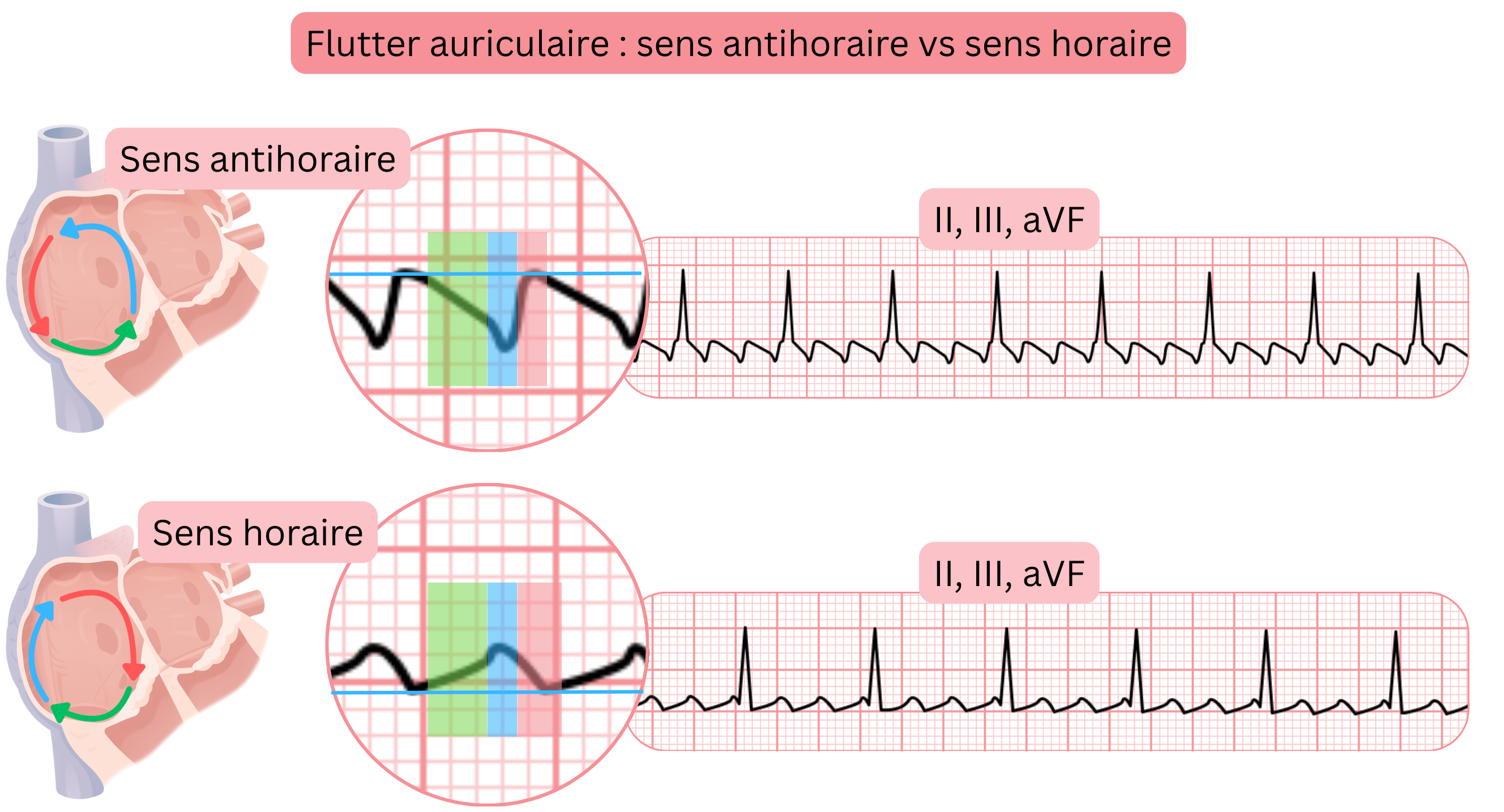
- Selon le sens de rotation de l’impulsion dans le circuit de réentrée, l’AFl typique est divisé en :
- AFl antihoraire (CCW)
- l’impulsion tourne dans le sens antihoraire
- AFl horaire (CW)
- l’impulsion tourne dans le sens horaire
L’AFl atypique signifie que le circuit de réentrée diffère de celui de l’AFl typique.
- Dans l’AFl atypique, la réentrée peut se produire dans n’importe quelle région anatomique de l’oreillette gauche ou droite.
- L’AFl atypique n’est pas classé selon le sens de rotation de l’impulsion.
- Le diamètre du circuit de réentrée dans l’AFl atypique est d’au moins 1 cm, correspondant à une longueur de trajet d’environ 3 cm.
L’AFl non bloqué signifie que le nœud AV commence à conduire les impulsions d’AFl vers les ventricules avec une conduction 1:1 (sans bloc).
- La fréquence ventriculaire résultante est de 240–300/min (le patient est hémodynamiquement instable).
- L’AFl non bloqué peut survenir :
- lors du traitement de la FA par des antiarythmiques de classe IC (Propafénone, Flécaïnide).
- Par conséquent, les antiarythmiques de classe IC sont administrés en association avec des médicaments ralentissant la conduction nodale AV (bêta-bloquants, Vérapamil, Diltiazem).
- Le risque d’AFl non bloqué est de 2–6 % :
- chez les patients atteints de FA ou d’AFl recevant des antiarythmiques de classe IC sans traitement freinant la conduction nodale AV,
- 20 % des patients atteints de FA présentent également un AFl pouvant ne pas être documenté à l’ECG.
Mécanisme de l’AFl non bloqué sous traitement par antiarythmiques de classe IC chez les patients atteints d’AFl :
- Les antiarythmiques de classe IC ralentissent la conduction dans le circuit de réentrée.
- Une impulsion circulant à environ 300/min est ralentie à 200–240/min.
- L’impulsion circule ainsi plus lentement dans le circuit de réentrée et, à chaque « tour », commence à être conduite aux ventricules via le nœud AV,
- car les impulsions atteignent le nœud AV à une fréquence permettant une conduction 1:1.
- À des fréquences plus élevées, les impulsions rencontrent la période réfractaire effective du nœud AV,
- et le nœud AV bloque la conduction, par exemple avec une conduction 2:1 ou 3:1.
Lors du traitement de la FA ou de l’AFl par des antiarythmiques de classe IC, un traitement freinant la conduction nodale AV doit toujours être co-administré :
- bêta-bloquants, Vérapamil ou Diltiazem,
- les médicaments freinant la conduction nodale AV préviennent la survenue d’un AFl 1:1 non bloqué.
Pour le traitement de l’AFl, l’ablation par radiofréquence est recommandée, car le traitement antiarythmique a un effet limité.
- Le principe du traitement pharmacologique de l’AFl est de ralentir la conduction de l’AFl à travers le nœud AV,
- afin que l’AFl soit conduit aux ventricules à une fréquence <100/min.
- Les médicaments freinant la conduction nodale AV sont utilisés : bêta-bloquants, Vérapamil, Diltiazem.
- Le traitement pharmacologique ne permet généralement pas d’interrompre le circuit de réentrée.
- Les antiarythmiques de classe IC ralentissent la réentrée sans l’interrompre ; il existe un risque d’AFl 1:1 non bloqué,
- ainsi, les antiarythmiques de classe IC sont toujours administrés en association avec des médicaments freinant la conduction nodale AV :
- bêta-bloquants, Vérapamil, Diltiazem.
| Flutter atrial et fibrillation atriale |
Classe |
| Le traitement anticoagulant dans le flutter atrial est indiqué selon le score CHA2DS2-VA. |
I |
| Pour le traitement du flutter atrial, l’ablation par radiofréquence est recommandée. |
I |
Lors du traitement de la fibrillation atriale par des antiarythmiques de classe IC (Propafénone, Flécaïnide), il est recommandé d’administrer également :
- des médicaments freinant la conduction nodale AV (bêta-bloquants, Vérapamil ou Diltiazem),
- afin de prévenir un flutter atrial 1:1 non bloqué
- (20 % des patients atteints de fibrillation atriale présentent également un flutter atrial).
|
I |