

L’accident vasculaire cérébral (AVC) peut être ischémique ou hémorragique.
| AVC – classification | |
|---|---|
| Type d’AVC | Proportion des cas (%) |
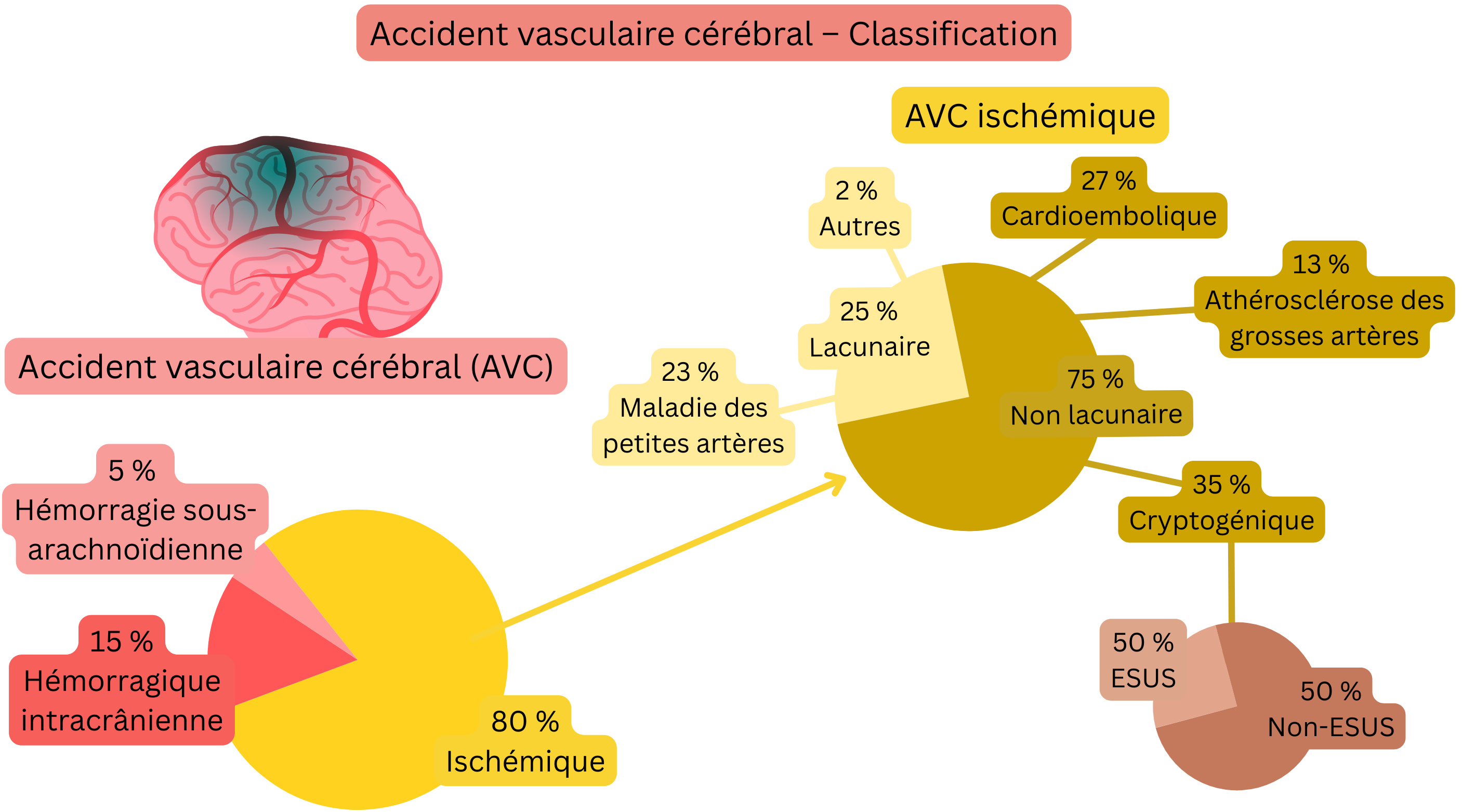
| Ischémique | 80 % |
| Hémorragique – intracrânien | 15 % |
| Hémorragique – sous-arachnoïdien | 5 % |
La prévalence globale de l’AVC ischémique est de 2–3 % (> 7 % dans la population > 65 ans).
Selon l’imagerie par TDM ou IRM, l’AVC ischémique peut être classé en :
| AVC ischémique | |||
|---|---|---|---|
| Type d’AVC | Lésion en TDM/IRM | Caractéristiques | Causes typiques |
| Lacunaire | < 15 mm (TDM) < 20 mm (IRM) |
Petite lésion sous-corticale |
Maladie des petites artérioles Hypertension artérielle Diabète sucré |
| Non lacunaire | > 15 mm (TDM) > 20 mm (IRM) |
Lésion sous-corticale et corticale étendue |
Occlusion des grosses artères cérébrales Fibrillation atriale (embolisation) Rupture d’une plaque athéroscléreuse |
AVC lacunaire
AVC non lacunaire
AVC ischémique silencieux
| AVC ischémique – classification selon l’étiologie | |||
|---|---|---|---|
| AVC ischémique | Imagerie TDM ou IRM | Proportion | Étiologie |
| AVC cardioembolique | Non lacunaire | 27 % |
Fibrillation atriale (FA) – connue antérieurement Flutter atrial – connu antérieurement Infarctus aigu du myocarde Insuffisance cardiaque (FE < 40 %) Sténose mitrale Prothèse valvulaire Endocardite |
| AVC cryptogénique | Non lacunaire | 35 % |
Fibrillation atriale silencieuse (asymptomatique, non diagnostiquée) ESUS (Embolic Stroke of Undetermined Source) Foramen ovale perméable Cardiomyopathie atriale sans fibrillation atriale |
| AVC lié à l’athérosclérose des grosses artères | Non lacunaire | 13 % |
Athérosclérose carotidienne Athérosclérose aortique Athérosclérose des artères intracrâniennes |
| AVC lié à une maladie des petites artères | Lacunaire | 23 % |
Lipohyalinose Microathéromatose Angiopathie hypertensive |
| AVC dû à une autre cause déterminée | Lacunaire | 2 % |
Dissection artérielle Vascularite États thrombophiliques Migraine avec aura Maladie de Moyamoya |
L’examen histologique peut différencier les emboles cardioemboliques des emboles non cardioemboliques.
La fibrillation atriale (FA) peut provoquer un AVC ischémique cardioembolique ou cryptogénique.
Dans certains cas, la cause de l’AVC ne peut pas être clairement déterminée, par exemple si le patient présente une FA, une athérosclérose carotidienne significative et un foramen ovale perméable.
La fibrillation atriale (FA) est responsable d’AVC ischémiques cardioemboliques.
AVC ischémique cryptogénique
L’AVC cryptogénique est un diagnostic per exclusionem, ce qui signifie que la cause de l’AVC est recherchée étape par étape. Tant que la cause n’est pas clarifiée, l’AVC reste classé comme cryptogénique. Si la cause de l’AVC cryptogénique est ultérieurement identifiée, par exemple une FA silencieuse, l’AVC cryptogénique est reclassé en AVC cardioembolique en cas de FA. En cas d’AVC cryptogénique, les investigations visent à diagnostiquer :
| AVC cryptogénique – explorations | |
|---|---|
| Cause possible d’AVC cryptogénique | Explorations |
| Fibrillation atriale |
|
| Foramen ovale perméable (FOP) et thrombose veineuse profonde |
|
| Thrombus intracardiaque |
|
| Athérosclérose des grosses artères (carotides, aorte) |
|
| État d’hypercoagulabilité |
|
| Vascularite |
|
Foramen ovale perméable (FOP)
Syndrome de la classe économique
| Syndrome de la classe économique | |
|---|---|
| Durée du vol | Risque de thrombose veineuse (membres inférieurs, bassin) |
| < 4 heures | presque 0 % |
| 4–8 heures | 1 / 5 000 |
| > 8 heures | 1 / 1 500 |
La thrombose veineuse n’entraîne pas automatiquement une embolie ; le risque d’embolisation dépend de la localisation du thrombus.
| Risque d’embolisation en cas de thrombose veineuse | |
|---|---|
| Type de thrombose veineuse (TV) | Risque d’embolisation |
| TV proximale (veines fémorales, iliaques) | 25–50 % |
| TV distale (sous le genou – v. tibialis, fibularis) | < 5 % (en l’absence d’extension proximale) |
| TV pelvienne (v. iliaque interne/externe, v. cave inférieure) | 50–70 % |
Ces recommandations sont non officielles et ne représentent pas des recommandations formelles émises par une société professionnelle de cardiologie. Elles sont destinées uniquement à des fins éducatives et informatives.
