

Ein Schlaganfall kann ischämisch oder hämorrhagisch sein.
| Schlaganfall – Klassifikation | |
|---|---|
| Art des Schlaganfalls | Anteil der Fälle (%) |
| Ischämisch | 80 % |
| Hämorrhagisch – intrakraniell | 15 % |
| Hämorrhagisch – subarachnoidal | 5 % |
Die Gesamtprävalenz des ischämischen Schlaganfalls beträgt 2–3 % (> 7 % in der Bevölkerung > 65 Jahre).
Gemäß CT- oder MRT-Bildgebung kann der ischämische Schlaganfall klassifiziert werden als:
| Ischämischer Schlaganfall | |||
|---|---|---|---|
| Art des Schlaganfalls | CT/MRT-Läsion | Charakteristika | Typische Ursachen |
| Lakunär | < 15 mm (CT) < 20 mm (MRT) |
Kleine subkortikale Läsion |
Erkrankung kleiner Arteriolen Arterielle Hypertonie Diabetes mellitus |
| Nicht-lakunär | > 15 mm (CT) > 20 mm (MRT) |
Größere subkortikale und kortikale Läsion |
Okklusion großer zerebraler Arterien Vorhofflimmern (Embolisation) Ruptur einer atherosklerotischen Plaque |
Lakunärer Schlaganfall
Nicht-lakunärer Schlaganfall
Stiller ischämischer Schlaganfall
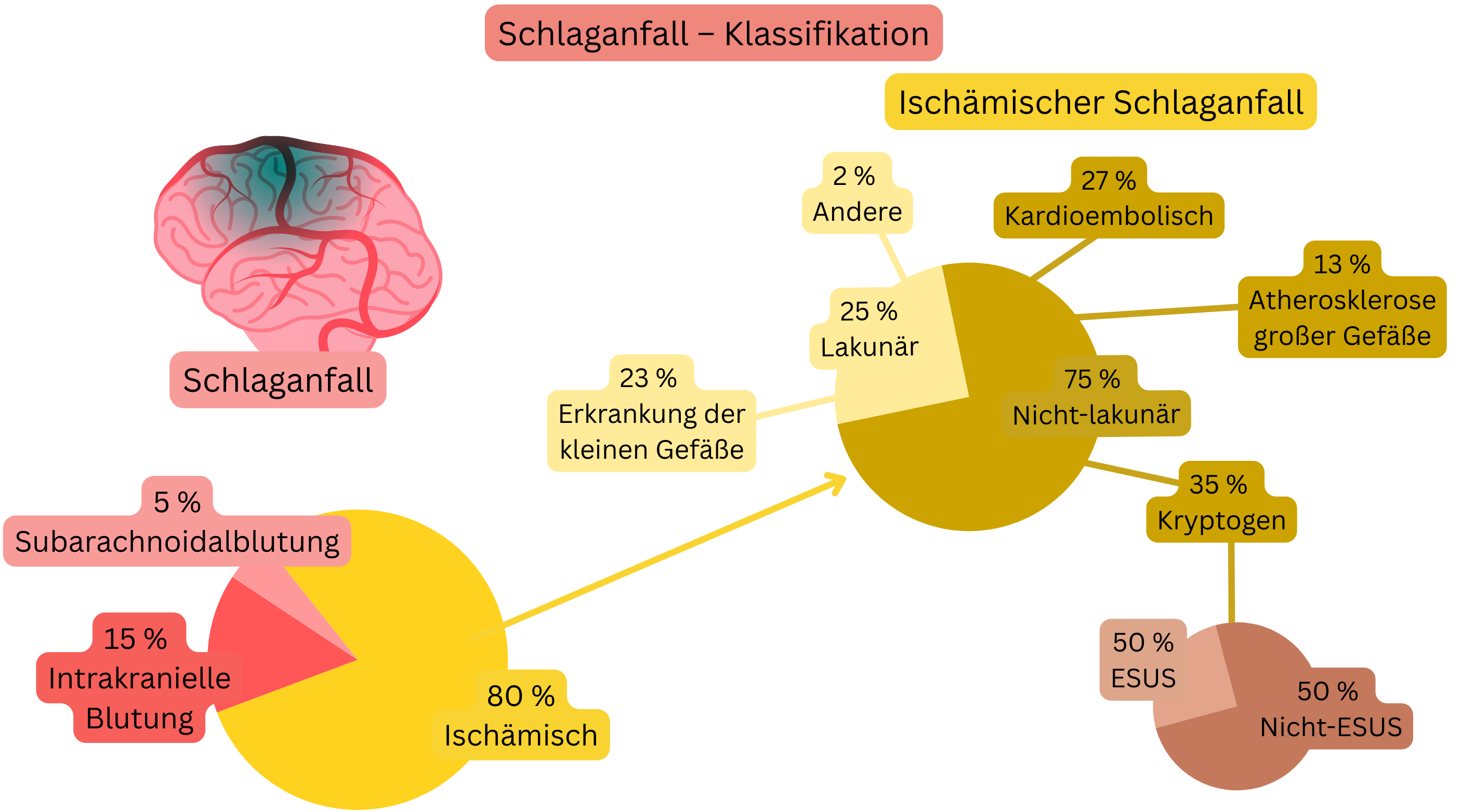
| Ischämischer Schlaganfall – Klassifikation nach Ätiologie | |||
|---|---|---|---|
| Ischämischer Schlaganfall | CT- oder MRT-Bildgebung | Anteil | Ätiologie |
| Kardioembolischer Schlaganfall | Nicht-lakunär | 27 % |
Vorhofflimmern (VHF) – zuvor diagnostiziert Vorhofflattern – zuvor diagnostiziert Akuter Myokardinfarkt Herzinsuffizienz (EF < 40 %) Mitralstenose Klappenprothese Endokarditis |
| Kryptogener Schlaganfall | Nicht-lakunär | 35 % |
Stilles Vorhofflimmern (asymptomatisch, nicht diagnostiziert) ESUS (Embolic Stroke of Undetermined Source) Persistierendes Foramen ovale Atriale Kardiomyopathie ohne Vorhofflimmern |
| Schlaganfall durch große Arteriosklerose | Nicht-lakunär | 13 % |
Karotisatherosklerose Aortenatherosklerose Intrakranielle Arteriosklerose |
| Schlaganfall durch Small-Vessel-Erkrankung | Lakunär | 23 % |
Lipohyalinose Mikroatheromatose Hypertensive Angiopathie |
| Schlaganfall anderer definierter Ursache | Lakunär | 2 % |
Arterielle Dissektion Vaskulitis Thrombophile Zustände Migräne mit Aura Moyamoya |
Die histologische Untersuchung kann zwischen kardioembolischen und nicht-kardioembolischen Emboli differenzieren.
Vorhofflimmern (VHF) kann einen kardioembolischen oder kryptogenen ischämischen Schlaganfall verursachen.
In einigen Fällen kann die Ursache des Schlaganfalls nicht eindeutig bestimmt werden, z. B. wenn der Patient VHF, eine relevante Karotisatherosklerose und ein persistierendes Foramen ovale aufweist.
Vorhofflimmern (VHF) verursacht kardioembolische ischämische Schlaganfälle.
Kryptogener ischämischer Schlaganfall
Der kryptogene Schlaganfall ist eine Diagnose per exclusionem, das heißt, die Ursache des Schlaganfalls wird schrittweise abgeklärt. Bis zur Klärung bleibt der Schlaganfall als kryptogen klassifiziert. Wird später die Ursache des kryptogenen Schlaganfalls diagnostiziert, z. B. stilles VHF, wird der kryptogene Schlaganfall als kardioembolischer Schlaganfall bei VHF reklassifiziert. Beim kryptogenen Schlaganfall erfolgen Untersuchungen zur Diagnose von:
| Kryptogener Schlaganfall – Diagnostik | |
|---|---|
| Mögliche Ursache des kryptogenen Schlaganfalls | Diagnostik |
| Vorhofflimmern |
|
| Persistierendes Foramen ovale (PFO) und tiefe Venenthrombose |
|
| Intrakardialer Thrombus |
|
| Großarterielle Atherosklerose (Karotiden, Aorta) |
|
| Hyperkoagulabilität |
|
| Vaskulitis |
|
Persistierendes Foramen ovale (PFO)
Economy-Class-Syndrom
| Economy-Class-Syndrom | |
|---|---|
| Flugdauer | Risiko einer venösen Thrombose (untere Extremitäten, Becken) |
| < 4 Stunden | nahezu 0 % |
| 4–8 Stunden | 1 / 5 000 |
| > 8 Stunden | 1 / 1 500 |
Eine venöse Thrombose embolisiert nicht automatisch; das Embolierisiko hängt von der Lokalisation des Thrombus ab.
| Embolierisiko bei venöser Thrombose | |
|---|---|
| Art der venösen Thrombose (VT) | Embolierisiko |
| Proximale VT (Vena femoralis, Vena iliaca) | 25–50 % |
| Distale VT (unterhalb des Knies – V. tibialis, V. fibularis) | < 5 % (wenn keine proximale Ausdehnung erfolgt) |
| Becken-VT (V. iliaca interna/externa, V. cava inferior) | 50–70 % |
Diese Leitlinien sind inoffiziell und stellen keine offiziellen Leitlinien dar, die von einer kardiologischen Fachgesellschaft herausgegeben wurden. Sie dienen ausschließlich zu Bildungs- und Informationszwecken.
