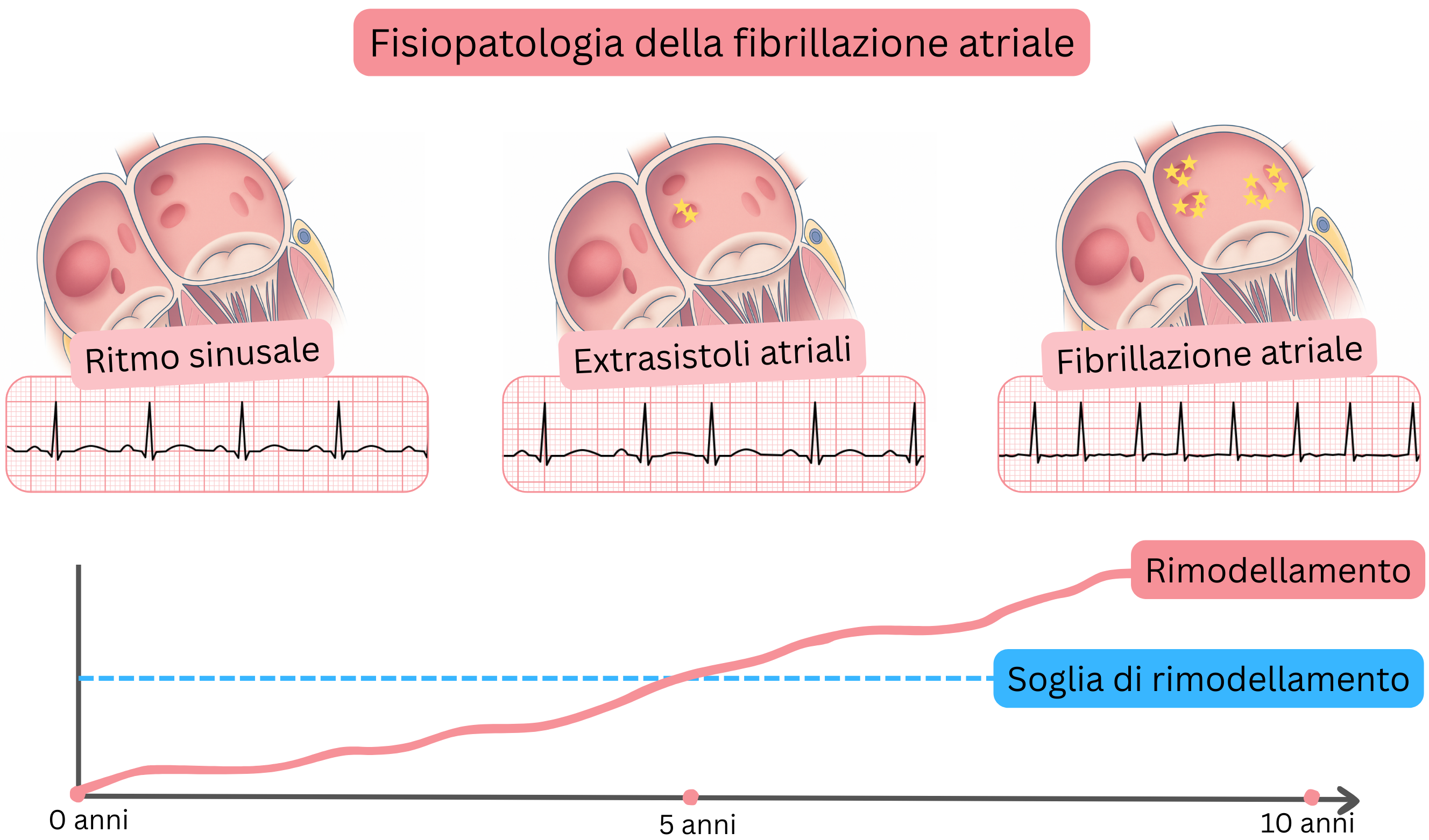
Fisiopatologia della fibrillazione atriale
Il substrato (trigger e substrato) della fibrillazione atriale (FA) si sviluppa quando si verifica un disturbo elettrico degli atri come conseguenza del rimodellamento atriale (strutturale, meccanico o elettrico). Il rimodellamento atriale può essere:
- Acuto (nell’arco di alcune ore)
- Cronico (nell’arco di diversi anni)
Rimodellamento atriale acuto
- Si sviluppa nell’arco di alcune ore durante una condizione critica acuta (ad es. infarto miocardico).
- Il rimodellamento acuto spesso regredisce dopo il trattamento della condizione critica.
- Il rimodellamento acuto è generalmente reversibile.
Rimodellamento atriale cronico
- Si sviluppa nell’arco di diversi anni a causa della cardiomiopatia atriale (ACMP).
- Nel 10% dei casi si sviluppa spontaneamente senza fattori di rischio (ACMP genetica).
- Nel 90% dei casi si sviluppa a causa di fattori di rischio.
- Il rimodellamento cronico è irreversibile.
Il rimodellamento atriale conduce allo sviluppo di un trigger negli atri, con molteplici foci elettrici (5–20) che generano impulsi in modo indipendente e attivano il substrato. La frequenza degli impulsi risultante è di 300–600/min. Gli atri non producono più una sistole sincrona, ma fibrillano—“tremolano”.
Il rimodellamento inizia più frequentemente nella regione degli osti delle vene polmonari nell’atrio sinistro, dove si sviluppano progressivamente sia il trigger sia il substrato della FA. L’ostio è la regione anatomica in cui la vena polmonare si connette all’atrio sinistro. Il rimodellamento si estende quindi progressivamente a tutto l’atrio sinistro e parzialmente all’atrio destro nell’arco di 5–15 anni.

| Fisiopatologia della fibrillazione atriale |
| Il substrato (trigger e substrato) della fibrillazione atriale si sviluppa più frequentemente a causa della cardiomiopatia atriale. |
| Lo stato pre-fibrillatorio consiste in extrasistoli atriali o tachicardia atriale originate dalla regione degli osti delle vene polmonari, talvolta visibili all’ECG. |
| Lo stato pre-fibrillatorio progredisce nell’arco di 6–12 mesi verso una fibrillazione atriale parossistica. |
| La fibrillazione atriale parossistica è più frequentemente innescata da extrasistoli atriali o tachicardia atriale originate dagli osti delle vene polmonari. |
Gli osti delle vene polmonari presentano proprietà elettrofisiologiche differenti rispetto al miocardio atriale. Gli osti contengono la più elevata densità di fibre nervose autonome e hanno un periodo refrattario breve. Pertanto, anche un rimodellamento minimo nella regione ostiale conduce facilmente allo sviluppo di foci (trigger) che generano impulsi tramite attività triggered o automaticità anomala. Questi foci generano quindi extrasistoli atriali o tachicardia atriale, che attivano il substrato e innescano la FA.
Stato pre-fibrillatorio
- Negli osti delle vene polmonari rimodellati si sviluppano inizialmente extrasistoli atriali (trigger) o brevi episodi (<60 s) di tachicardia atriale. Queste aritmie possono essere molto raramente documentate all’ECG o al monitoraggio Holter.
- Questo rappresenta il cosiddetto stato pre-fibrillatorio; il paziente non presenta ancora FA, ma nel prossimo futuro (nell’arco di 6–12 mesi) l’atrio sinistro raggiunge la cosiddetta soglia di rimodellamento e si sviluppa la FA.
Soglia di rimodellamento
- Se il rimodellamento supera la soglia di rimodellamento (si sviluppa il substrato), compare la FA.
- La FA si sviluppa quando extrasistoli atriali o tachicardia atriale originate dagli osti delle vene polmonari (trigger) attivano foci negli osti e nel miocardio dell’atrio sinistro (substrato). Questi foci generano quindi impulsi a una frequenza di 300–600/min.
- La FA inizia più frequentemente come FA parossistica (si interrompe spontaneamente entro 7 giorni).
Trigger della fibrillazione atriale
- La FA è più frequentemente innescata da extrasistoli atriali o tachicardia atriale.
- Le extrasistoli o la tachicardia originano più frequentemente da foci negli osti delle vene polmonari, sebbene i foci possano essere localizzati anche al di fuori della regione ostiale.
Episodio di fibrillazione atriale
- Durante un episodio di FA, gli impulsi originano in foci elettrici (all’interno del substrato) in modo indipendente a una frequenza di 300–600/min. Il nodo del seno è inattivato poiché viene continuamente depolarizzato dagli impulsi provenienti da questi foci.
- Gli atri si depolarizzano in modo asincrono e fibrillano in maniera non coordinata a una frequenza di 300–600/min.
- L’attività elettrica atriale viene trasmessa in modo irregolare ai ventricoli attraverso il nodo AV, che agisce come filtro, più frequentemente con una frequenza ventricolare di <100/min.

Fibrillazione atriale pre-eccitata
- Se il paziente presenta una via accessoria con conduzione anterograda, durante la FA gli impulsi vengono condotti ai ventricoli sia attraverso la via accessoria sia attraverso il nodo AV.
- La FA pre-eccitata significa che durante la FA l’ECG mostra un’onda delta.
- In tali pazienti non devono essere somministrati farmaci che bloccano il nodo AV, poiché può insorgere fibrillazione ventricolare.
- La fibrillazione ventricolare può verificarsi se il paziente presenta una via accessoria maligna (SPERRI <250 ms).





