Physiopathologie de la fibrillation atriale
Le substrat (déclencheur et substrat) de la fibrillation atriale (FA) se développe lorsqu’un trouble électrique des oreillettes survient en conséquence d’un remodelage atrial (structurel, mécanique ou électrique). Le remodelage atrial peut être :
- Aigu (en quelques heures)
- Chronique (sur plusieurs années)
Remodelage atrial aigu
- Se développe en quelques heures au cours d’une affection aiguë critique (p. ex. infarctus du myocarde).
- Le remodelage aigu régresse souvent après traitement de l’affection critique.
- Le remodelage aigu est généralement réversible.
Remodelage atrial chronique
- Se développe sur plusieurs années en raison d’une cardiomyopathie atriale (ACMP).
- 10% se développent spontanément sans facteurs de risque (ACMP génétique).
- 90% se développent en raison de facteurs de risque.
- Le remodelage chronique est irréversible.
Le remodelage atrial conduit au développement d’un déclencheur au sein des oreillettes, avec de multiples foyers électriques (5–20) générant des impulsions de manière indépendante et activant le substrat. La fréquence des impulsions résultantes est de 300–600/min. Les oreillettes ne produisent plus une systole synchrone mais fibrillent — « frémissent ».
Le remodelage débute le plus souvent au niveau des ostiums des veines pulmonaires dans l’oreillette gauche, où se développent progressivement le déclencheur et le substrat de la FA. L’ostium est la région anatomique où la veine pulmonaire se connecte à l’oreillette gauche. Le remodelage s’étend ensuite progressivement à l’ensemble de l’oreillette gauche et partiellement à l’oreillette droite sur une période de 5–15 ans.
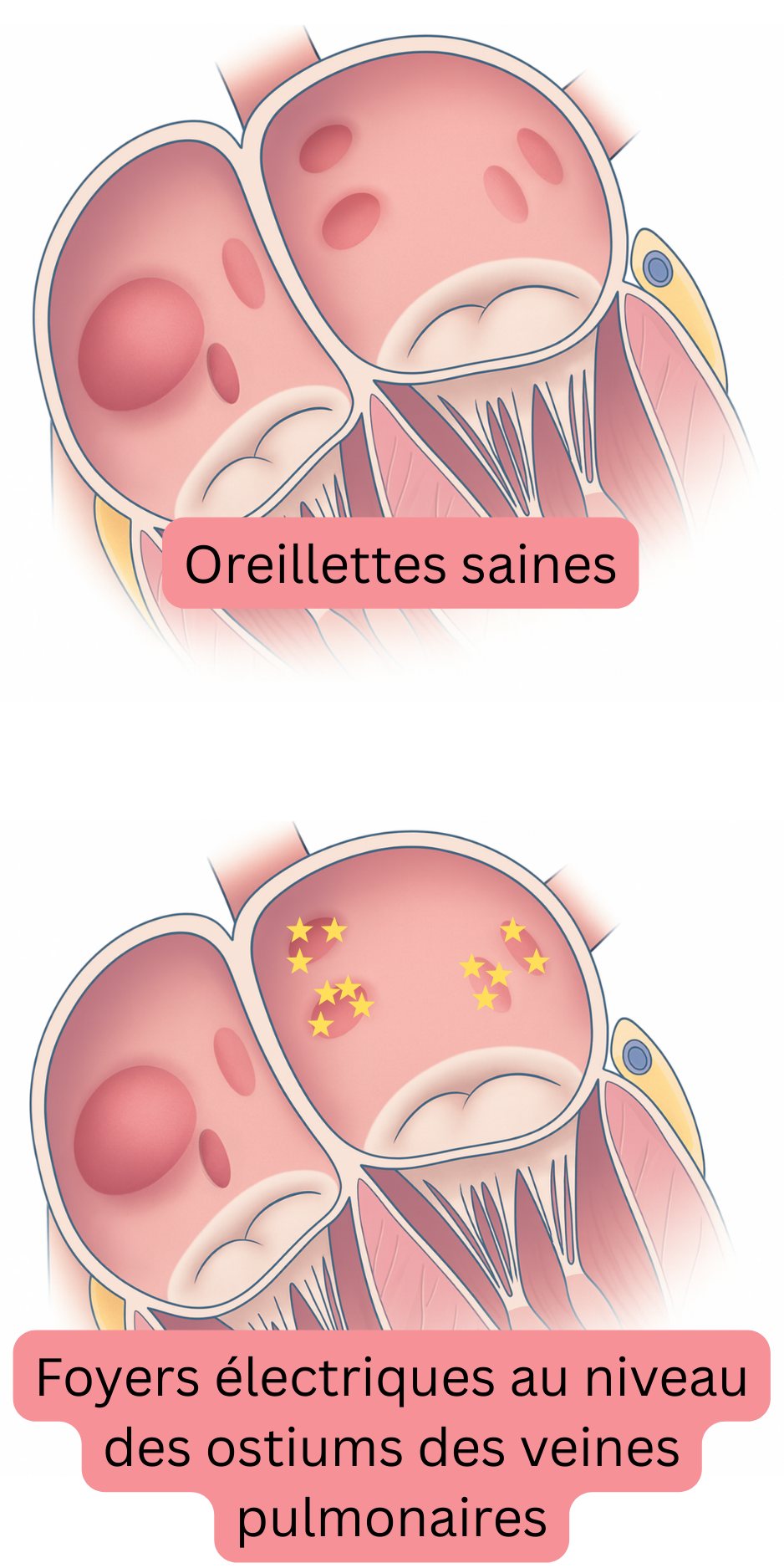
| Physiopathologie de la fibrillation atriale |
| Le substrat (déclencheur et substrat) de la fibrillation atriale se développe le plus souvent en raison d’une cardiomyopathie atriale. |
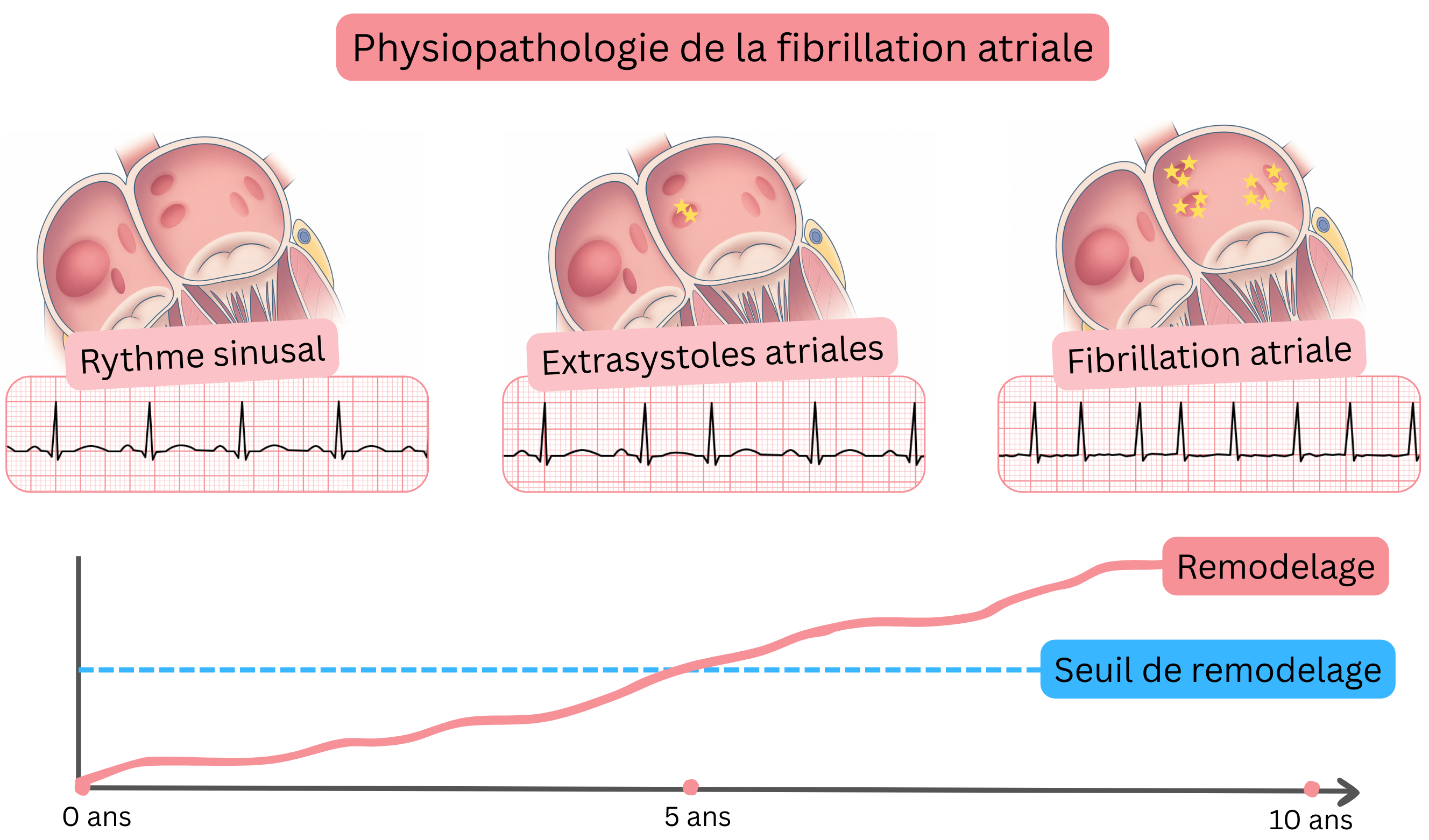
| L’état pré-fibrillatoire consiste en des extrasystoles atriales ou une tachycardie atriale provenant de la région des ostiums des veines pulmonaires, parfois visibles à l’ECG. |
| L’état pré-fibrillatoire progresse en 6–12 mois vers une fibrillation atriale paroxystique. |
| La fibrillation atriale paroxystique est le plus souvent déclenchée par des extrasystoles atriales ou une tachycardie atriale provenant des ostiums des veines pulmonaires. |
Les ostiums des veines pulmonaires présentent des propriétés électrophysiologiques différentes de celles du myocarde atrial. Les ostiums contiennent la plus forte densité de fibres nerveuses autonomes et ont une période réfractaire courte. Ainsi, même un remodelage minimal dans la région ostiale conduit facilement au développement de foyers (déclencheurs) générant des impulsions par activité déclenchée ou automaticité anormale. Ces foyers génèrent ensuite des extrasystoles atriales ou une tachycardie atriale, qui activent le substrat et initient la FA.
État pré-fibrillatoire
- Au niveau des ostiums des veines pulmonaires remodelés, des extrasystoles atriales (déclencheurs) ou une tachycardie atriale de courte durée (<60 s) se développent initialement. Ces arythmies ne sont que très rarement captées à l’ECG ou au Holter.
- Cela correspond à l’état dit pré-fibrillatoire ; le patient ne présente pas encore de FA, mais dans un avenir proche (dans les 6–12 mois) l’oreillette gauche atteint le seuil dit de remodelage et la FA se développe.
Seuil de remodelage
- Si le remodelage dépasse le seuil de remodelage (développement du substrat), la FA survient.
- La FA se développe lorsque des extrasystoles atriales ou une tachycardie atriale provenant des ostiums des veines pulmonaires (déclencheurs) activent des foyers au niveau des ostiums et du myocarde de l’oreillette gauche (substrat). Ces foyers génèrent alors des impulsions à une fréquence de 300–600/min.
- La FA débute le plus souvent sous forme de FA paroxystique (interruption spontanée en moins de 7 jours).
Déclencheur de la fibrillation atriale
- La FA est le plus souvent déclenchée par des extrasystoles atriales ou une tachycardie atriale.
- Les extrasystoles ou la tachycardie proviennent le plus souvent de foyers situés dans les ostiums des veines pulmonaires, bien que des foyers puissent également être localisés en dehors de la région ostiale.
Épisode de fibrillation atriale
- Au cours d’un épisode de FA, des impulsions naissent dans des foyers électriques (au sein du substrat) de manière indépendante à une fréquence de 300–600/min. Le nœud sinusal est désactivé car il est continuellement dépolarisé par les impulsions issues de ces foyers.
- Les oreillettes se dépolarisent de manière asynchrone et fibrillent de façon non coordonnée à une fréquence de 300–600/min.
- L’activité électrique atriale est transmise de façon irrégulière aux ventricules par le nœud AV, qui agit comme un filtre, le plus souvent avec une fréquence ventriculaire de <100/min.
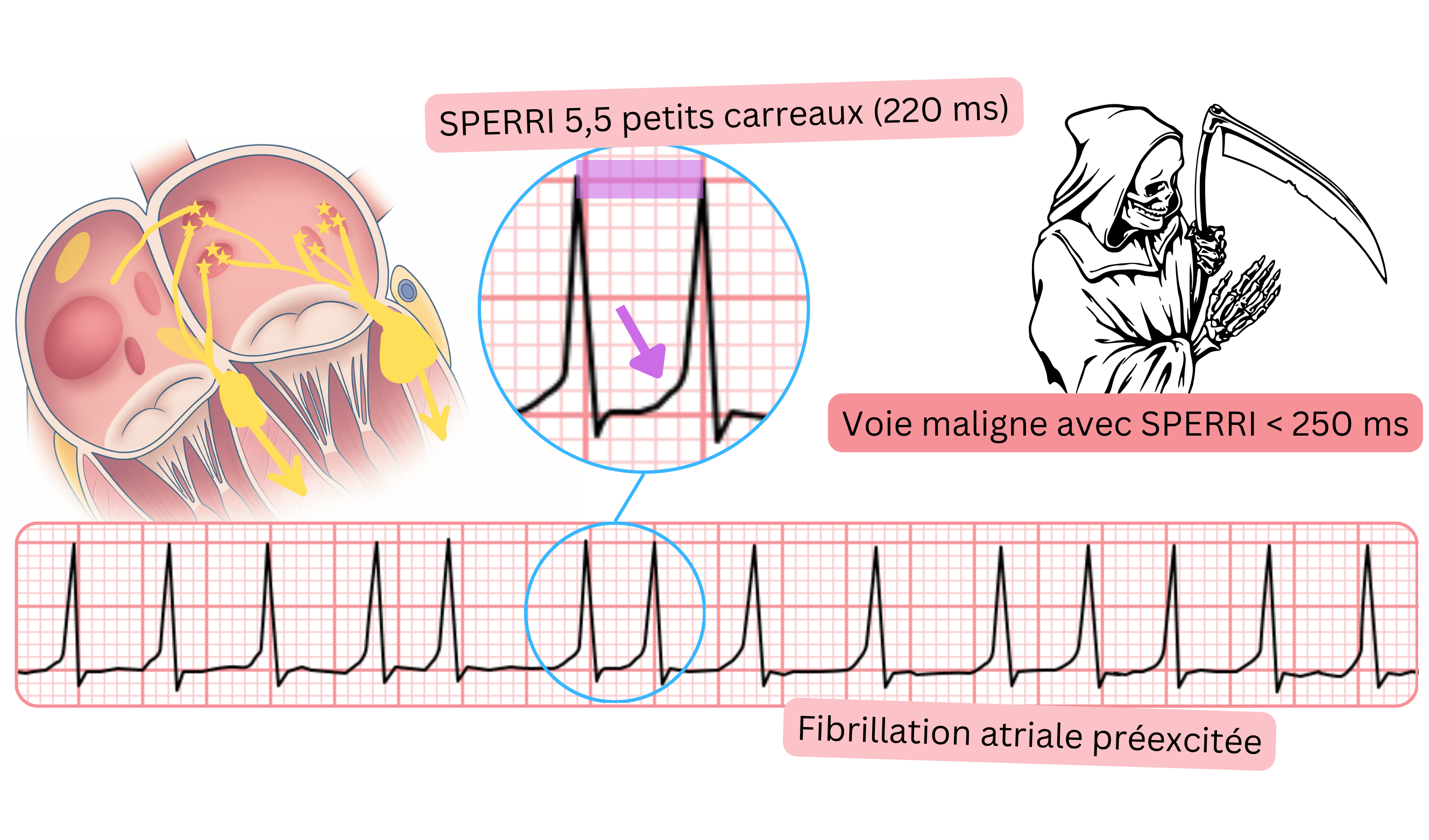
Fibrillation atriale pré-excitée
- Si le patient présente une voie accessoire antérograde, les impulsions au cours de la FA sont conduites aux ventricules à la fois par la voie accessoire et par le nœud AV.
- Une FA pré-excitée signifie que pendant la FA l’ECG montre une onde delta.
- Un tel patient ne doit pas recevoir de médicaments bloquant le nœud AV, car une fibrillation ventriculaire peut survenir.
- Une fibrillation ventriculaire peut survenir si le patient présente une voie accessoire maligne (SPERRI <250 ms).





