Atriyal fibrilasyonun (AF) antiaritmik farmakolojik tedavisinde aşağıdaki kavramlar ve ilkeler temel öneme sahiptir:
- Aksiyon potansiyeli
- Nodal aksiyon potansiyeli
- Nodaldışı aksiyon potansiyeli
- Kullanıma bağlı antiaritmik ilaçlar (Sınıf IC – Propafenon, Flekainid)
- Ters kullanıma bağlı antiaritmik ilaçlar (Sınıf III – Sotalol – en güçlü, Amiodaron, Dronedaron)
- Etkili refrakter periyot (Sınıf III ve IA)
- Otonom sinir sistemi
- Sempatik sinir sistemi (Sınıf II – beta-blokerler)
- Parasempatik sinir sistemi (Digoksin)
Aksiyon potansiyeli
- Kalpteki her kardiyomiyositin membranının dış ve iç yüzleri arasında elektriksel voltaj farkı vardır.
- Bu voltaj, membranın her iki tarafındaki farklı iyon konsantrasyonlarına (özellikle Na⁺, K⁺ ve Ca²⁺) bağlı olarak oluşur
- ve Na⁺/K⁺-ATPaz tarafından sürdürülen seçici geçirgenlik sayesinde korunur.
- Kardiyak siklus sırasında iyonlar membran boyunca hareket eder ve elektriksel voltaj buna bağlı olarak değişir.
- Kardiyak siklus sırasında elektriksel voltajdaki değişim aksiyon potansiyeli (AP) eğrisi ile gösterilir.
- AP, SA düğümünde spontan olarak oluşur ve ardından komşu kardiyomiyositler aracılığıyla atriyumlara yayılır.

Nodal aksiyon potansiyeli
- Pil (pacemaker) aksiyon potansiyeli (AP) olarak da adlandırılır.
- SA düğümünde ve AV düğümünde bulunur; bu nedenle nodal AP olarak adlandırılır.
- Spontan olarak oluşur; yani spontan depolarizasyon tekrarlayıcı şekilde gerçekleşir.
- Spontan depolarizasyon If akımları aracılığıyla gerçekleşir; bu sırada Na⁺ iyonları membranı geçer.
- Depolarizasyon sırasında Ca²⁺ iyonları membranı yavaş geçtiği için yavaş bir AP’dir.
- Başlangıcı (depolarizasyonu) yavaştır ancak süresi kısadır; bu nedenle yeni bir AP nispeten hızlı oluşur.
- Her fazda belirli iyonların membranı geçtiği 3 fazdan (4, 0, 3) oluşur.
| Nodal aksiyon potansiyeli ve antiaritmik ilaçlar |
| İlaç |
Sınıf |
Mekanizma |
SA düğüm |
AV düğüm |
| β-blokerler |
II |
↓ sempatik tonus |
↓ hız |
↓ iletim |
| Ca-blokerler |
IV |
Ca²⁺ blokajı |
↓ hız |
↓ iletim |
| Digoksin |
– |
↑ parasempatik tonus |
↓ hız |
↓ iletim |
| Ivabradin |
– |
If blokajı |
↓ hız |
– |

Nodaldışı aksiyon potansiyeli
- Pil dışı (non-pacemaker) aksiyon potansiyeli (AP) olarak da adlandırılır.
- Atriyum ve ventriküllerin çalışan miyokardında ve Purkinje liflerinde bulunur.
- Spontan depolarize olmaz; tetiklenmesi için komşu bir kardiyomiyositten gelen AP’ye ihtiyaç duyar.
- Depolarizasyon sırasında Na⁺ iyonları membranı hızlı geçtiği için hızlıdır.
- Her fazda belirli iyonların membranı geçtiği 5 fazdan (0, 1, 2, 3, 4) oluşur.
| Nodaldışı aksiyon potansiyeli (AP) ve antiaritmik ilaçlar |
| İlaç |
Sınıf |
Mekanizma |
AP |
EKG (QRS/QT) |
| Kinidin, Prokainamid, Disopiramid |
I A |
Na⁺ + K⁺ kanal blokajı |
↑ AP |
↑ QT |
| Lidokain, Meksiletin |
I B |
Na⁺ kanal blokajı (iskemik doku) |
↓ AP |
↓ QT |
| Flekainid, Propafenon |
I C |
Güçlü Na⁺ kanal blokajı |
≈ AP |
↑ QRS, QT ≈ |
| Amiodaron, Sotalol, Dronedaron |
III |
K⁺ kanal blokajı |
↑ AP |
↑ QT |
Nodaldışı AP, SA düğümünden başlayarak atriyal miyokard boyunca ilerler ve atriyal depolarizasyon (faz 0) EKG’de P dalgası olarak görülür. Depolarizasyon dalgası atriyumları < 100 ms’de geçer; bu nedenle P dalgası süresi < 100 ms’dir.
Nodaldışı AP, atriyumlardan AV düğüm üzerinden Purkinje liflerine ve ventriküllere yayılır. Ventriküler depolarizasyon (faz 0) EKG’de QRS kompleksi olarak görülür. Depolarizasyon dalgası ventrikülleri < 110 ms’de geçer; bu nedenle QRS süresi < 110 ms’dir.

Etkili refrakter periyot (ERP)
- Depolarizasyon başlangıcından (faz 0) repolarizasyonun neredeyse sonuna (faz 3) kadar olan süredir.
- ERP sırasında kardiyomiyositlerde yeni bir depolarizasyon, yani ek bir aksiyon potansiyeli oluşamaz,
- çünkü Na⁺ kanalları yeniden aktive olabilmek için depolarizasyondan sonra istirahat durumuna dönmelidir.
- ERP süresi EKG’de QT aralığı ile yansıtılır.
- QT aralığı nodaldışı AP süresini temsil eder
- ERP (QT aralığı) esas olarak Sınıf IA ve Sınıf III antiaritmik ilaçlarla uzar,
- çünkü bu ilaçlar K⁺ kanallarını bloke ederek repolarizasyonu yavaşlatır.
- Daha uzun ERP, miyokardın daha uzun süre uyarılamaz kalması anlamına gelir; bu da impulsların hızlı yeniden yayılımını önler
- böylece taşikardik AF sırasında maksimum ventrikül hızını azaltır ve
- re-entry mekanizmasını engeller.
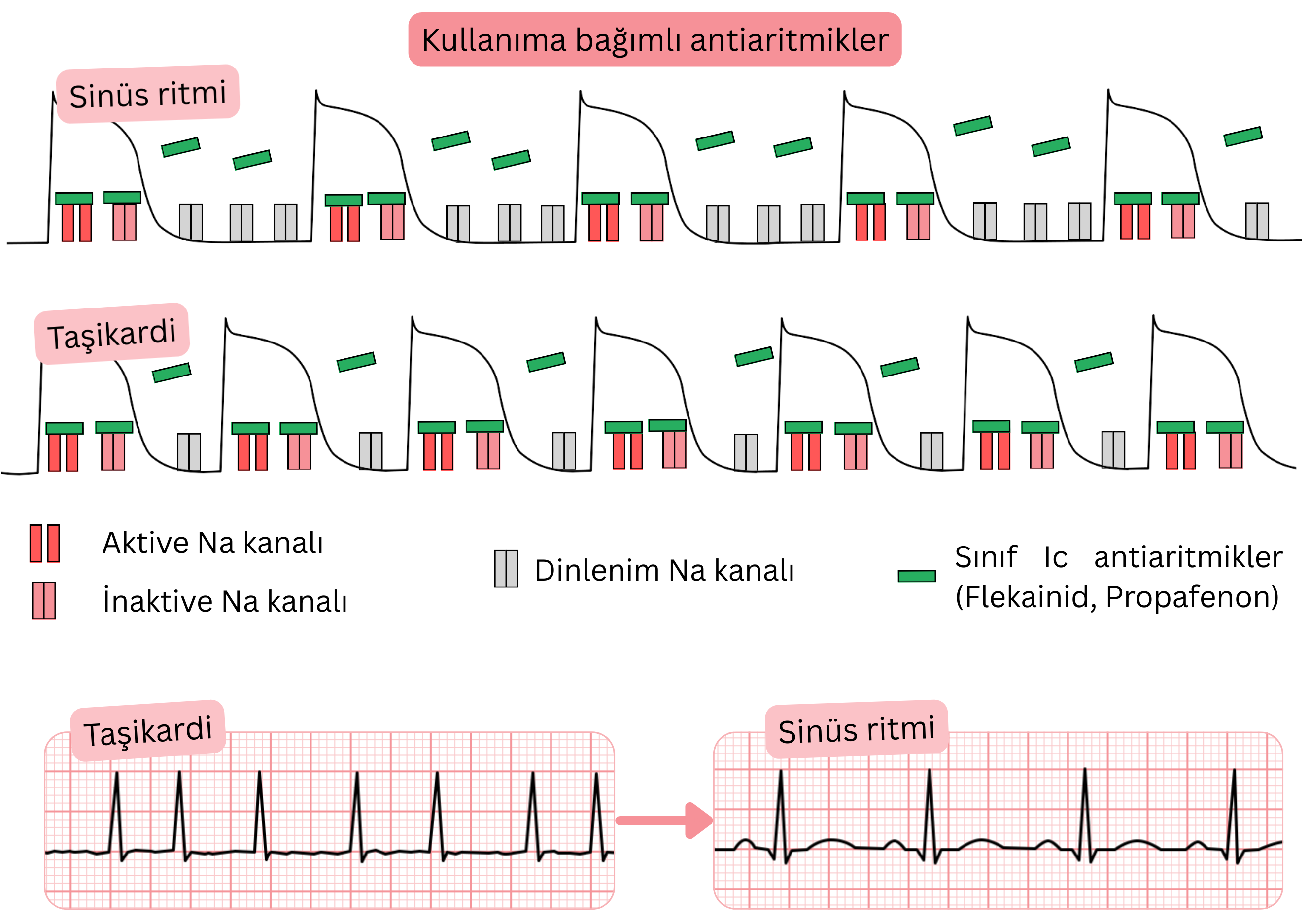
Kullanıma bağlı antiaritmik ilaçlar
- Kullanıma bağlılık, antiaritmik ilaçların iyon kanallarına
- daha yüksek kalp hızlarında (> 90/dk) daha yoğun bağlanmasını ifade eder
- Buna Sınıf IC antiaritmik ilaçlar (Propafenon, Flekainid) dahildir; AF’de şu amaçlarla kullanılır:
- taşikardik AF’nin (> 100/dk) farmakolojik kardiyoversiyonu ile sinüs ritmine dönüş
- sinüs ritminin sürdürülmesi (ritim kontrolü)
- Etki mekanizması (kullanıma bağlı antiaritmik ilaçlar):
- Aktive ve inaktive olmuş Na⁺ kanallarına tercihli olarak bağlanırlar
- Daha yüksek kalp hızı (> 90/dk) → daha fazla blokaj (kullanıma bağlılık)
- Taşikardi sırasında diyastol (aksiyon potansiyelinin faz 4’ü) kısalır,
- bu nedenle Na⁺ kanalları daha uzun süre aktive veya inaktive durumda kalır
- Sınıf IC antiaritmik ilaçlar Na⁺ kanallarına daha uzun süre bağlı kalır → daha yüksek kümülatif etki.
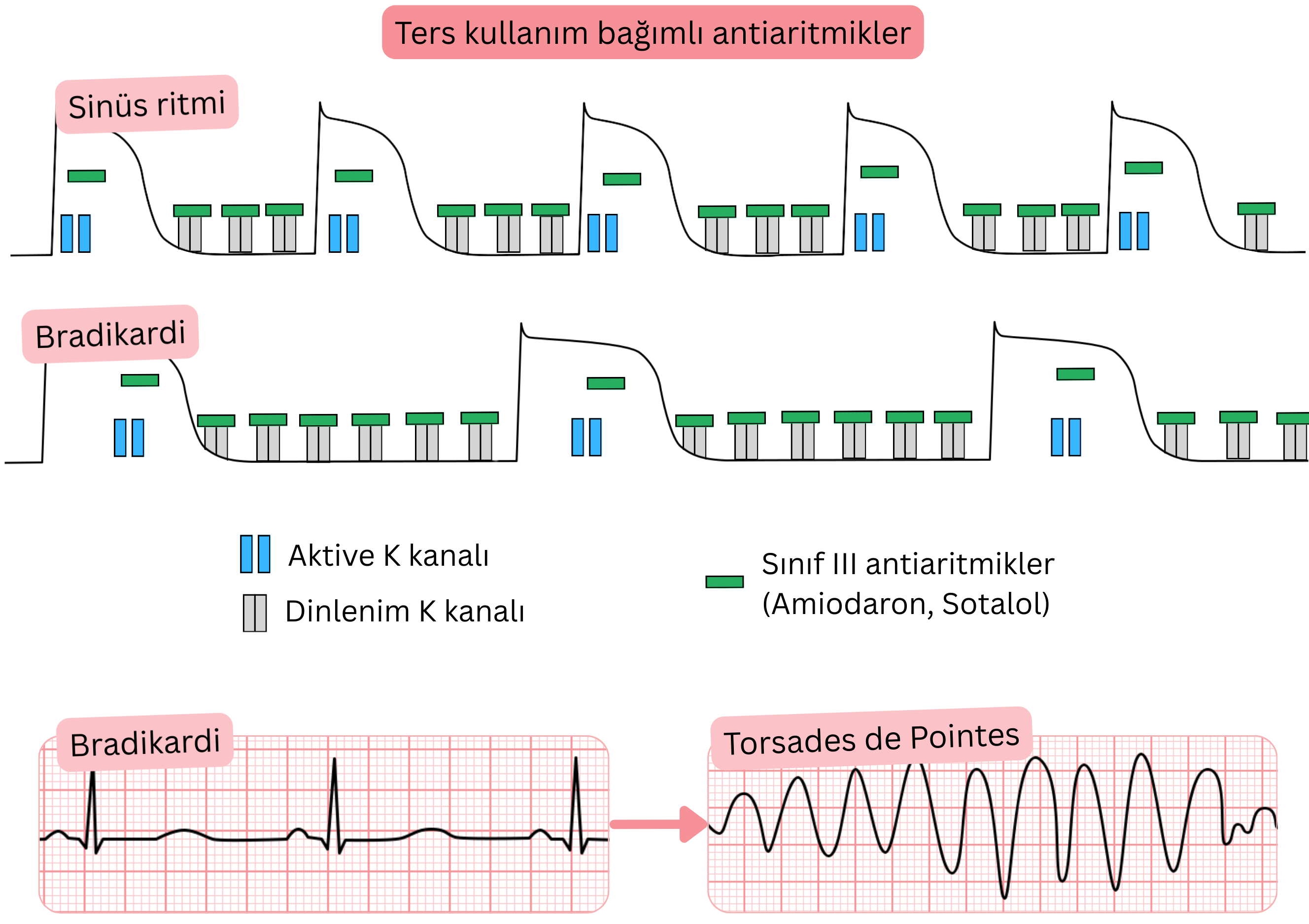
Ters kullanıma bağlı antiaritmik ilaçlar
- Ters kullanıma bağlılık, antiaritmik ilaçların iyon kanallarına
- daha düşük kalp hızlarında (< 90/dk) daha yoğun bağlanmasını ifade eder
- Buna Sınıf III antiaritmik ilaçlar (Sotalol – en güçlü, Amiodaron, Dronedaron) dahildir
- AF’de şu amaçla kullanılır:
- sinüs ritminin sürdürülmesi (ritim kontrolü)
- Etki mekanizması (ters kullanıma bağlı antiaritmik ilaçlar):
- Tercihen K⁺ kanallarına (faz 4) bağlanır ve K⁺ kanallarını bloke ederler
- Daha sonra K⁺ kanalları faz 3’te de bloke edilir ve QT aralığı uzar
- Daha düşük kalp hızı (bradikardi) → daha fazla blokaj (ters kullanıma bağlılık)
- Daha yavaş kalp hızlarında diyastol (faz 4) ve tüm aksiyon potansiyeli (faz 3) uzar
| Kullanıma bağlı ve ters kullanıma bağlı antiaritmik ilaçlar |
| Sınıf |
Antiaritmik ilaçlar |
Mekanizma |
Tip |
EKG etkisi |
Kesme kriteri |
| I A |
Kinidin,
prokainamid,
disopiramid |
Na⁺ ve K⁺ kanal blokajı |
Kullanıma bağlı |
↑ QT;
↑ QRS/PR (± hafif) |
QTc > 500 ms veya
ΔQTc > 60 ms;
QRS ↑ ≥ 25 % veya
> 120 – 130 ms |
| I B |
Lidokain,
meksiletin |
Na⁺ kanal blokajı (iskemik doku) |
Kullanıma bağlı |
↓ QT;
QRS ≈;
PR ≈ |
QRS ↑ ≥ 25 % başlangıca göre
veya BBB |
| I C |
Flekainid,
propafenon |
Güçlü Na⁺ kanal blokajı |
Kullanıma bağlı |
↑ QRS;
QT ≈;
PR ≈/↑ |
QRS ↑ ≥ 25 % veya
> 120 – 130 ms;
PR > 240 ms;
yeni BBB/AV blok |
| III |
Sotalol,
dofetilid,
ibutilid |
K⁺ kanal blokajı |
Ters kullanıma bağlı |
↑ QT (HR < 50/dk’da TdP riski) |
QTc > 500 ms veya ΔQTc > 60 ms;
HR < 50 – 60/dk |
| III |
Amiodaron |
K⁺, Na⁺, Ca²⁺ kanal blokajı + β-blokaj |
Ters kullanıma bağlı (hafif) |
↑ QT (hafif);
± ↑ PR/QRS |
QTc > 500 ms;
HR < 50/dk;
AV blok, BBB |
| III |
Dronedaron |
K⁺, Na⁺, Ca²⁺ kanal blokajı + β-blokaj (daha zayıf) |
Ters kullanıma bağlı (hafif) |
↑ QT (hafif) |
QTc > 500 ms;
HR < 50/dk;
AV blok, BBB |
BBB – Dal bloğu (RBBB veya LBBB), TdP – Torsades de Pointes
Otonom sinir sisteminin iki ana karşıt bileşeni vardır:
- Sempatik sinir sistemi
- Parasempatik sinir sistemi

Sempatik sinir sistemi
- Sempatik sinir sisteminin başlıca mediyatörleri adrenerjik reseptörlere bağlanan katekolaminlerdir
- Katekolaminler (adrenalin, noradrenalin, dopamin)
- Adrenerjik reseptörler (α1, α2, β1, β2, β3)
- Antiaritmik ilaçlar açısından özellikle beta reseptörler önemlidir:
- β1 – kalpte, özellikle SA düğümde ve daha az olarak AV düğümde bulunur
- β2 – bronşlar, akciğerler ve damarlarda bulunur
- Sempatik sinir sistemi esas olarak Sınıf II antiaritmik ilaçlar (beta-blokerler) ile hedeflenir
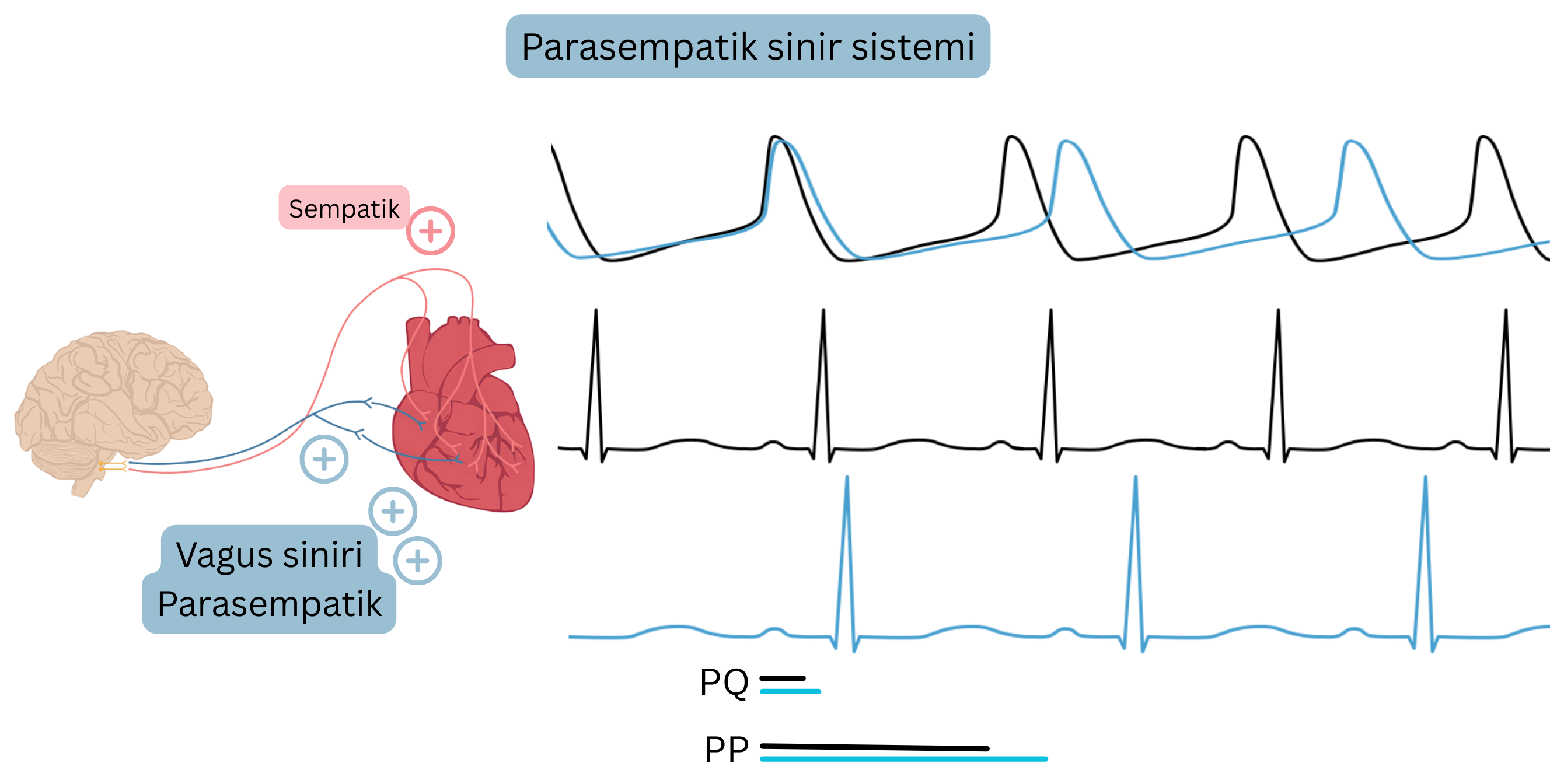
Parasempatik sinir sistemi
- Başlıca parasempatik sinir vagus siniridir
- Göz bebeklerini, tükürük bezlerini, bronşları, gastrointestinal sistemi, mesaneyi ve kalbi innerve eder
- Kalpte vagus esas olarak AV düğümü ve daha az olarak SA düğümü innerve eder; ayrıca atriyal miyokardı ve minimal düzeyde ventrikülleri innerve eder
- SA düğüm sağ vagus aracılığıyla innerve edilir
- AV düğüm sol vagus aracılığıyla innerve edilir
- bu nedenle supraventriküler taşikardinin (AVNRT, AVRT) sonlandırılmasında sol karotis sinüs masajı daha etkilidir.
- Parasempatik sinir sistemi esas olarak digoksin ile etkilenir
| Otonom sinir sistemi ve antiaritmik ilaçlar |
| İlaçlar |
Sinir sistemi üzerine etki |
Mekanizma |
Etki |
| β-blokerler |
Sempatik tonusu inhibe eder |
β1 (± β2) reseptör blokajı |
↓ SA hızı; ↓ AV iletimi |
| Digoksin |
Parasempatik tonusu artırır |
↑ vagal tonus |
↓ AV iletimi; ± ↓ SA hızı |









