Die folgenden Konzepte und Prinzipien sind für die antiarrhythmische pharmakologische Therapie des Vorhofflimmerns (VHF) von zentraler Bedeutung:
- Aktionspotenzial
- Nodales Aktionspotenzial
- Nicht-nodales Aktionspotenzial
- Use-dependente Antiarrhythmika (Klasse IC – Propafenon, Flecainid)
- Reverse-use-dependente Antiarrhythmika (Klasse III – Sotalol – am stärksten, Amiodaron, Dronedaron)
- Effektive Refraktärzeit (Klasse III und IA)
- Autonomes Nervensystem
- Sympathisches Nervensystem (Klasse II – Betablocker)
- Parasympathisches Nervensystem (Digoxin)
Aktionspotenzial
- Jeder Kardiomyozyt im Herzen weist eine elektrische Spannungsdifferenz zwischen der Außen- und Innenseite der Zellmembran auf.
- Diese Spannung entsteht durch unterschiedliche Ionenkonzentrationen (hauptsächlich Na⁺, K⁺ und Ca²⁺) auf beiden Seiten der Membran
- sowie durch deren selektive Permeabilität, die durch die Na⁺/K⁺-ATPase aufrechterhalten wird.
- Während des Herzzyklus bewegen sich Ionen über die Membran, wodurch sich die elektrische Spannung entsprechend verändert.
- Die Veränderung der elektrischen Spannung während des Herzzyklus wird durch die Kurve des Aktionspotenzials (AP) dargestellt.
- Das AP entsteht spontan im Sinusknoten und breitet sich anschließend über benachbarte Kardiomyozyten auf die Vorhöfe aus.
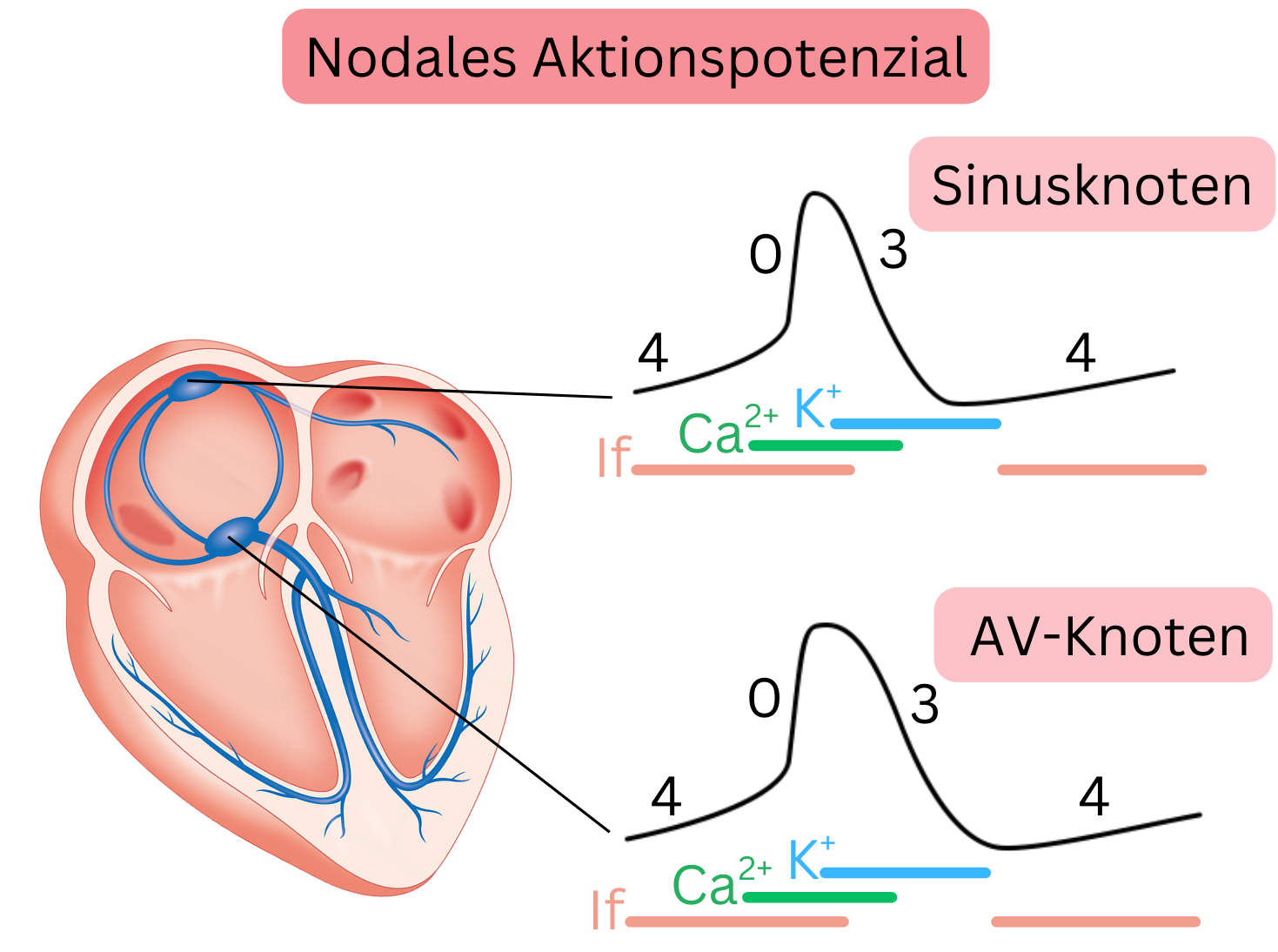
Nodales Aktionspotenzial
- Wird auch als Schrittmacher-Aktionspotenzial (AP) bezeichnet.
- Es ist im Sinusknoten und im AV-Knoten vorhanden und wird daher als nodales AP bezeichnet.
- Es entsteht spontan, d. h. eine spontane Depolarisation tritt wiederholt auf.
- Die spontane Depolarisation wird durch If-Ströme vermittelt, bei denen Na⁺-Ionen die Membran passieren.
- Es handelt sich um ein langsames AP, da Ca²⁺-Ionen die Membran während der Depolarisation langsam passieren.
- Es weist einen langsamen Anstieg (Depolarisation), jedoch eine kurze Dauer auf, sodass relativ rasch ein neues AP generiert wird.
- Es umfasst 3 Phasen (4, 0, 3), in denen jeweils spezifische Ionen die Membran passieren.
| Nodales Aktionspotenzial und Antiarrhythmika |
| Arzneimittel |
Klasse |
Mechanismus |
Sinusknoten |
AV-Knoten |
| β-Blocker |
II |
↓ sympathischer Tonus |
↓ Frequenz |
↓ Überleitung |
| Ca-Blocker |
IV |
Ca²⁺-Blockade |
↓ Frequenz |
↓ Überleitung |
| Digoxin |
– |
↑ parasympathischer Tonus |
↓ Frequenz |
↓ Überleitung |
| Ivabradin |
– |
If-Blockade |
↓ Frequenz |
– |
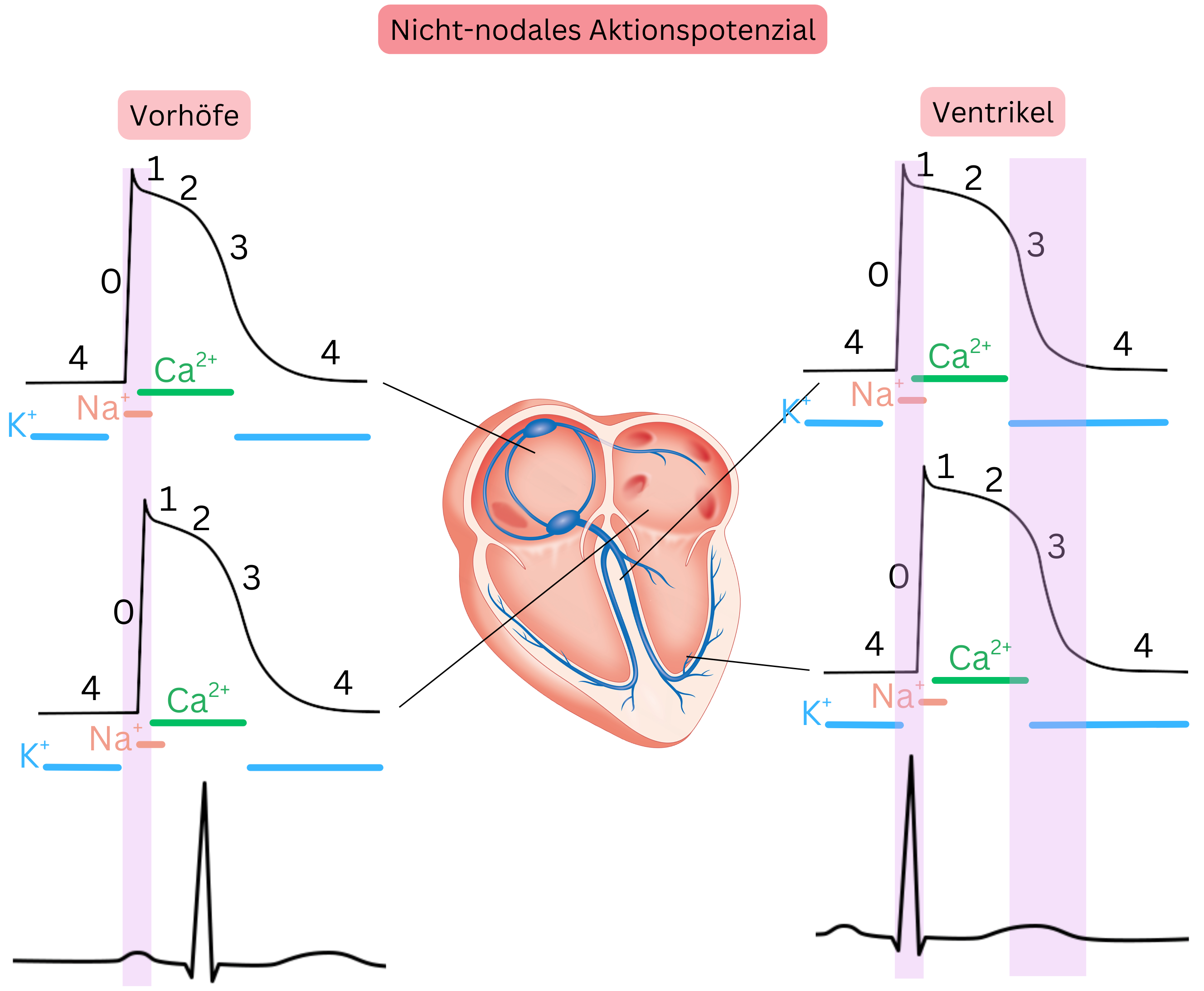
Nicht-nodales Aktionspotenzial
- Wird auch als Nicht-Schrittmacher-Aktionspotenzial (AP) bezeichnet.
- Es ist im Arbeitsmyokard der Vorhöfe und Ventrikel sowie in den Purkinje-Fasern vorhanden.
- Es depolarisiert nicht spontan; es benötigt ein AP eines benachbarten Kardiomyozyten als Trigger.
- Es ist schnell, da Na⁺-Ionen die Membran während der Depolarisation rasch passieren.
- Es umfasst 5 Phasen (0, 1, 2, 3, 4), in denen jeweils spezifische Ionen die Membran passieren.
| Nicht-nodales Aktionspotenzial (AP) und Antiarrhythmika |
| Arzneimittel |
Klasse |
Mechanismus |
AP |
EKG (QRS/QT) |
| Chinidin, Procainamid, Disopyramid |
I A |
Na⁺- und K⁺-Kanalblockade |
↑ AP |
↑ QT |
| Lidocain, Mexiletin |
I B |
Na⁺-Kanalblockade (ischämisches Gewebe) |
↓ AP |
↓ QT |
| Flecainid, Propafenon |
I C |
Starke Na⁺-Kanalblockade |
≈ AP |
↑ QRS, QT ≈ |
| Amiodaron, Sotalol, Dronedaron |
III |
K⁺-Kanalblockade |
↑ AP |
↑ QT |
Das nicht-nodale AP breitet sich vom Sinusknoten progressiv über das Vorhofmyokard aus, und die atriale Depolarisation (Phase 0) zeigt sich im EKG als P-Welle. Die Depolarisationswelle durchquert die Vorhöfe in < 100 ms; daher beträgt die P-Wellen-Dauer < 100 ms.
Das nicht-nodale AP breitet sich von den Vorhöfen über den AV-Knoten zu den Purkinje-Fasern und in die Ventrikel aus. Die ventrikuläre Depolarisation (Phase 0) zeigt sich im EKG als QRS-Komplex. Die Depolarisationswelle durchquert die Ventrikel in < 110 ms; daher beträgt die QRS-Dauer < 110 ms.
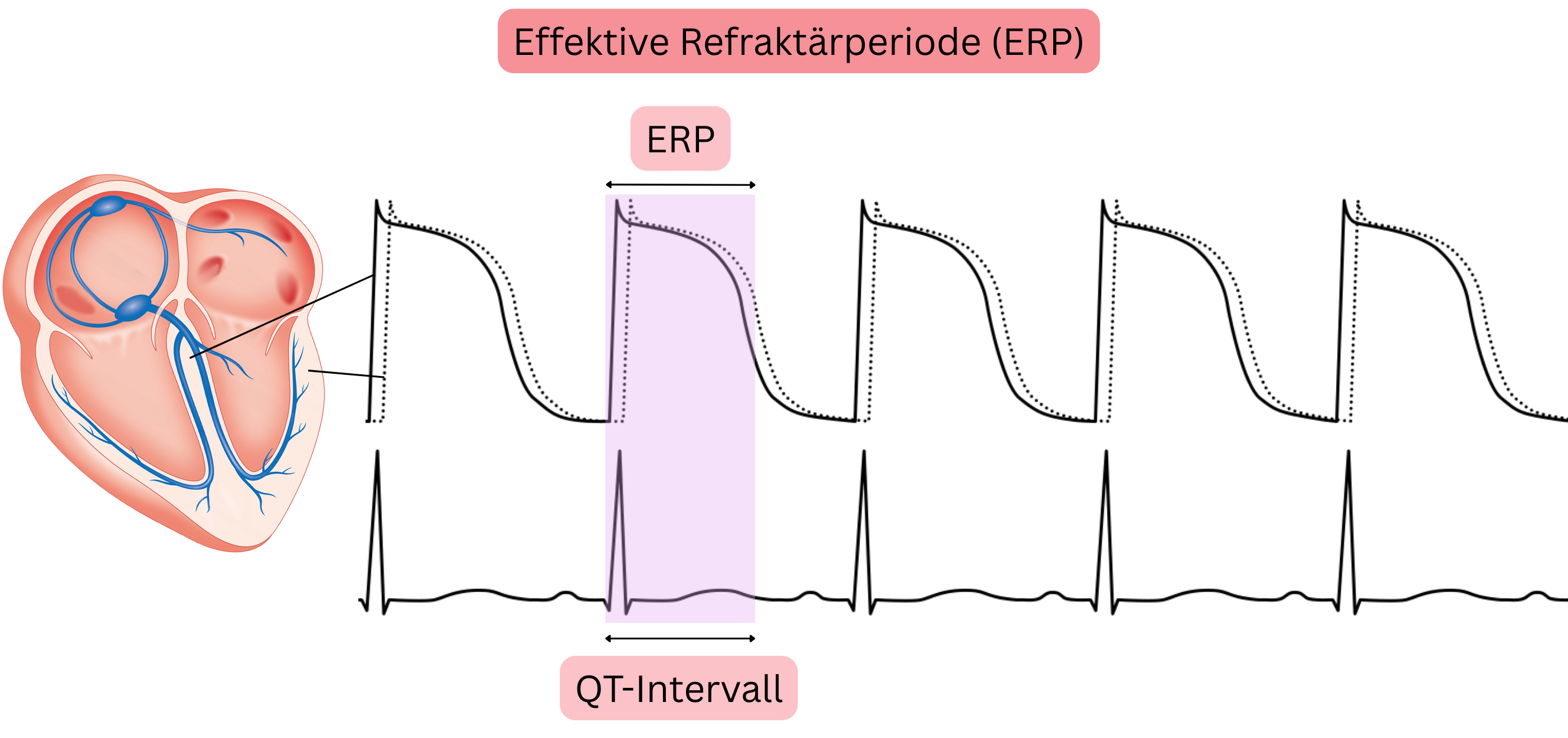
Effektive Refraktärzeit (ERP)
- Zeitraum vom Beginn der Depolarisation (Phase 0) bis nahezu zum Ende der Repolarisation (Phase 3)
- Während der ERP kann keine erneute Depolarisation, d. h. kein zusätzliches Aktionspotenzial, in den Kardiomyozyten auftreten,
- da die Na⁺-Kanäle nach der Depolarisation in den Ruhezustand zurückkehren müssen, bevor sie erneut aktiviert werden können.
- Die Dauer der ERP spiegelt sich im EKG als QT-Intervall wider.
- Das QT-Intervall repräsentiert die Dauer des nicht-nodalen AP.
- Die ERP (QT-Intervall) wird hauptsächlich durch Antiarrhythmika der Klasse IA und III verlängert,
- da sie K⁺-Kanäle blockieren und dadurch die Repolarisation verlangsamen.
- Eine verlängerte ERP bedeutet, dass das Myokard länger nicht erregbar bleibt, wodurch eine schnelle erneute Impulsausbreitung verhindert wird,
- wodurch die maximale Kammerfrequenz bei tachykardem VHF reduziert wird und
- Reentry-Mechanismen verhindert werden.
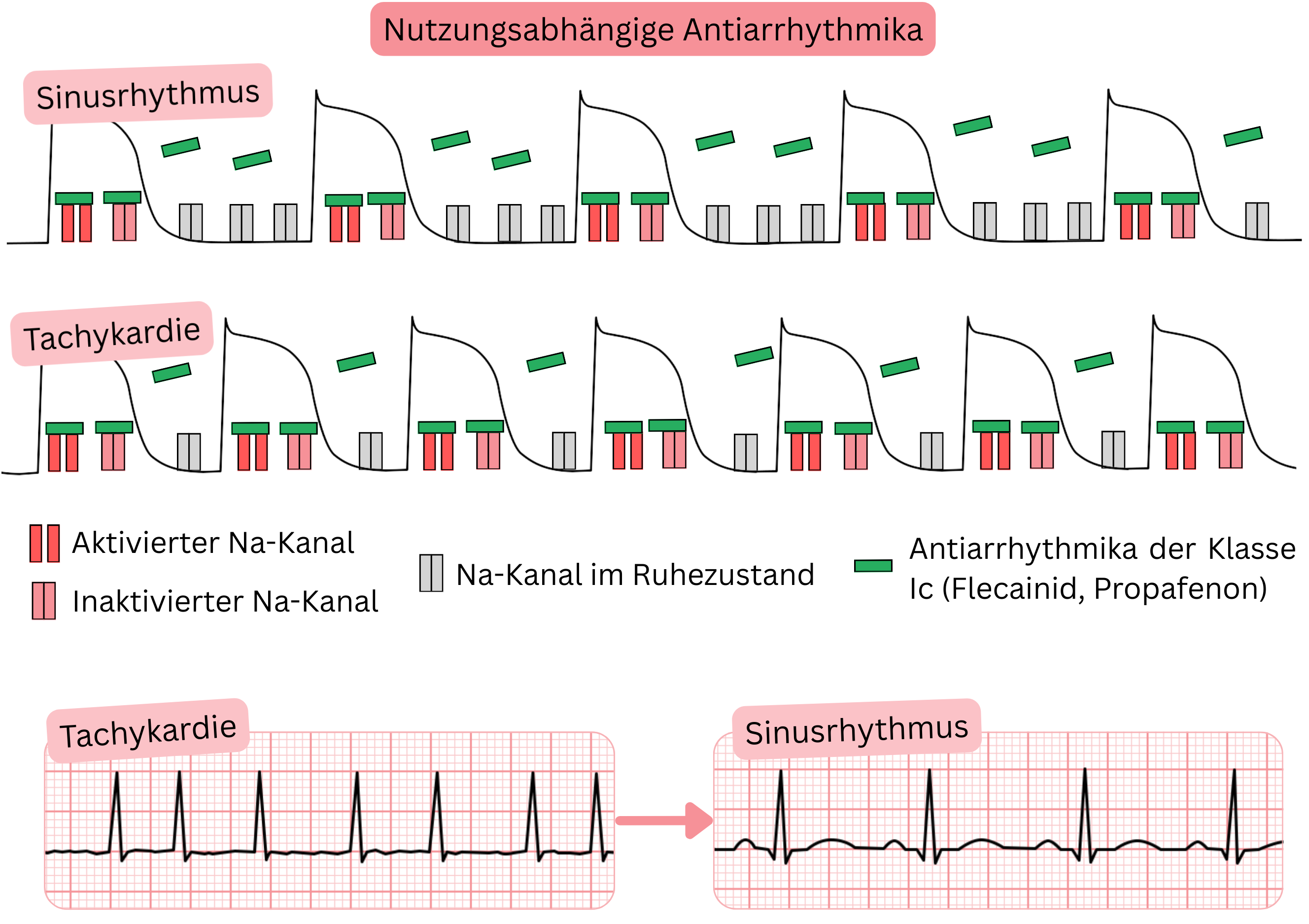
Use-dependente Antiarrhythmika
- Use-Dependence bezeichnet Antiarrhythmika, die an Ionenkanäle binden
- mit zunehmender Intensität bei höheren Herzfrequenzen (> 90/min).
- Hierzu gehören Antiarrhythmika der Klasse IC (Propafenon, Flecainid), die bei VHF eingesetzt werden zur:
- pharmakologischen Kardioversion eines tachykarden VHF (> 100/min) in den Sinusrhythmus
- Aufrechterhaltung des Sinusrhythmus (Rhythmuskontrolle)
- Wirkmechanismus (use-dependente Antiarrhythmika):
- Sie binden bevorzugt an aktivierte und inaktivierte Na⁺-Kanäle.
- Höhere Herzfrequenz (> 90/min) → stärkerer Blockadegrad (Use-Dependence).
- Während einer Tachykardie verkürzt sich die Diastole (Phase 4 des Aktionspotenzials),
- sodass Na⁺-Kanäle länger im aktivierten oder inaktivierten Zustand verbleiben.
- Antiarrhythmika der Klasse IC bleiben daher länger an Na⁺-Kanäle gebunden → höherer kumulativer Effekt.
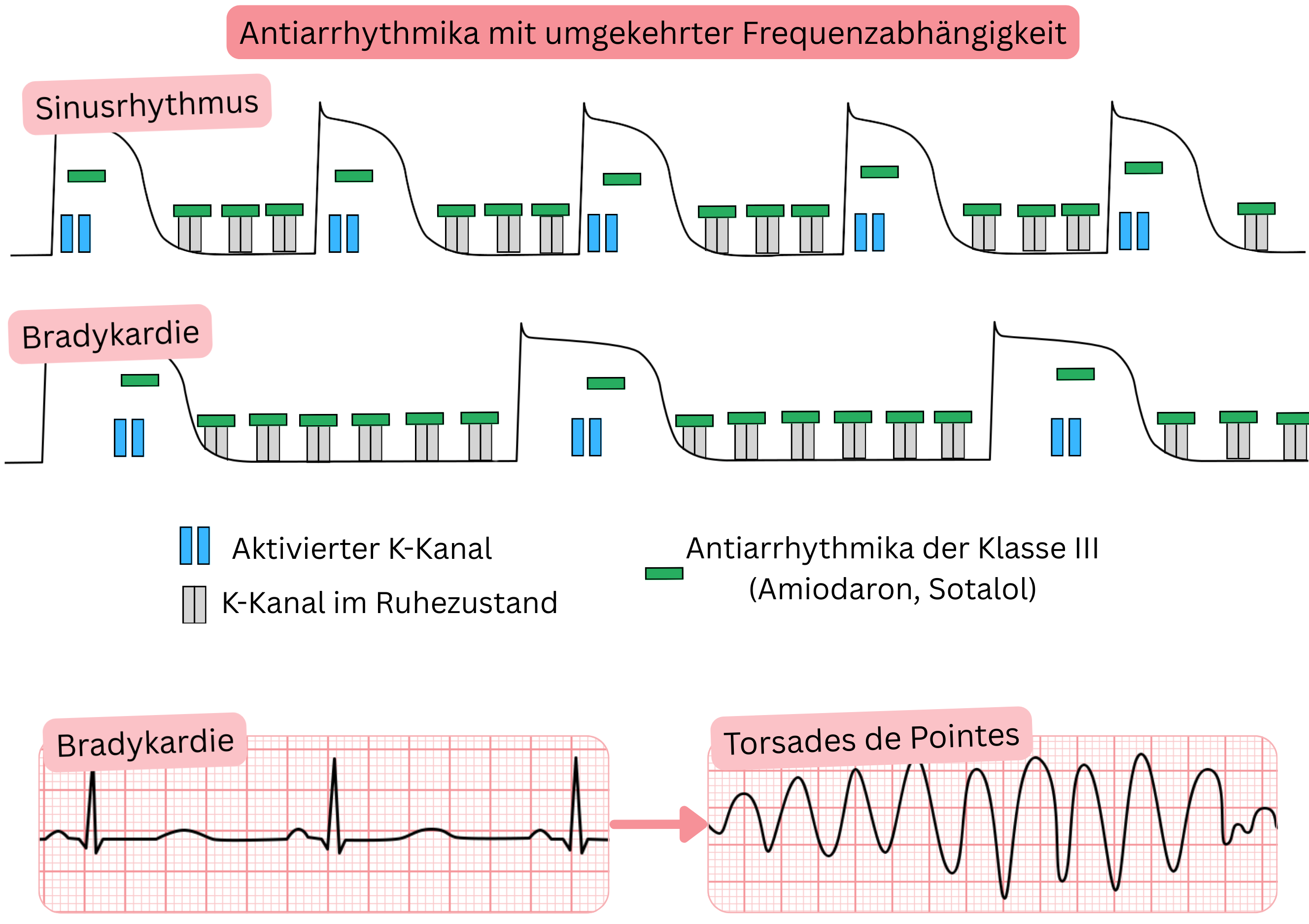
Reverse-use-dependente Antiarrhythmika
- Reverse-Use-Dependence bezeichnet Antiarrhythmika, die an Ionenkanäle binden
- mit zunehmender Intensität bei niedrigeren Herzfrequenzen (< 90/min).
- Hierzu gehören Antiarrhythmika der Klasse III (Sotalol – am stärksten, Amiodaron, Dronedaron).
- Bei VHF werden sie eingesetzt zur:
- Aufrechterhaltung des Sinusrhythmus (Rhythmuskontrolle)
- Wirkmechanismus (reverse-use-dependente Antiarrhythmika):
- Sie binden bevorzugt an K⁺-Kanäle (Phase 4) und blockieren diese.
- Anschließend sind K⁺-Kanäle auch in Phase 3 blockiert, was zu einer Verlängerung des QT-Intervalls führt.
- Niedrigere Herzfrequenz (Bradykardie) → stärkerer Blockadegrad (Reverse-Use-Dependence).
- Bei langsameren Herzfrequenzen sind die Diastole (Phase 4) und das gesamte Aktionspotenzial (Phase 3) verlängert.
| Use-Dependence und Reverse-Use-Dependence von Antiarrhythmika |
| Klasse |
Antiarrhythmika |
Mechanismus |
Typ |
EKG-Effekt |
Absetzen bei |
| I A |
Chinidin,
Procainamid,
Disopyramid |
Na⁺- und K⁺-Kanalblockade |
Use-Dependence |
↑ QT;
↑ QRS/PR (± mild) |
QTc > 500 ms oder
ΔQTc > 60 ms;
QRS ↑ ≥ 25 % oder
> 120 – 130 ms |
| I B |
Lidocain,
Mexiletin |
Na⁺-Kanalblockade (ischämisches Gewebe) |
Use-Dependence |
↓ QT;
QRS ≈;
PR ≈ |
QRS ↑ ≥ 25 % vom Ausgangswert
oder neu aufgetretener Schenkelblock |
| I C |
Flecainid,
Propafenon |
Starke Na⁺-Kanalblockade |
Use-Dependence |
↑ QRS;
QT ≈;
PR ≈/↑ |
QRS ↑ ≥ 25 % oder
> 120 – 130 ms;
PR > 240 ms;
neu aufgetretener Schenkelblock/AV-Block |
| III |
Sotalol,
Dofetilid,
Ibutilid |
K⁺-Kanalblockade |
Reverse-Use-Dependence |
↑ QT (Risiko für TdP bei HF < 50/min) |
QTc > 500 ms oder ΔQTc > 60 ms;
HF < 50 – 60/min |
| III |
Amiodaron |
K⁺-, Na⁺-, Ca²⁺-Kanalblockade + β-Blockade |
Reverse-Use-Dependence (mild) |
↑ QT (mild);
± ↑ PR/QRS |
QTc > 500 ms;
HF < 50/min;
AV-Block, Schenkelblock |
| III |
Dronedaron |
K⁺-, Na⁺-, Ca²⁺-Kanalblockade + β-Blockade (schwächer) |
Reverse-Use-Dependence (mild) |
↑ QT (mild) |
QTc > 500 ms;
HF < 50/min;
AV-Block, Schenkelblock |
BBB – Schenkelblock (RBBB oder LBBB), TdP – Torsade de Pointes
Das autonome Nervensystem umfasst zwei gegensätzlich wirkende Hauptkomponenten:
- Sympathisches Nervensystem
- Parasympathisches Nervensystem
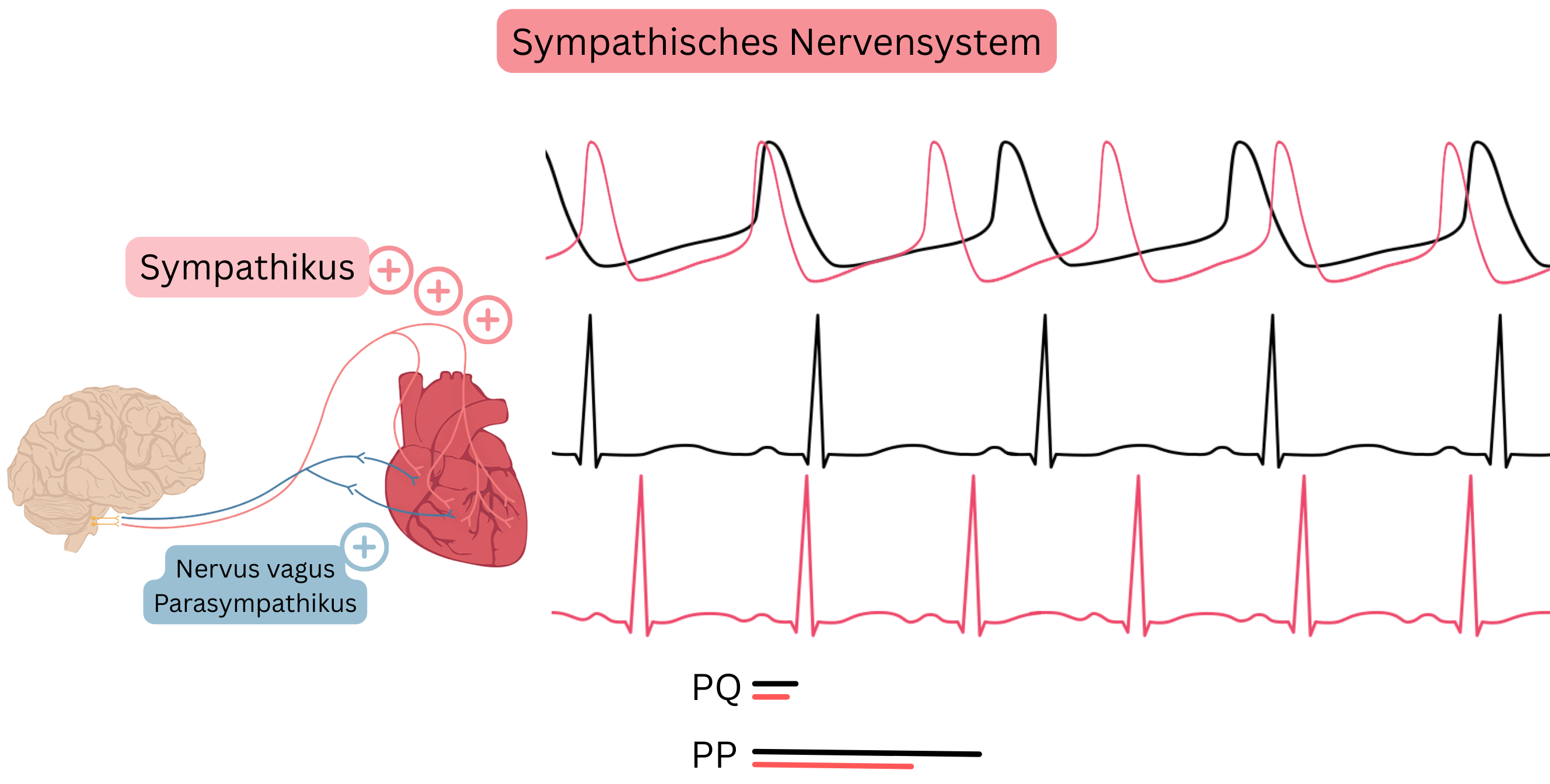
Sympathisches Nervensystem
- Die Hauptmediatoren des sympathischen Nervensystems sind Katecholamine, die an adrenerge Rezeptoren binden.
- Katecholamine (Adrenalin, Noradrenalin, Dopamin)
- Adrenerge Rezeptoren (α1, α2, β1, β2, β3)
- Für Antiarrhythmika sind insbesondere β-Rezeptoren relevant:
- β1 – im Herzen lokalisiert, überwiegend im Sinusknoten und geringer im AV-Knoten
- β2 – in Bronchien, Lunge und Gefäßen lokalisiert
- Das sympathische Nervensystem wird hauptsächlich durch Antiarrhythmika der Klasse II (Betablocker) beeinflusst.
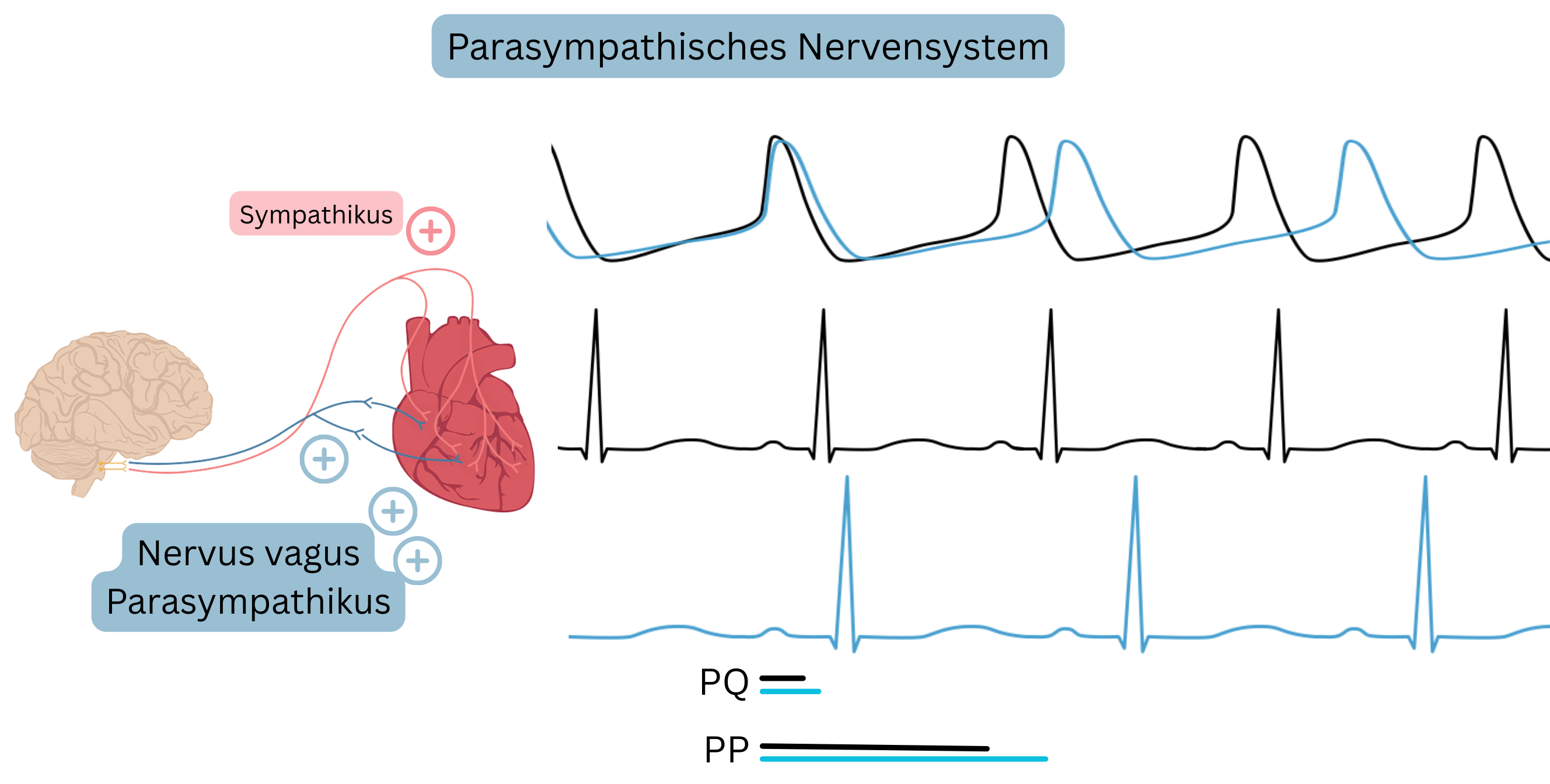
Parasympathisches Nervensystem
- Der wichtigste parasympathische Nerv ist der Nervus vagus.
- Er innerviert Pupillen, Speicheldrüsen, Bronchien, Gastrointestinaltrakt, Harnblase und das Herz.
- Am Herzen innerviert der Vagus überwiegend den AV-Knoten und in geringerem Maße den Sinusknoten; zudem innerviert er das Vorhofmyokard und minimal die Ventrikel.
- Der Sinusknoten wird über den rechten Vagus innerviert.
- Der AV-Knoten wird über den linken Vagus innerviert.
- Daher ist zur Terminierung einer supraventrikulären Tachykardie (AVNRT, AVRT) die Massage des linken Karotissinus wirksamer.
- Das parasympathische Nervensystem wird hauptsächlich durch Digoxin beeinflusst.
| Autonomes Nervensystem und Antiarrhythmika |
| Arzneimittel |
Wirkung auf das Nervensystem |
Mechanismus |
Effekt |
| β-Blocker |
Hemmung des sympathischen Tonus |
β1- (± β2-) Rezeptorblockade |
↓ Sinusfrequenz; ↓ AV-Überleitung |
| Digoxin |
Steigerung des parasympathischen Tonus |
↑ Vagotonus |
↓ AV-Überleitung; ± ↓ Sinusfrequenz |









