I seguenti concetti e principi sono fondamentali per il trattamento farmacologico antiaritmico della fibrillazione atriale (FA):
- Potenziale d’azione
- Potenziale d’azione nodale
- Potenziale d’azione non nodale
- Farmaci antiaritmici use-dependent (Classe IC – Propafenone, Flecainide)
- Farmaci antiaritmici reverse use-dependent (Classe III – Sotalolo – più potente, Amiodarone, Dronedarone)
- Periodo refrattario efficace (Classe III e IA)
- Sistema nervoso autonomo
- Sistema nervoso simpatico (Classe II – beta-bloccanti)
- Sistema nervoso parasimpatico (Digossina)
Potenziale d’azione
- Ogni cardiomiocita del cuore presenta una differenza di potenziale elettrico tra il versante esterno e quello interno della membrana.
- Questa differenza di potenziale deriva dalla diversa concentrazione ionica (principalmente Na⁺, K⁺ e Ca²⁺) ai due lati della membrana
- e dalla sua permeabilità selettiva mantenuta dalla Na⁺/K⁺-ATPasi.
- Durante il ciclo cardiaco, gli ioni attraversano la membrana e il potenziale elettrico varia di conseguenza.
- La variazione del potenziale elettrico durante il ciclo cardiaco è rappresentata dalla curva del potenziale d’azione (PA).
- Il PA origina spontaneamente nel nodo senoatriale (SA) e successivamente si propaga ai cardiomiociti adiacenti fino agli atri.

Potenziale d’azione nodale
- Definito anche potenziale d’azione pacemaker (PA).
- È presente nel nodo SA e nel nodo atrioventricolare (AV) ed è pertanto denominato PA nodale.
- Origina spontaneamente, cioè si verifica una depolarizzazione spontanea ripetuta.
- La depolarizzazione spontanea è mediata dalle correnti If, durante le quali gli ioni Na⁺ attraversano la membrana.
- È un PA lento poiché durante la depolarizzazione gli ioni Ca²⁺ attraversano lentamente la membrana.
- Presenta un inizio lento (depolarizzazione) ma una durata breve, per cui un nuovo PA si genera relativamente rapidamente.
- Presenta 3 fasi (4, 0, 3), durante le quali specifici ioni attraversano la membrana in ciascuna fase.
| Potenziale d’azione nodale e farmaci antiaritmici |
| Farmaco |
Classe |
Meccanismo |
Nodo SA |
Nodo AV |
| β-bloccanti |
II |
↓ tono simpatico |
↓ frequenza |
↓ conduzione |
| Ca-antagonisti |
IV |
Blocco Ca²⁺ |
↓ frequenza |
↓ conduzione |
| Digossina |
– |
↑ tono parasimpatico |
↓ frequenza |
↓ conduzione |
| Ivabradina |
– |
Blocco If |
↓ frequenza |
– |

Potenziale d’azione non nodale
- Definito anche potenziale d’azione non pacemaker (PA).
- È presente nel miocardio di lavoro degli atri, dei ventricoli e nelle fibre del Purkinje.
- Non si depolarizza spontaneamente; necessita di un PA proveniente da un cardiomiocita adiacente per essere attivato.
- È rapido poiché durante la depolarizzazione gli ioni Na⁺ attraversano rapidamente la membrana.
- Presenta 5 fasi (0, 1, 2, 3, 4), durante le quali specifici ioni attraversano la membrana in ciascuna fase.
| Potenziale d’azione non nodale (PA) e farmaci antiaritmici |
| Farmaco |
Classe |
Meccanismo |
PA |
ECG (QRS/QT) |
| Chinidina, Procainamide, Disopiramide |
I A |
Blocco dei canali Na⁺ + K⁺ |
↑ PA |
↑ QT |
| Lidocaina, Mexiletina |
I B |
Blocco dei canali Na⁺ (tessuto ischemico) |
↓ PA |
↓ QT |
| Flecainide, Propafenone |
I C |
Blocco potente dei canali Na⁺ |
≈ PA |
↑ QRS, QT ≈ |
| Amiodarone, Sotalolo, Dronedarone |
III |
Blocco dei canali K⁺ |
↑ PA |
↑ QT |
Il PA non nodale si propaga progressivamente dal nodo SA attraverso il miocardio atriale e la depolarizzazione atriale (fase 0) è visibile all’ECG come onda P. L’onda di depolarizzazione attraversa gli atri in < 100 ms; pertanto la durata dell’onda P è < 100 ms.
Il PA non nodale si propaga dagli atri attraverso il nodo AV fino alle fibre del Purkinje e ai ventricoli. La depolarizzazione ventricolare (fase 0) è visibile all’ECG come complesso QRS. L’onda di depolarizzazione attraversa i ventricoli in < 110 ms; pertanto la durata del QRS è < 110 ms.

Periodo refrattario efficace (ERP)
- Intervallo di tempo dall’inizio della depolarizzazione (fase 0) fino quasi al termine della ripolarizzazione (fase 3)
- Durante l’ERP non può verificarsi un’ulteriore depolarizzazione, cioè un nuovo potenziale d’azione, nei cardiomiociti,
- poiché i canali Na⁺ devono ritornare allo stato di riposo dopo la depolarizzazione prima di poter essere nuovamente attivati.
- La durata dell’ERP è riflessa all’ECG dall’intervallo QT.
- L’intervallo QT rappresenta la durata del PA non nodale
- L’ERP (intervallo QT) è prolungato principalmente dai farmaci antiaritmici di Classe IA e Classe III,
- poiché bloccano i canali K⁺ e quindi rallentano la ripolarizzazione.
- Un ERP più lungo significa che il miocardio rimane non eccitabile per un tempo maggiore, prevenendo la rapida ri-propagazione degli impulsi
- riducendo così la frequenza ventricolare massima nella FA tachicardica e
- prevenendo i circuiti di rientro.
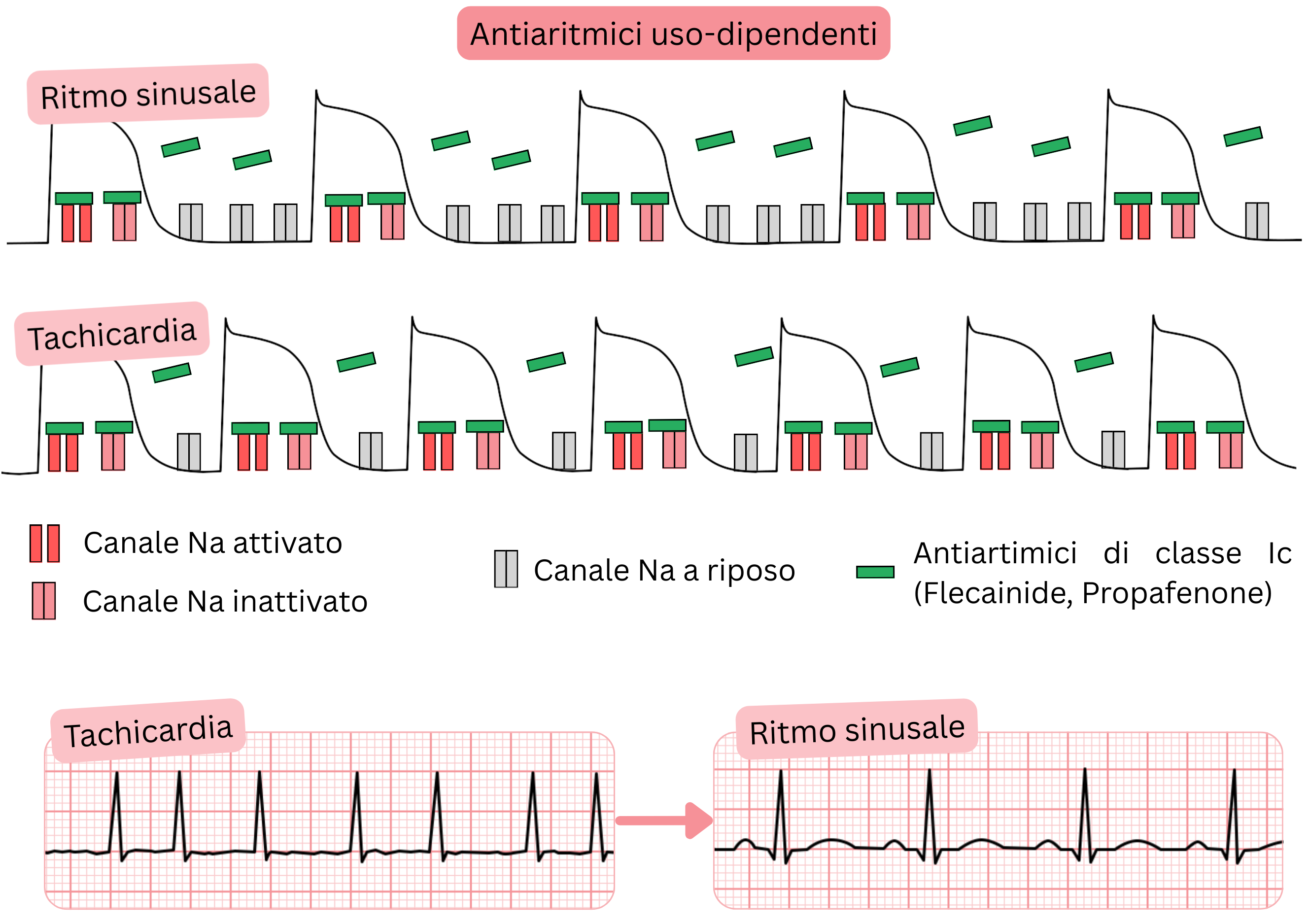
Farmaci antiaritmici use-dependent
- La use dependence si riferisce ai farmaci antiaritmici che si legano ai canali ionici
- in modo più intenso a frequenze cardiache elevate (> 90/min)
- Comprende i farmaci antiaritmici di Classe IC (Propafenone, Flecainide), che nella FA sono utilizzati per:
- cardioversione farmacologica della FA tachicardica (> 100/min) a ritmo sinusale
- mantenimento del ritmo sinusale (controllo del ritmo)
- Meccanismo d’azione (farmaci antiaritmici use-dependent):
- Si legano preferenzialmente ai canali Na⁺ attivati e inattivati
- Frequenza cardiaca più elevata (> 90/min) → maggiore grado di blocco (use dependence)
- Durante la tachicardia, la diastole (fase 4 del potenziale d’azione) si accorcia,
- per cui i canali Na⁺ rimangono più a lungo nello stato attivato o inattivato
- I farmaci antiaritmici di Classe IC rimangono pertanto legati ai canali Na⁺ più a lungo → maggiore effetto cumulativo.
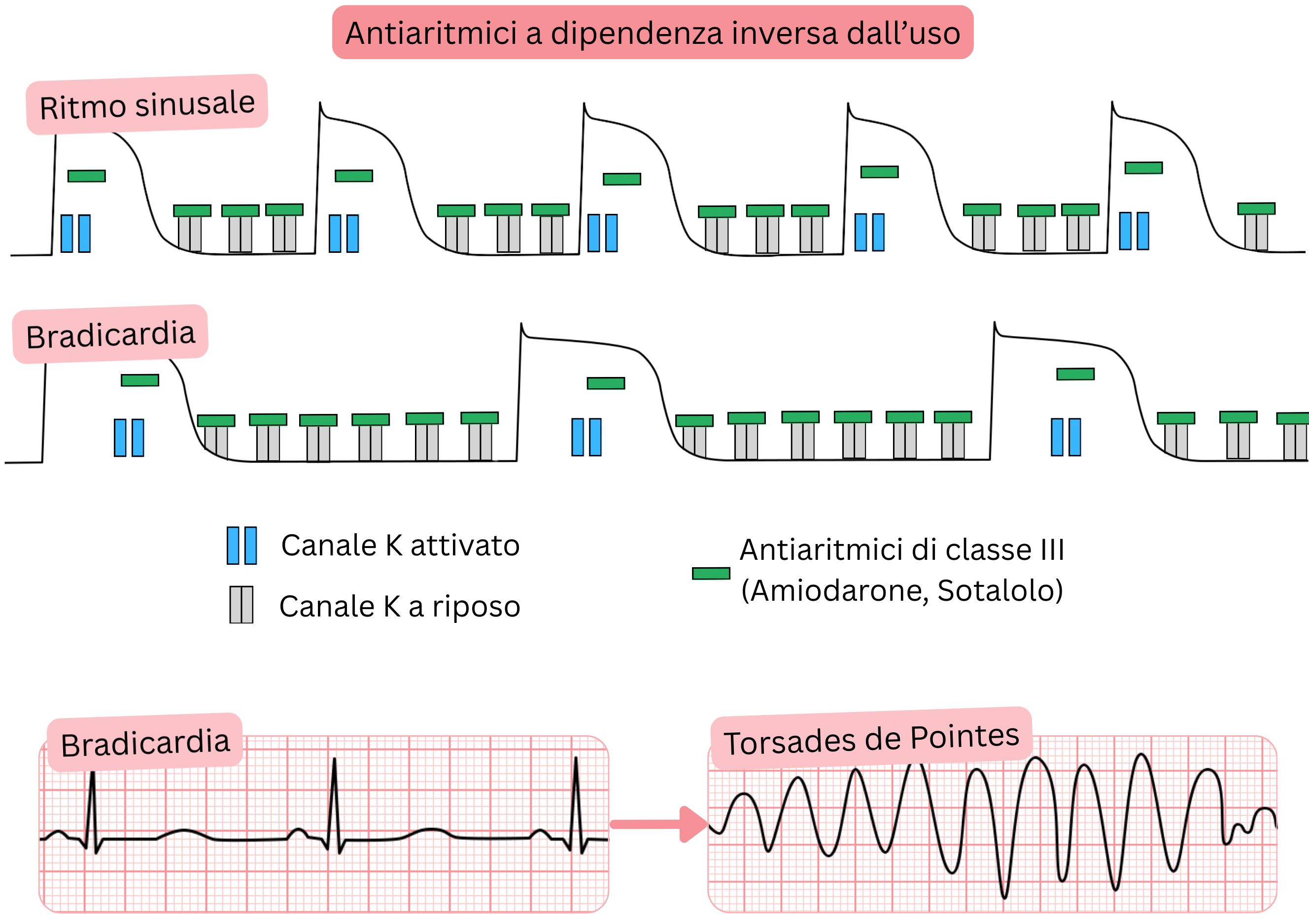
Farmaci antiaritmici reverse use-dependent
- La reverse use dependence si riferisce ai farmaci antiaritmici che si legano ai canali ionici
- in modo più intenso a frequenze cardiache basse (< 90/min)
- Comprende i farmaci antiaritmici di Classe III (Sotalolo – più potente, Amiodarone, Dronedarone)
- Nella FA sono utilizzati per:
- mantenimento del ritmo sinusale (controllo del ritmo)
- Meccanismo d’azione (farmaci antiaritmici reverse use-dependent):
- Si legano preferenzialmente ai canali K⁺ (fase 4) e li bloccano
- Successivamente, i canali K⁺ risultano bloccati anche nella fase 3, con conseguente prolungamento dell’intervallo QT
- Frequenza cardiaca più bassa (bradicardia) → maggiore grado di blocco (reverse use dependence)
- A frequenze cardiache più lente, la diastole (fase 4) e l’intero potenziale d’azione (fase 3) risultano prolungati
| Farmaci antiaritmici con use dependence e reverse use dependence |
| Classe |
Farmaci antiaritmici |
Meccanismo |
Tipo |
Effetto ECG |
Quando sospendere |
| I A |
Chinidina,
procainamide,
disopiramide |
Blocco dei canali Na⁺ e K⁺ |
Use dependence |
↑ QT;
↑ QRS/PR (± lieve) |
QTc > 500 ms o
ΔQTc > 60 ms;
QRS ↑ ≥ 25 % o
> 120 – 130 ms |
| I B |
Lidocaina,
mexiletina |
Blocco dei canali Na⁺ (tessuto ischemico) |
Use dependence |
↓ QT;
QRS ≈;
PR ≈ |
QRS ↑ ≥ 25 % rispetto al basale
o BBB |
| I C |
Flecainide,
propafenone |
Blocco potente dei canali Na⁺ |
Use dependence |
↑ QRS;
QT ≈;
PR ≈/↑ |
QRS ↑ ≥ 25 % o
> 120 – 130 ms;
PR > 240 ms;
nuovo BBB/blocco AV |
| III |
Sotalolo,
dofetilide,
ibutilide |
Blocco dei canali K⁺ |
Reverse use dependence |
↑ QT (rischio di TdP a FC < 50/min) |
QTc > 500 ms o ΔQTc > 60 ms;
FC < 50 – 60/min |
| III |
Amiodarone |
Blocco dei canali K⁺, Na⁺, Ca²⁺ + β-blocco |
Reverse use dependence (lieve) |
↑ QT (lieve);
± ↑ PR/QRS |
QTc > 500 ms;
FC < 50/min;
blocco AV, BBB |
| III |
Dronedarone |
Blocco dei canali K⁺, Na⁺, Ca²⁺ + β-blocco (più debole) |
Reverse use dependence (lieve) |
↑ QT (lieve) |
QTc > 500 ms;
FC < 50/min;
blocco AV, BBB |
BBB – Blocco di branca (RBBB o LBBB), TdP – Torsione di punta
Il sistema nervoso autonomo presenta due componenti principali antagoniste:
- Sistema nervoso simpatico
- Sistema nervoso parasimpatico

Sistema nervoso simpatico
- I principali mediatori del sistema nervoso simpatico sono le catecolamine, che si legano ai recettori adrenergici
- Catecolamine (adrenalina, noradrenalina, dopamina)
- Recettori adrenergici (α1, α2, β1, β2, β3)
- Per i farmaci antiaritmici, i recettori beta sono particolarmente rilevanti:
- β1 – localizzati nel cuore, prevalentemente nel nodo SA e in misura minore nel nodo AV
- β2 – localizzati nei bronchi, nei polmoni e nei vasi
- Il sistema nervoso simpatico è principalmente modulato dai farmaci antiaritmici di Classe II (beta-bloccanti)

Sistema nervoso parasimpatico
- Il principale nervo parasimpatico è il nervo vago
- Innerva le pupille, le ghiandole salivari, i bronchi, il tratto gastrointestinale, la vescica urinaria e il cuore
- Nel cuore, il vago innerva prevalentemente il nodo AV e in misura minore il nodo SA; innerva inoltre il miocardio atriale e minimamente i ventricoli
- Il nodo SA è innervato dal vago destro
- Il nodo AV è innervato dal vago sinistro
- pertanto, per l’interruzione della tachicardia sopraventricolare (AVNRT, AVRT), il massaggio del seno carotideo sinistro è più efficace.
- Il sistema nervoso parasimpatico è principalmente influenzato dalla digossina
| Sistema nervoso autonomo e farmaci antiaritmici |
| Farmaci |
Effetto sul sistema nervoso |
Meccanismo |
Effetto |
| β-bloccanti |
Inibiscono il tono simpatico |
Blocco recettori β1 (± β2) |
↓ frequenza SA; ↓ conduzione AV |
| Digossina |
Stimola il tono parasimpatico |
↑ tono vagale |
↓ conduzione AV; ± ↓ frequenza SA |









