Les concepts et principes suivants sont essentiels pour le traitement pharmacologique antiarythmique de la fibrillation atriale (FA) :
- Potentiel d’action
- Potentiel d’action nodal
- Potentiel d’action non nodal
- Médicaments antiarythmiques à dépendance d’usage (Classe IC – Propafénone, Flécaïnide)
- Médicaments antiarythmiques à dépendance inverse d’usage (Classe III – Sotalol – le plus marqué, Amiodarone, Dronédarone)
- Période réfractaire efficace (Classe III et IA)
- Système nerveux autonome
- Système nerveux sympathique (Classe II – bêtabloquants)
- Système nerveux parasympathique (Digoxine)
Potentiel d’action
- Chaque cardiomyocyte possède une différence de potentiel électrique entre les faces externe et interne de la membrane.
- Ce potentiel résulte de concentrations ioniques différentes (principalement Na⁺, K⁺ et Ca²⁺) de part et d’autre de la membrane
- et de sa perméabilité sélective maintenue par la Na⁺/K⁺-ATPase.
- Au cours du cycle cardiaque, les ions traversent la membrane et le potentiel électrique se modifie en conséquence.
- La variation du potentiel électrique au cours du cycle cardiaque est représentée par la courbe du potentiel d’action (PA).
- Le PA naît spontanément au niveau du nœud sinusal (SA) puis se propage aux cardiomyocytes adjacents des oreillettes.

Potentiel d’action nodal
- Également appelé potentiel d’action pacemaker (PA).
- Il est présent au niveau du nœud sinusal (SA) et du nœud auriculo-ventriculaire (AV), d’où le terme de PA nodal.
- Il est spontané, c’est-à-dire qu’une dépolarisation spontanée se produit de façon répétée.
- La dépolarisation spontanée est médiée par les courants If, au cours desquels les ions Na⁺ traversent la membrane.
- Il s’agit d’un PA lent, car les ions Ca²⁺ traversent la membrane lentement lors de la dépolarisation.
- Il présente un début lent (dépolarisation) mais une durée courte, permettant la génération rapide d’un nouveau PA.
- Il comporte 3 phases (4, 0, 3), au cours desquelles des ions spécifiques traversent la membrane à chaque phase.
| Potentiel d’action nodal et médicaments antiarythmiques |
| Médicament |
Classe |
Mécanisme |
Nœud SA |
Nœud AV |
| β-bloquants |
II |
↓ tonus sympathique |
↓ fréquence |
↓ conduction |
| Antagonistes calciques |
IV |
Blocage des canaux Ca²⁺ |
↓ fréquence |
↓ conduction |
| Digoxine |
– |
↑ tonus parasympathique |
↓ fréquence |
↓ conduction |
| Ivabradine |
– |
Blocage du courant If |
↓ fréquence |
– |

Potentiel d’action non nodal
- Également appelé potentiel d’action non pacemaker (PA).
- Il est présent dans le myocarde de travail des oreillettes, des ventricules et dans les fibres de Purkinje.
- Il ne se dépolarise pas spontanément ; il nécessite un PA provenant d’un cardiomyocyte adjacent pour être déclenché.
- Il est rapide, car les ions Na⁺ traversent la membrane rapidement lors de la dépolarisation.
- Il comporte 5 phases (0, 1, 2, 3, 4), au cours desquelles des ions spécifiques traversent la membrane à chaque phase.
| Potentiel d’action non nodal (PA) et médicaments antiarythmiques |
| Médicament |
Classe |
Mécanisme |
PA |
ECG (QRS/QT) |
| Quinidine, Procainamide, Disopyramide |
I A |
Blocage des canaux Na⁺ + K⁺ |
↑ PA |
↑ QT |
| Lidocaïne, Mexilétine |
I B |
Blocage des canaux Na⁺ (tissu ischémique) |
↓ PA |
↓ QT |
| Flécaïnide, Propafénone |
I C |
Blocage puissant des canaux Na⁺ |
≈ PA |
↑ QRS, QT ≈ |
| Amiodarone, Sotalol, Dronédarone |
III |
Blocage des canaux K⁺ |
↑ PA |
↑ QT |
Le PA non nodal se propage progressivement du nœud SA à travers le myocarde auriculaire, et la dépolarisation auriculaire (phase 0) apparaît sur l’ECG sous la forme de l’onde P. L’onde de dépolarisation traverse les oreillettes en < 100 ms ; la durée de l’onde P est donc < 100 ms.
Le PA non nodal se propage des oreillettes à travers le nœud AV vers les fibres de Purkinje et les ventricules. La dépolarisation ventriculaire (phase 0) apparaît sur l’ECG sous la forme du complexe QRS. L’onde de dépolarisation traverse les ventricules en < 110 ms ; la durée du QRS est donc < 110 ms.

Période réfractaire efficace (PRE)
- Temps écoulé entre le début de la dépolarisation (phase 0) et presque la fin de la repolarisation (phase 3)
- Durant la PRE, aucune nouvelle dépolarisation, c’est-à-dire aucun nouveau potentiel d’action, ne peut survenir dans les cardiomyocytes,
- car les canaux Na⁺ doivent revenir à l’état de repos après la dépolarisation avant de pouvoir être réactivés.
- La durée de la PRE se reflète sur l’ECG par l’intervalle QT.
- L’intervalle QT représente la durée du PA non nodal
- La PRE (intervalle QT) est prolongée principalement par les antiarythmiques de Classe IA et de Classe III,
- car ils bloquent les canaux K⁺ et ralentissent ainsi la repolarisation.
- Une PRE plus longue signifie que le myocarde reste inexitable plus longtemps, ce qui empêche la repropagation rapide des impulsions
- réduisant ainsi la fréquence ventriculaire maximale en cas de FA tachycardique et
- prévenant les phénomènes de réentrée.
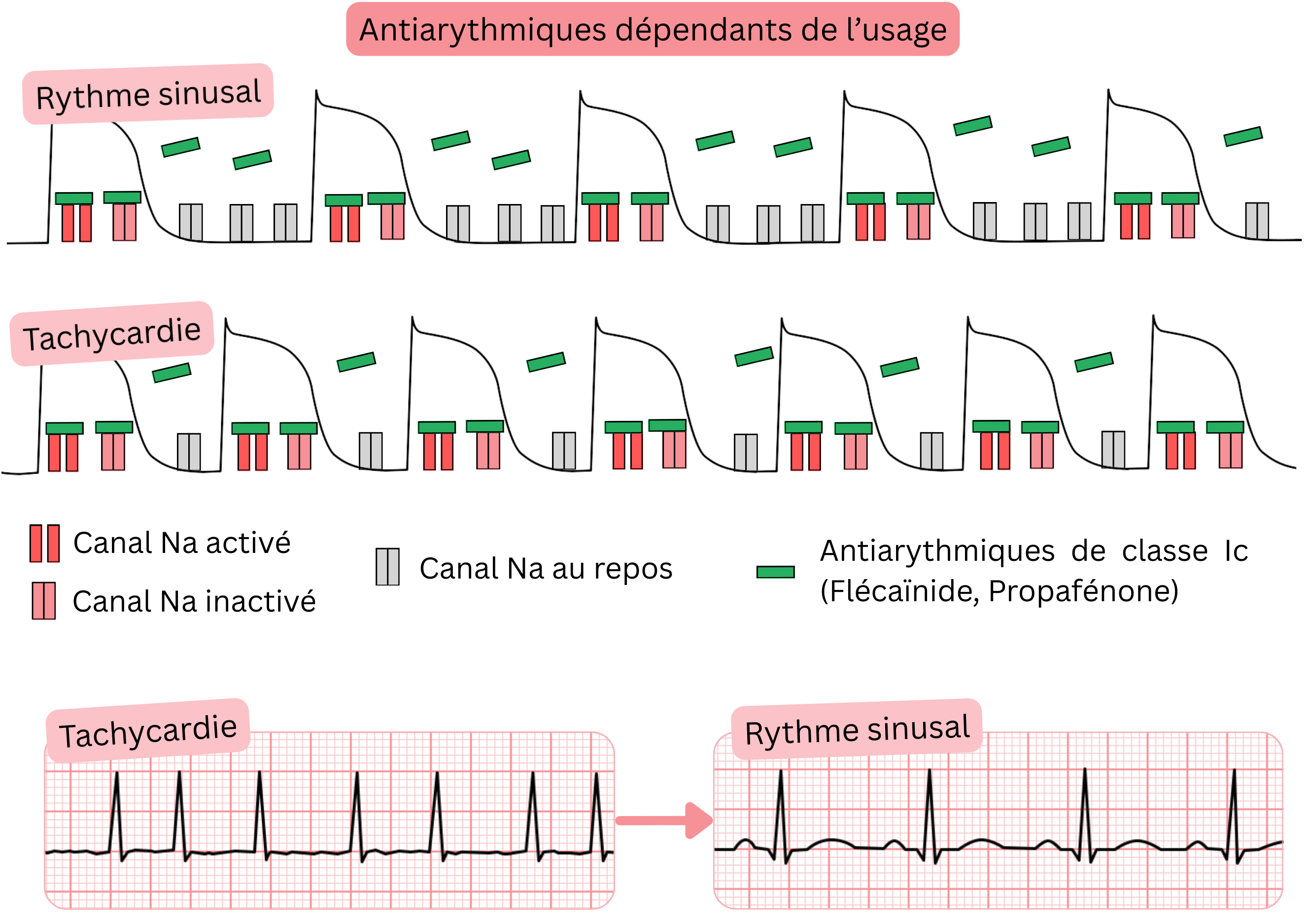
Médicaments antiarythmiques à dépendance d’usage
- La dépendance d’usage désigne des antiarythmiques qui se lient aux canaux ioniques
- plus intensément à des fréquences cardiaques élevées (> 90/min)
- Il s’agit des antiarythmiques de Classe IC (Propafénone, Flécaïnide), utilisés dans la FA pour :
- la cardioversion pharmacologique d’une FA tachycardique (> 100/min) en rythme sinusal
- le maintien du rythme sinusal (contrôle du rythme)
- Mécanisme d’action (antiarythmiques à dépendance d’usage) :
- Ils se lient préférentiellement aux canaux Na⁺ activés et inactivés
- Fréquence cardiaque élevée (> 90/min) → degré de blocage plus important (dépendance d’usage)
- Lors d’une tachycardie, la diastole (phase 4 du PA) est raccourcie,
- de sorte que les canaux Na⁺ restent plus longtemps à l’état activé ou inactivé
- Les antiarythmiques de Classe IC restent donc liés plus longtemps aux canaux Na⁺ → effet cumulatif plus important.
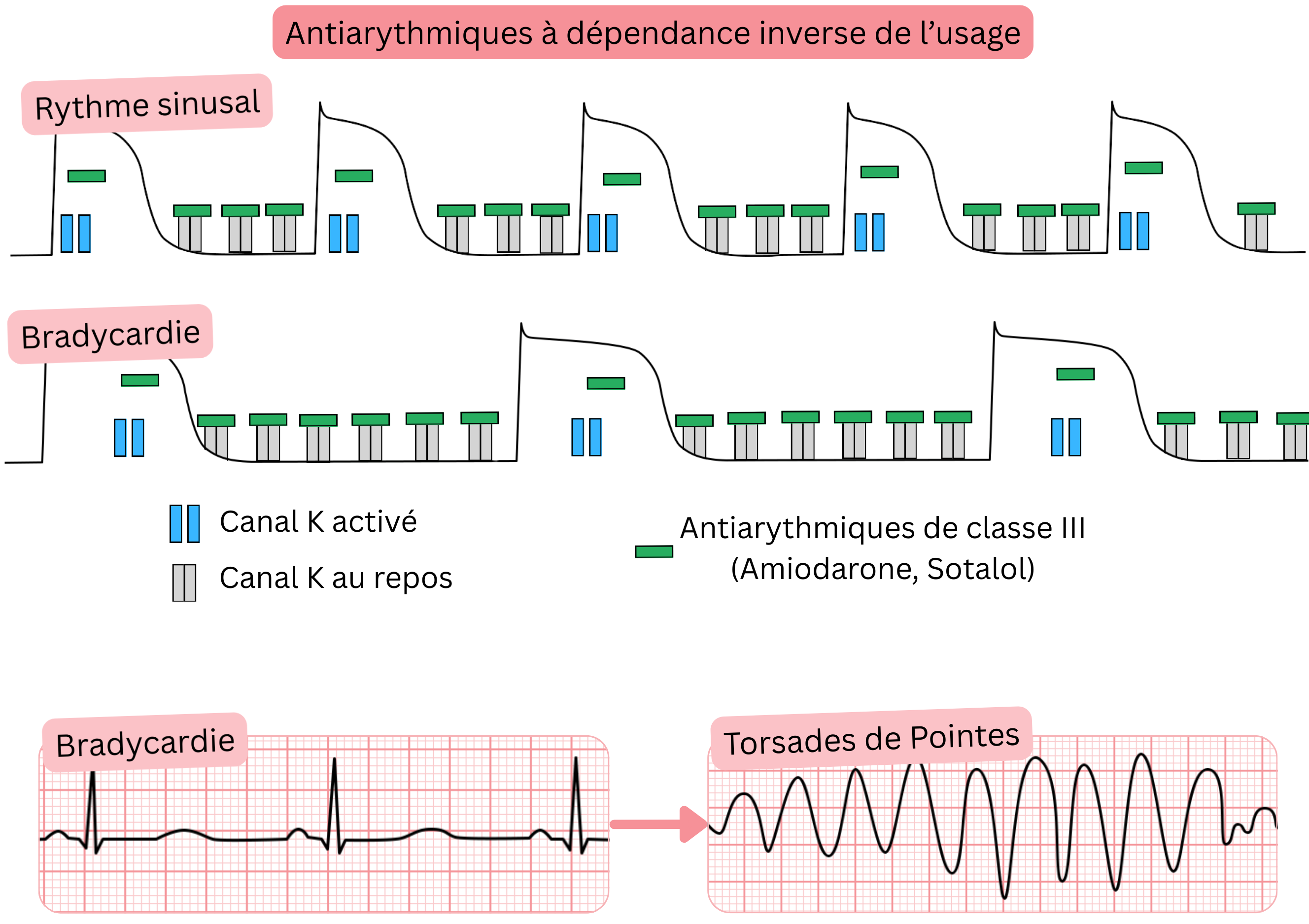
Médicaments antiarythmiques à dépendance inverse d’usage
- La dépendance inverse d’usage désigne des antiarythmiques qui se lient aux canaux ioniques
- plus intensément à des fréquences cardiaques basses (< 90/min)
- Il s’agit des antiarythmiques de Classe III (Sotalol – le plus marqué, Amiodarone, Dronédarone)
- Dans la FA, ils sont utilisés pour :
- le maintien du rythme sinusal (contrôle du rythme)
- Mécanisme d’action (antiarythmiques à dépendance inverse d’usage) :
- Ils se lient préférentiellement aux canaux K⁺ (phase 4) et les bloquent
- Les canaux K⁺ sont ensuite également bloqués en phase 3, entraînant un allongement de l’intervalle QT
- Fréquence cardiaque basse (bradycardie) → degré de blocage plus important (dépendance inverse d’usage)
- À des fréquences cardiaques plus lentes, la diastole (phase 4) et l’ensemble du PA (phase 3) sont prolongés
| Dépendance d’usage et dépendance inverse d’usage des antiarythmiques |
| Classe |
Antiarythmiques |
Mécanisme |
Type |
Effet ECG |
Quand arrêter |
| I A |
Quinidine,
procainamide,
disopyramide |
Blocage des canaux Na⁺ et K⁺ |
Dépendance d’usage |
↑ QT;
↑ QRS/PR (± léger) |
QTc > 500 ms ou
ΔQTc > 60 ms;
QRS ↑ ≥ 25 % ou
> 120 – 130 ms |
| I B |
Lidocaïne,
mexilétine |
Blocage des canaux Na⁺ (tissu ischémique) |
Dépendance d’usage |
↓ QT;
QRS ≈;
PR ≈ |
QRS ↑ ≥ 25 % par rapport au basal
ou BBG/BBD |
| I C |
Flécaïnide,
propafénone |
Blocage puissant des canaux Na⁺ |
Dépendance d’usage |
↑ QRS;
QT ≈;
PR ≈/↑ |
QRS ↑ ≥ 25 % ou
> 120 – 130 ms;
PR > 240 ms;
nouveau BBG/BAV |
| III |
Sotalol,
dofétilide,
ibutilide |
Blocage des canaux K⁺ |
Dépendance inverse d’usage |
↑ QT (risque de TdP si FC < 50/min) |
QTc > 500 ms ou ΔQTc > 60 ms;
FC < 50 – 60/min |
| III |
Amiodarone |
Blocage des canaux K⁺, Na⁺, Ca²⁺ + β-bloquant |
Dépendance inverse d’usage (modérée) |
↑ QT (modéré);
± ↑ PR/QRS |
QTc > 500 ms;
FC < 50/min;
BAV, BBG/BBD |
| III |
Dronédarone |
Blocage des canaux K⁺, Na⁺, Ca²⁺ + β-bloquant (plus faible) |
Dépendance inverse d’usage (modérée) |
↑ QT (modéré) |
QTc > 500 ms;
FC < 50/min;
BAV, BBG/BBD |
BBB – Bloc de branche (BBD ou BBG), TdP – Torsades de pointes
Le système nerveux autonome comporte deux composantes principales opposées :
- Système nerveux sympathique
- Système nerveux parasympathique

Système nerveux sympathique
- Les principaux médiateurs du système sympathique sont les catécholamines, qui se lient aux récepteurs adrénergiques
- Catécholamines (adrénaline, noradrénaline, dopamine)
- Récepteurs adrénergiques (α1, α2, β1, β2, β3)
- Pour les antiarythmiques, les récepteurs β sont particulièrement pertinents :
- β1 – localisés au niveau cardiaque, principalement dans le nœud SA et dans une moindre mesure dans le nœud AV
- β2 – localisés dans les bronches, les poumons et les vaisseaux
- Le système sympathique est principalement ciblé par les antiarythmiques de Classe II (bêtabloquants)

Système nerveux parasympathique
- Le principal nerf parasympathique est le nerf vague
- Il innerve les pupilles, les glandes salivaires, les bronches, le tractus gastro-intestinal, la vessie et le cœur
- Au niveau cardiaque, le nerf vague innerve principalement le nœud AV et dans une moindre mesure le nœud SA ; il innerve également le myocarde auriculaire et très peu les ventricules
- Le nœud SA est innervé par le nerf vague droit
- Le nœud AV est innervé par le nerf vague gauche
- ainsi, pour interrompre une tachycardie supraventriculaire (AVNRT, AVRT), le massage du sinus carotidien gauche est plus efficace.
- Le système parasympathique est principalement influencé par la digoxine
| Système nerveux autonome et médicaments antiarythmiques |
| Médicaments |
Effet sur le système nerveux |
Mécanisme |
Effet |
| β-bloquants |
Inhibent le tonus sympathique |
Blocage des récepteurs β1 (± β2) |
↓ fréquence SA ; ↓ conduction AV |
| Digoxine |
Stimule le tonus parasympathique |
↑ tonus vagal |
↓ conduction AV ; ± ↓ fréquence SA |









